
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Оформите библиографическое описание источников 40 страница
|
|
|
|
CaC2 + 2H2O = Ca(OH)2 + H2C2
H2C2 + 2HCl = CH3CHCl2
Задача 2.
Из бинарных соединений натрия при взаимодействии с водой газ будут образовывать гидрид, карбид, нитрид, фосфид. Соответственно, продуктами взаимодействия с водой могут быть водород, ацетилен, аммиак и фосфин. Поскольку относительная плотность выделяющегося при взаимодействии с водой газа равна 1,30, молярная масса этого газа составляет М = 1,30 · 20 = 26 г/моль. Данному условию отвечает ацетилен, С2Н2.
По-видимому, второй газ поглощается кислотой. Из указанных выше вариантов основные свойства проявляет только аммиак. Следовательно, исходная смесь состояла из карбида и нитрида натрия.
Na3N + 3H2O = 3NaOH + NH3
Na2C2 + 2H2O = 2NaOH + C2H2
2Na3N + 4H3PO3 = 3Na2HPO3 + (NH4)2HPO3
Na2C2 + H3PO3 = Na2HPO3 + C2H2
Определим мольное соотношение нитрида и карбида натрия. Пусть мольная доля аммиака в смеси газообразных продуктов составляет х. Тогда:
17х +26 · (1-х) = 1,00 · 20 = 20
Х = 2/3, т.е., на 2/3 моль нитрида натрия приходится 1/3 моль карбида.
Тогда массовая доля нитрида натрия составит
2/3 · 83: (2/3 · 83 + 1/3 · 70) = 70,3%
Массовая доля карбида натрия – 29,7%.
Задача 3.
При электролизе будет протекать процесс:
2HBr = H2 + Br2
Полученный бром будет взаимодействовать с раствором поташа:
3K2CO3 + Br2 = 5KBr + KBrO3 + 3CO2
В исходном растворе хлороводорода присутствовало 200 · 1,15 · 0,15: 81 = 0,426 моль HBr. Для получения 1 моль брома требуется 96500 · 2 = 193000 Кл. По условию задачи через раствор пропустили 7 000 Кл электричества, следовательно, бромоводород в недостатке. В результате электролиза получилось 7000: 193000 = 0,036 моль брома.
В растворе поташа присутствовало 200 · 0,08: 138 = 0,116 моль карбоната калия. По-видимому, бром взят в недостатке. Тогда в результате реакции получится 0,18 моль бромида калия и 0,036 моль бромата калия, а также останется 0,01 моль карбоната калия.
Масса сухого остатка составит
m = 0,18 · 110 + 0,036 · 167 + 0,01 · 138 = 27,192 г
Задача 4.
Запишем кинетическое уравнение реакции.
V = k[CH3CHO]2
Понижение давления равнозначно уменьшению концентрации газообразных веществ. Следовательно, концентрация стала равна (0,72:1,5)[CH3CHO] = 0,48[CH3CHO].
V’ = k[CH3CHO]’2 = k∙0,482[CH3CHO]2 = 0,2304V
По условию также увеличили температуру на 20 oС. По правилу Вант-Гоффа:
V’ = V∙gDT/10 = V∙2,22 = 4,84V
В результате скорость реакции увеличится в 0,2304∙4,84 = 1,12 раза.
Схема катализа:
СН3СНО + I2 → СН3I + НI + СО
СН3I + НI → СН4 + I2
Ответ: скорость реакции увеличится в 1,12 раза.
Задача 5.
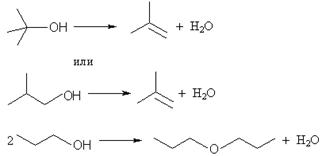
Кислотная дегидратация спиртов приводит к образованию алкенов или простых эфиров (только в случае первичных спиртов). Рассмотрим возможные случаи образования продуктов в температурном интервале нагревания до 140 oС (тогда исключается возможность образования алкенов из первичных спиртов):
1) первичный (1)/первичный (2) – эфир (1), эфир(2), эфир (3) – продукт перекрестной дегидратации: образуется 3 продукта, противоречит условию;
2) вторичный (1)/ вторичный (2) – алкен (1), алкен (2); для случаев третичный (1)/третичный (2) и вторичный/третичный аналогично: массовая доля углерода 12n: 14n = 6/7 есть величина постоянная для любого алкена (CnH2n), противоречит условию;
3) первичный/ вторичный – эфир, алкен; для случая первичный/третичный аналогично – удовлетворяет условию.
Легко показать, что массовая доля углерода в любом эфире всегда меньше, чем в алкене. Общая формула эфира CnH2n+2O, ω(C) = 12n: (14n + 18) = 6/7 – 0,151. Решая это уравнение, получим n = 6. В спирте число атомов углерода в 2 раза меньше. Таким образом, один из спиртов н-C3H7OH.
ω(C в н-C3H7OH) = 100∙12∙3: 60 = 60%, тогда ω(C в CmH2m + 2O) = (60 ± 4,9)% = 100∙12m: (14m + 18). Решая два уравнения, получим, m = 2,3 и m = 4. m должно быть натуральным числом, т.е. m = 4. Второй спирт – t-C4H9OH или i-C4H9OH.
Задача 6.
Пусть Х – доля минорного компонента. По выражению для константы равновесия: 0,11=Х: (1-Х), Х=0,099, т.е 9,9% и 90,1%. Наиболее термодинамически стабилен 2-бромпропан, он будет в избытке.
Одним из удобных способов синтеза является следующий:
CaC2 + 2H2O = HC≡CH + Ca(OH)2
Al4C3 + 12HCl = 3CH4 + 4AlCl3
CH4 + Br2 = CH3Br
HC≡CH + NaNH2 = HC≡CNa + NH3 (вместо NaNH2 можно использовать Na)
HC≡CNa + CH3Br = HC≡CCH3 + NaBr
HC≡CCH3 + H2 = H2C=CHCH3 (реакция идет в присутствии каталитически активного Pd)
H2C=CHCH3 + HBr = H3CCHBrCH3
Однако возможны и другие пути синтеза.
Составляя RFC, инициатор изменения должен по мере возможности предоставить не менее чем описанную ниже информацию.
· Имя инициатора изменения, должность и контактная информация.
· Описание изменения, т.е. полный отчет о характере изменения.
· Предложение, касающееся назначения изменению приоритета и категории, которое основано на имеющейся информации.
· Номер отчета о проблеме (Problem Report — PR), относящийся к любой проблеме, которая касается этого изменения, или номера инцидентов, если они известны.
· Описание и идентификация любых элементов, подлежащих изменению, включая идентификацию конфигурационных единиц.
· Причина для внесения изменения.
· Анализ затрат и результатов, связанных с изменением, и резолюция бюджетного органа, если она является необходимой.
· Последствия, связанные с отказом от реализации изменение, включая любые соглашения об уровне сервиса, риск нарушения которых может быть вызван этим отказом.
· Оценка воздействия и ресурсов, т.е. описание того, какие пользователи будет затронуты этим изменением и насколько значительным окажется его результат.
· Обозначение релиза, к которому относится изменение, и предлагаемый план реализации с обозначением временных этапов.
· План восстановления того положения, которое предшествовало внесению изменения, с описанием предпосылок принятия решения об отмене изменения и указанием контактной информации лица, принимающего решение.
· Описание влияния на бесперебойную работу компании и планы действий в чрезвычайных обстоятельствах.
· Риск, связанный с внесением изменения.
От инициатора изменения может также потребоваться предоставление вспомогательной документации, такой как бизнес оценка, анализ затрат и результатов или предлагаемый план реализации для менеджера изменений и других лиц, участвующих в процессе утверждения изменения.
Два из элементов RFC в списке инициатора изменений (рекомендуемый или предлагаемый приоритет и категория изменения) заслуживают более подробного описания.
Приоритет изменения
При рассмотрении определения приоритета часто возникает определенная путаница; например, в словарном определении указано: “Степень предшествования, при определении которой особое значение придается порядку значимости или безотлагательности”.
В процессе управления изменениями безотлагательность определяется тем, насколько быстро требуется внести изменение на деловом предприятии.
Ниже перечислены четыре рекомендуемых уровня приоритетов.
· Экстренный приоритет. Таковым является изменение, которое, не будучи немедленно реализовано, оставит организацию подверженной огромному риску. Например, к изменению с таким приоритетом относится установка патча в системе обеспечения безопасности.
· Высокий приоритет. Изменением с таким приоритетом является изменение, важное для организации, которое должно быть вскоре реализовано. В качестве примера можно указать обновление, продиктованное вводом в действие новых требований законодательства.
· Средний приоритет. Изменение, которое должно быть реализовано в целях получения преимуществ в связи с модификацией сервиса. Например, обновление, применяемое между сменами версий в ответ на пожелания службы обратной связи с заказчиком.
· Низкий приоритет. Изменение, которое не является срочным, но может оказаться выгодным. Примером такого изменения может стать дополнение к профилю пользователя, которое предусмотрено в связи с пожеланиями, высказанными пользователями.
Эти уровни приоритетов определены в соответствии с наилучшими рекомендациями, выработанными в данной отрасти промышленности. Тем не менее, в зависимости от размеров организации, ее структуры и основополагающих SLA, существующих между ИТ отделом и деловым предприятием, которое он обслуживает, организациям может потребоваться модифицировать эти определения приоритетов и ввести собственные определения. Например, в некоторых организациях установлена такая практика, что если какое-то лицо, желающее внести дополнение к своему профилю пользователя, работает в области, важной с точки зрения функционирования предприятия, то указанное изменение может рассматриваться как имеющее высокий приоритет. И наоборот, если такое же изменение затребовано представителем той части делового предприятия, деятельность которой постепенно сворачивается, то изменение может рассматриваться как имеющее низкий приоритет. Важно, чтобы каждая организация предусмотрела правильное использование этих приоритетов для своей собственной среды, поскольку от этих приоритетов зависит, когда и как должно быть реализовано изменение. Приоритеты определяют также порядок рассмотрения запроса на изменение.
|
|
|
|
|
Дата добавления: 2015-01-04; Просмотров: 296; Нарушение авторских прав?; Мы поможем в написании вашей работы!