
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Поляризаця электродов
|
|
|
|
На электроде гальванического элемента, находящемся в равновесии, постоянно протекают химические реакции (см. Ток обмена). Если начать поляризацию электрода (например, повышая или понижая его потенциал, что вызывает прохождение электрического тока через границу раздела электрод — раствор), то, после определённого периода протекания неравновесных процессов, строение двойного электрического слоя изменится. При этом, в соответствии с поляризационной кривой, изменится и электродный потенциал рассматриваемого электрода. Отклонение потенциала от равновесного под действием внешнего потенциала (или при протекании тока) называется электрохимической поляризацией электрода.
Величина отклонения потенциала электрода от равновесного значения называется перенапряжением. Исследование перенапряжения позволяет понять механизмы электрохимических реакций в данной системе. Оно проводится с помощью потенциостатов, также используется осциллография, метод вращающегося дискового электрода
65. Виды поляризации:
Концентрационная поляризация обусловлена замедленным переносом исходных или конечных компонентов, протекающих на электроде реакций. В результате, концентрации исходных веществ в зоне реакции понижаются, а конечных - повышаются. Это смещает равновесие в сторону обратной реакции. Приложение дополнительной разности потенциалов (поляризация) увеличивает скорость переноса компонентов и компенсирует нежелательные процессы. Концентрационная поляризация уменьшается при перемешивании раствора, т.к. это ускоряет выравнивание концентраций компонентов на поверхности электродов.
Электрохимическая поляризация (перенапряжение) обусловлена пониженной скоростью электрохимических реакций на электроде. Скорость электрохимических реакций может быть повышена увеличением температуры и использованием катализатора, а также при повышении потенциала электрода по сравнению с его равновесным значением, т.е. при поляризации. Роль поляризации сводится к уменьшению энергии активации и величина этого снижения пропорциональна величине поляризации. Уменьшение энергии активации сопровождается увеличением скорости реакции, что в случае электрохимических процессов ведет к увеличению плотности тока.
66. Количественные характеристики электролиза выражаются двумя законами Фарадея:
1) Масса вещества, выделяющегося на электроде, прямо пропорциональна количеству электричества, прошедшего через электролит.
2) Для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорционально эквивалентной массе элемента. Эквивалентной массой вещества является его молярная масса, делённая на целое число, зависящее от химической реакции, в которой участвует вещество.
Законы Фарадея можно записать в виде следующей формулы:
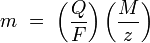
где:
m — масса осаждённого на электроде вещества в граммах
Q — полный электрический заряд, прошедший через вещество
F = 96,487 C mol−1 — постоянная Фарадея
M — молярная масса вещества
z — валентное число ионов вещества (число электронов на один ион).
Заметим, что M/z — это эквивалентная масса осаждённого вещества.
Для первого закона Фарадея M, F и z являются константами, так что чем больше величина Q, тем больше будет величина m. Для второго закона Фарадея Q, F и z являются константами, так что чем больше величина M/z (эквивалентная масса), тем больше будет величина m. В простейшем случае постоянного тока электролиза Q = It приводит к:
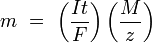 и тогда
и тогда 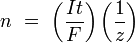 ,где:
,где:
n — выделенное количество вещества («количество молей»): n = m/M
t — время действия постоянного тока.
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, который возникает при прохождении электрического тока через раствор либо расплав электролита. Упорядоченное движение ионов в проводящих жидкостях происходит в электрическом поле, которое создается электродами — проводниками, соединёнными с полюсами источника электрической энергии. Анодом при электролизе называется положительный электрод, катодом — отрицательный. Положительные ионы — катионы — (ионы металлов, водородные ионы, ионы аммония и др.) — движутся к катоду, отрицательные ионы — анионы — (ионы кислотных остатков и гидроксильной группы) — движутся к аноду.
|
|
|
|
|
Дата добавления: 2014-12-24; Просмотров: 485; Нарушение авторских прав?; Мы поможем в написании вашей работы!