
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные технологические показатели химико-технологического процесса
|
|
|
|
Химико-технологический процесс и его содержание
Химико-технологический процесс представляет собой совокупность операций, позволяющих получить целевой продукт из исходного сырья. Некоторые из этих операций необходимы для подготовки исходных реагентов к проведению химической реакции, перевода их в наиболее реакционноспособное состояние. Например, известно, что скорость химических реакций сильно зависит от температуры, поэтому часто реагенты до проведения реакции нагревают. Чтобы устранить побочные явления и получить продукт высокого качества, исходное сырье подвергают очистке от посторонних примесей, пользуясь методами основанными на различии физических свойств (растворимость в различных растворителях, плотность, температуры конденсации и кристаллизации и т.д.). При очистке сырья и реакционных смесей широко применяют явления тепло- и массообмена, гидромеханические процессы. Возможно также использование химических методов очистки, например, химических реакций, в результате которых посторонние примеси превращаются в легкоотделимые вещества.
Соответствующим образом подготовленные реагенты подвергают химическому взаимодействию, включающему часто несколько этапов. В промежутках между этими этапами иногда необходимо вновь использовать тепломассообменные и другие физические процессы. Например, при производстве серной кислоты диоксид серы частично окисляют до триоксида, затем реакционную смесь охлаждают, извлекают из нее путем абсорбции триоксид серы и вновь направляют ее на окисление.
В результате химических реакций получают смесь продуктов (целевых побочных) и непрореагировавших реагентов. Заключительные операции связаны с разделением этой смеси, для чего вновь применяют гидромеханические, тепло- и массообменные процессы, например, фильтрование, центрифугирование, ректификацию, абсорбцию, экстракцию и т.д. Продукты реакции направляют на склад готовой продукции или на дальнейшую переработку; непрореагировавшее сырье вновь используют в процессе, организуя его рецикл. На заключительных этапах проводят также рекуперацию энергии и очистку промышленных выбросов, чтобы извлечь из отходящих газов и сточных вод все ценные компоненты, а также ликвидировать опасность загрязнения окружающей среды.
Таким образом, химико-технологический процесс в целом это сложная система, состоящая из единичных связанных между собой процессов (элементов) и взаимодействующая с окружающей средой. Элементами химико-технологической системы являются названные процессы тепло- и массообмена, гидромеханические, химические и т.д. Их рассматривают как единичные процессы химической технологии.
Важной подсистемой сложного химико-технологического процесса является химический процесс. Он представляет собой одну или несколько химических реакций, сопровождаемых тепло- и массообменными явлениями.
Анализ единичных процессов, их взаимного влияния позволяет разработать технологический режим.
Технологическим режимом называется совокупность параметров, определяющих условия работы аппарата или системы аппаратов.
Оптимальные условия ведения процесса – это сочетание основных параметров (температуры, давления, состава исходной реакционной смеси, катализатора и т.д.), позволяющее получить наибольший выход продукта с высокой скоростью или обеспечить наименьшую себестоимость.
Единичные процессы протекают в различных аппаратах – химических реакторах, абсорбционных и ректификационных колоннах, теплообменниках и т.д. Отдельные аппараты соединены в технологическую схему процесса. Разработка и построение рациональной технологической схемы – важная задача химической технологии.
Процесс создания химического производства складывается из следующих операций.
1) Разработка химико-технологического процесса.
2) Составление проектной документации.
3) Построение цеха, т.е. сооружение здания, монтаж оборудования, размещение аппаратов и приборов контроля и регулирования.
В курсе "Общая химическая технология" изучаются вопросы, посвященные главным образом решению первых двух задач, которые наиболее тесно связаны с сущностью химического производства. Но прежде следует ознакомиться с основными элементами химико-технологического процесса.
Показателем, характеризующим эффективность работы машин, аппаратов, цехов и заводов в целом, служит производительность. Производительность - это количество выработанного продукта или пере-работанного сырья в единицу времени t
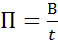 , (2.1)
, (2.1)
где П – производительность; В– количество продукта; τ – время.
Производительность измеряется в килограммах в час (кг/ч), тоннах в сутки (т/сут), или, кубических метрах в сутки (м3/сут) и т.д. Максимально возможная производительность называется мощностью.
Для сравнения работы аппаратов и установок различного устройства и размеров, в которых протекают одни и те же химические процессы, используется понятие интенсивность.
Интенсивность – это производительность, отнесенная к какой-либо величине, характеризующей размеры аппарата, – к его объему или сечению; она, например, может быть выражена в виде уравнения
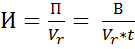 , (2.2)
, (2.2)
где Vr– объем аппарата (реактора).
Интенсивность может измеряться количеством продукта, получаемого в течение единицы времени с единицы объема аппарата. Например, (кг/ч⋅ м3), или с единицы сечения аппарата (т/сут⋅ м2) и т.д.
Расход сырья, воды, энергии и различных реагентов, отнесенный к единице целевого продукта, называют расходным коэффициентом b
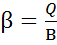 (2.3)
(2.3)
где Q – расход сырья реагента и др.
Расходные коэффициенты выражают в тоннах на тонну (т/т), кубических метрах на тонну (м3/т), киловатт-часах на тонну (кВт⋅ч /т) и т.п.
Глубина протекания реакции, от которой зависит степень использования сырья и другие показатели химико-технологического процесса, характеризуется степенью превращения и выходом продукта, а для сложных реакций, кроме того, селективностью.
Степень превращения – это отношение количества реагента, вступившего в реакцию, к его исходному количеству. Например, для простой необратимой реакции типа A → R степень превращения выражается уравнением
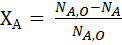 , (2.4)
, (2.4)
где XA – степень превращение реагента А; NA,0, NA– количество исходного реагента А в начале и в конце процесса.
Степень превращения выражают в долях процента, в последнем случае
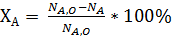 (2.5)
(2.5)
Из уравнения (2.4) следует, что
NA = NA,0 (1− XA). (2.6)
Если реакция протекает без изменения объема, то
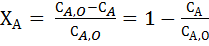 , (2.7)
, (2.7)
где CA,0, CA– концентрация исходного реагента A в начале и в конце процесса.
Из уравнения (2.7) находим, что
CA = CA ,0 (1− XA). (2.8)
Выход продукта – это отношение количества полученного целевого продукта к его количеству, которое должно быть получено по стехиометрическому уравнению.
Для необратимой реакция A → R имеем
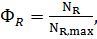 (2.9)
(2.9)
где ФR– выход целевого продукта; NR– количество продукта Rв конце процесса; NR, max – максимально возможное количество продукта R.
Однако в данном случае NR,max = N A,0; NR = NA,0 – NA, поэтому для необратимых процессов
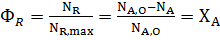 (2.10)
(2.10)
Для обратимых реакций важным понятием является равновесная степень превращения; для реакции A ↔ Rона описывается уравнением
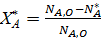 , (2.11)
, (2.11)
где X*A– равновесная степень превращения; N*A– количество исходного реагента Ав состоянии равновесия.
Для обратимых реакций NR, max = N*R, поэтому
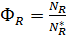 , (2.12)
, (2.12)
где N*R– количество продукта R в состоянии равновесия.
Но NR = NA,0 − NA, а N*R= NA,O∙X*A, поэтому из уравнения (2.12) следует, что для обратимой реакции
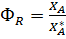 (2.13)
(2.13)
Селективностью называется отношение количества целевого продукта к общему количеству получаемых продуктов. Селективность характеризует процессы, в которых протекают сложные параллельные и последовательные реакции с получением нескольких продуктов, что часто встречается на практике. Например, если в процессе протекают параллельные реакции
 R
R
 A
A
S
и целевым является продукт R, то селективность будет выражаться в виде
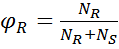 , (2.14)
, (2.14)
где ϕR– селективность; NR, NS– количество продукта R и S.
Между выходом, степенью превращения и селективностью существуют определенные зависимости. Для простой необратимой реакции (А → R): Ф = Х; простой обратимой реакции (A ↔ R): Ф = Х / Х*; для сложной реакции: Ф = X ∙φ.
В производственных условиях с целью уменьшения расходных коэффициентов сырья стремятся иметь возможно более высокие значения X, φ, Ф.
Вопросы для самоконтроля
1. Дайте определения понятиям: химическое производство, химико-технологический процесс, химико-технологическая система и объясните их
2. В чём заключается метод системного анализа для исследования химико-технологического процесса?
3. Что может служить производственным эквивалентом химико-технологической системы?
4. Из каких частей состоит химико-технологическая система?
5. Какие подсистемы можно выделить в химико-технологической системе?
6. Какие элементы ХТС Вы можете указать? Их назначение и примеры в производстве.
7. Что такое связь в химико-технологической системе? Какие типы сязей и их назначения Вы знаете?
8. Как отображается ХТС система (виды её модели)?
9. Приведите пример химической, операционной и функциональной схем какого-либо производства?
10. Чем отличаются технологическая и структурная схемы химического производства? Покажите это на примере производства аммиака.
11. Перечислите основные технологические показатели эффективности химико-технологического процесса.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 3966; Нарушение авторских прав?; Мы поможем в написании вашей работы!