
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уровень а
|
|
|
|
1. Написать выражение ПР и привести их табличное значение для следующих соединений PbCl2 и Ag2S.
Ответ: PbCl2(к) <=> Pb  + 2Cl
+ 2Cl  ;
;
ПР 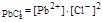 = 2 ∙ 10-5;
= 2 ∙ 10-5;
Ag2S(к) <=> 2Ag  +S
+S  ;
;
ПР  = 5,7 ∙ 10-51,
= 5,7 ∙ 10-51,
т.е. растворимость Ag2S значительно меньше растворимости PbCl2.
2. Написать уравнения диссоциации, выражения констант диссоциации и привести их табличное значение для H2S.
Ответ: поскольку H2S – слабый электролит, то процесс диссоциации является обратимым и протекает ступенчато:
| 1-я ступень: H2S <=> H+ + HS-; | |
 =6,0·10-8. =6,0·10-8.
| |
| 2-я ступень: HS- <=> Н+ + S2-; | |
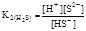 =1,0·10-14. =1,0·10-14.
|
Поскольку 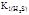 больше
больше 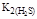 в 6∙106 раз, то можно считать, что диссоциация H2S протекает в основном по первой ступени.
в 6∙106 раз, то можно считать, что диссоциация H2S протекает в основном по первой ступени.
3. Определить силу электролитов и написать уравнения диссоциации сильных электролитов:
Zn(OH)2; HCl; H3PO4; NaOH; HCN.
Ответ: поскольку к сильным относятся кислоты HCl, HBr, HJ, HNO3, H2SO4, HClO4, а к сильным основаниям относятся LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2, то
Zn(OH)2 – слабый электролит; HCl – сильный электролит; H3PO4 – слабый электролит; NaOH – сильный электролит, HCN – слабый электролит.
Диссоциация сильных электролитов на ионы протекает нацело:
HCl = H+ + Cl-;
NaOH = Na+ + OH-.
8. ГИДРОЛИЗ СОЛЕЙ
|
|
|
|
|
Дата добавления: 2015-03-29; Просмотров: 366; Нарушение авторских прав?; Мы поможем в написании вашей работы!