
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Законы электролиза
|
|
|
|
Масса электролита, подверженная химическому превращению, а также массы веществ, выделившихся на электродах по законам Фарадея прямо пропорциональны количеству прошедшего через электролит электричества и молярным массам эквивалентов веществ:
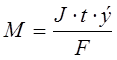 , где
, где
m -масса электролита, подвергшаяся электролизу или масса веществ, выделившаяся на электродах, г;
J -сила тока, А;
э-молярная масса эквивалентов вещества, г/моль;
F-число Фарадея – 96500 Кл;
t-время электролиза, с;
КОНТРОЛЬНЫЕ ЗАДАНИЯ
68. Составьте уравнения процессов, протекающих при электролизе расплавов NaOH и NiCl2 с инертными электродами.
69. Составьте схемы электролиза водных растворов серной кислоты, хлорида меди, нитрата свинца с платиновыми электродами.
70. Напишите уравнения электродных процессов, протекающих при электролизе водных растворов хлорида бария и хлорида железа (II) с угольными электродами.
71. Составьте схемы электролиза водного раствора хлорида цинка, если а) анод цинковый; б) анод угольный.
72. Какой объем водорода выделится при пропускании тока силой в 3 А в течение 1 часа через водный раствор серной кислоты.
73. При электролизе водного раствора SnCl2 на аноде выделилось 4,48 л. хлора (условия нормальные). Какое вещество и в каком количестве выделилось на катоде.
74. В какой последовательности будут выделяться металлы при электролизе раствора, содержащего в одинаковой концентрации сульфаты никеля, серебра, меди. Напишите уравнения процессов на электродах.
75. Составьте схему процессов, происходящих на медных электродах при электролизе водного раствора нитрата калия.
76. Неочищенная медь содержит примеси серебра и цинка. Что происходит с этими примесями при электролитическом рафинировании меди. Напишите уравнения процессов на электродах.
77. Сколько времени потребуется для полного разложения 2 молей воды током силой 2А.
78. Через растворы поваренной соли и фосфата натрия пропустили в течение некоторого времени постоянный ток. Изменится ли от этого количество соли в том и в другом случае. Ответ мотивируйте, составив электронные уравнения процессов идущих на катоде и аноде.
79. При электролизе раствора сульфата меди (II) на аноде выделилось 0,168 л газа (нормальные условия) составьте электронные уравнения процессов и вычислите, какая масса меди выделится на катоде.
80. Составьте электронные уравнения процессов происходящих при электролизе раствора и расплава КОН.
81. Какие вещества и в каком количестве выделятся на угольных электродах при электролизе раствора NaI в течении 2,5 часов если сила тока равна 6 А.
82. Сколько граммов серной кислоты образуется возле анода при электролизе раствора сульфата натрия, если на аноде выделится 1,12л кислорода (н.у.) вычислить массу вещества, выделившегося на катоде.
83. При электролизе раствора нитрата серебра на аноде выделилось 0,28 л кислорода. Сколько граммов серебра выделилось на катоде.
84. В воде растворены соли алюминия, цинка и меди с концентрацией катионов 1 моль/л. составьте электронные уравнения процессов на электродах и укажите последовательность реакций на катоде.
85. Какие продукты могут быть получены при электролизе раствора NaNO3, если анодное и катодное пространства:
а) разделены пористой перегородкой;
б) не разделены и раствор перемешивается.
86. Какие продукты будут выделяться на катоде и аноде в первую очередь при электролизе водных растворов с графитовыми электродами, если в электролите находится смесь сульфата меди (II) и хлорида калия.
87. В водный раствор нитрата серебра опущены медная и серебряная пластинки. К какому полюсу источника тока должна быть присоединена медная пластинка для покрытия ее серебром. Напишите схему процесса электролиза.
|
|
|
|
|
Дата добавления: 2015-03-29; Просмотров: 1089; Нарушение авторских прав?; Мы поможем в написании вашей работы!