
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Билет № 17. Опыт. Проведение реакций, подтверждающих свойства гидроксида кальция
|
|
|
|
Опыт. Проведение реакций, подтверждающих свойства гидроксида кальция.
1.
Гидроксид кальция (гашеная известь) – малорастворимое вещество. Взбалтываем немного извести в 2 мл воды (около 2 см по высоте пробирки), даем постоять несколько минут. Большая часть извести не растворится, осядет на дно.
2.
Сливаем раствор, фильтруем (если нет фильтра, ждем пока отстоится). Прозрачный раствор гидроксида кальция называется известковой водой. Делим на 2 пробирки. В одну капаем индикатор фенолфталеин (ф-ф), он окрашивается в малиновый цвет, что доказывает оснóвные свойства извести:
Ca(OH)2 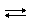 Ca2+ + 2OH-
Ca2+ + 2OH-
3.
Во вторую пробирку пропускаем углекислый газ, известковая вода мутнеет в результате образования нерастворимого карбоната кальция (это качественная реакция для обнаружения углекислого газа):
Ca(OH)2 + CO2 = CaCO3↓ + H2O
Если придется делать эти реакции на практике, углекислый газ можно получить в пробирке с газоотводной трубкой, добавив соляную или азотную кислоту в мел или соду.
Можно несколько раз пропустить выдыхаемый воздух через трубочку от коктейля или сока, принесенную с собой. Не стоит шокировать комиссию – дуть в трубку из лабораторного оборудования – в кабинете химии ничего нельзя пробовать на вкус!
^
1. Оксиды: их классификация и химические свойства (взаимодействие с водой, кислотами и щелочами).
Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород.
Оксиды делят на кислотные, оснóвные, амфотерные и несолеобразующие (безразличные).
^ Кислотным оксидам соответствуют кислоты. Кислотными свойствами обладают большинство оксидов неметаллов и оксиды металлов в высшей степени окисления, например CrO3.
Многие кислотные оксиды реагируют с водой с образованием кислот. Например, оксид серы (IV), или сернúстый газ, реагирует с водой с образованием сернúстой кислоты:
SO2 + H2O = H2SO3
Кислотные оксиды реагируют со щелочами с образованием соли и воды. Например, оксид углерода (IV), или углекислый газ, реагирует с гидроксидом натрия с образованием карбоната натрия (соды):
CO2 + 2NaOH = Na2CO3 + H2O
Оснóвным оксидам соответствуют основания. К оснóвным относятся оксиды щелочных металлов (главная подгруппа I группы),
магния и щелочноземельных (главная подгруппа II группы, начиная с кальция), оксиды металлов побочных подгрупп в низшей степени окисления (+1+2).
Оксиды щелочных и щелочноземельных металлов реагируют с водой с образованием оснований. Так, оксид кальция реагирует с водой, получается гидроксид кальция:
CaO + H2O = Ca(OH)2
Основные оксиды реагируют с кислотами с образованием соли и воды. Оксид кальция реагирует с соляной кислотой, получается хлорид кальция:
CaO + 2HCl = CaCl2 + H2O
Амфотерные оксиды реагируют и с кислотами, и со щелочами. Так, оксид цинка реагирует с соляной кислотой, получается хлорид цинка:
ZnO + 2HCl = ZnCl2 + H2O
Оксид цинка взаимодействует и с гидроксидом натрия с образованием цинката натрия:
ZnO + 2NaOH = Na2ZnO2 + H2O
С водой амфотерные оксиды не взаимодействуют. Поэтому оксидная пленка цинка и алюминия защищает эти металлы от коррозии.
Несолеобразующим (безразличным) оксидам не соответствуют гидроксиды, они не реагируют с водой. Несолеобразующие оксиды не реагируют ни с кислотами, ни со щелочами. К ним относится оксид азота (II) NO.
Иногда к несолеобразующим относят угарный газ, но это неудачный пример, т.к. этот оксид реагирует с гидроксидом натрия с образованием соли:
CO + NaOH = HCOONa
(эта реакция не для запоминания! Изучается в 10-11 классах)
^
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1229; Нарушение авторских прав?; Мы поможем в написании вашей работы!