
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Анализ диаграммы сплава, образующих неустойчивые химические соединения. Правило фаз
|
|
|
|
Коррозионно-стойкие стали, их маркировка и примеры применения.
Структура и свойства термопластов конструкционного назначения.
Термопласты — полимерные материалы, способные обратимо переходить при нагревании в высокоэластичное либо вязкотекучее состояние. При обычной температуре термопласты находятся в твёрдом состоянии. При повышении температуры они переходят в высокоэластичное и далее — в вязкотекучее состояние, что обеспечивает возможность формования их различными методами. Эти переходы обратимы и могут повторяться многократно, что позволяет, в частности, производить переработку бытовых и производственных отходов из термопластов в новые изделия.
Переработка термопластов в изделия не сопровождается необратимой химической реакцией. Пригодны к повторной обработке (формованию). Полимеры-термопласты могут иметь линейное или разветвлённое строение, быть аморфными (полистирол, полиметилметакрилат) либо кристаллическими (полиэтилен, полипропилен). В отличие от реактопластов для термопластов характерно отсутствие трёхмерной сшитой структуры и переход в текучее состояние, что делает возможным термоформовку, литьё и экструзию изделий из них. Некоторые линейные полимеры не являются термопластами, так как температура разложения у них ниже температуры текучести (целлюлоза).
Составы сталей, устойчивых к электрохимической коррозии, устанавливают в зависимости от среды, для которой они предназначаются. Эти стали можно разделить на два основных класса: хромистые, имеющие после охлаждения на воздухе ферритную, мартенситно-ферритную (феррита более 10 %) или мартенситную структуру, и хромоникелевые, имеющие аустенитную, аустенитно-мартенситную или аустенитно-ферритную (феррита более 10%) структуру.
Коррозионная стойкость стали повышается термической обработкой: закалкой и высоким отпуском и созданием шлифованной и полированной поверхности.
Стали 12X13 и 20X13 применяют для изготовления деталей с повышенной пластичностью, подвергающихся ударным нагрузкам (клапанов гидравлических прессов, предметов домашнего обихода), а также изделий, испытывающих действие слабоагрессивных сред (атмосферных осадков, водных растворов солей органических кислот и т. д.).
Стали 30X13 и 40X13 используют для карбюраторных игл, пружин, хирургических инструментов и т. д
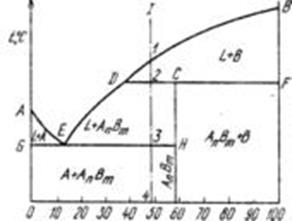 В отличие от диаграммы с устойчивым химическим соединением на рис. 104 приведена диаграмма состояний, где два компонента образуют неустойчивое химическое соединение, которое при нагреве до определенной температуры (t1)разлагается на жидкость и один из компонентов, т. е. не расплавляется полностью.
В отличие от диаграммы с устойчивым химическим соединением на рис. 104 приведена диаграмма состояний, где два компонента образуют неустойчивое химическое соединение, которое при нагреве до определенной температуры (t1)разлагается на жидкость и один из компонентов, т. е. не расплавляется полностью.
На линии DCF находятся в равновесии три фазы: жидкость концентрации D, кристаллы компонента В и кристаллы химического соединения АпВm.
При нагреве неустойчивое химическое соединение АпВm распадается на жидкость концентрации Dи кристаллы В.При охлаждении, следовательно, произойдет обратная реакция:
LD + B→AnBm.
Реакция эта подобна перитектической; жидкость реагирует с ранее выпавшими кристаллами, но образует не новый твердый раствор, как в случае перитектической реакции, а химическое соединение.
Процесс кристаллизации сплава I в равновесных условиях будет протекать следующим образом. В точке 1 начинается кристаллизация, выпадают кристаллы В, и концентрация жидкости изменяется по кривой 1— D.В точке 2 при постоянной температуре образуется неустойчивое химическое соединение по уравнению, приведенному выше. По окончании реакции в избытке остается жидкость, которая кристаллизуется с выделением соединения АпВm до тех пор, пока концентрация жидкости не достигнет точки Е. Тогда оставшаяся жидкость кристаллизуется в эвтектику, состоящую из кристаллов А и химического соединения. Следовательно, на кривой будем иметь две площадки: верхнюю, соответствующую образованию неустойчивого химического соединения, и нижнюю, соответствующую образованию эвтектики А + АпВm.
Правило фаз — соотношение, связывающее число веществ (компонентов), фаз и степеней свободы в гетерогенной системе.
Правило фаз записывается следующим образом:

где j — число фаз (например, агрегатных состояний вещества);
v — число степеней свободы, то есть независимых параметров (температура, давление, концентрация компонентов), которые полностью определяют состояние системы при равновесии и которые можно менять без изменения числа и природы фаз;
k — число компонентов системы — число входящих в систему индивидуальных веществ за вычетом числа химических уравнений, связывающих эти вещества. Иначе говоря, это минимальное количество веществ, из которых можно приготовить каждую фазу системы.
n — число переменных, характеризующих влияние внешних условий на равновесие системы.
При переменных давлении и температуре правило фаз сводится к выражению:
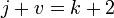
В случае однокомпонентной системы оно упрощается до:
 ,
,
Отсюда видно, например, что в однокомпонентной системе три фазы (j=3) могут сосуществовать при числе степеней свободы v, равном нулю, то есть при фиксированных давлении и температуре, что соответствует тройной точке на фазовой диаграмме. Две фазы (j=2) сосуществуют при произвольном измененнии либо давления, либо температуры, когда вторая из этих переменных не является независимой (v=1), то есть двухфазному равновесию на фазовой диаграмме соответствует линия. Если фаза одна (j=1), число степеней свободы системы равно двум, то есть температура и давление могут менятся независимо в пределах некоторой области на фазовой диаграмме — пока система не окажется на одной из линий двухфазного равновесия.
Иногда правило фаз записывают следующим образом:
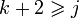
то есть при равновесии число фаз в системе меньше либо равно числу компонентов плюс 2.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 785; Нарушение авторских прав?; Мы поможем в написании вашей работы!