
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Билет 26. Ионное произведение воды. Водородный показатель (рН) среды. Определение рН с помощью индикаторов
|
|
|
|
Так как вода является очень слабым электролитом, то это означает, что
только весьма малая часть ее молекул диссоциирует. Концентрация молекул воды равна: 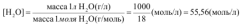 . Эту величину считают постоянной, поэтому:
. Эту величину считают постоянной, поэтому: 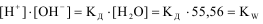 .
. 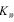 называют ионным произведением воды. Ионное произведение воды сильно зависит от температуры, также не зависит от концентрации ионов.
называют ионным произведением воды. Ионное произведение воды сильно зависит от температуры, также не зависит от концентрации ионов.
Для количественной характеристики среды используют специальную величину – водородный показатель или рН среды. Это есть взятый с обратным знаком десятичный логарифм концентрации ионов водорода в растворе.Если pH = 7 – среда нейтральная, pH< 7 – среда кислая, Hp >7 – cреда щелочная.
Для качественной характеристики среды служат вещества – индикаторы, которые меняют свою окраску в определенной области значений pH раствора. В качестве индикаторов используют слабые органические кислоты и основания, молекулы и ионы которых имеют разную окраску. При введении в раствор они диссоциируют. Выбор того или иного индикатора определяется интервалом pH, в котором необходимо поддерживать кислотность исследуемого раствора – это область перехода индикатора.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1200; Нарушение авторских прав?; Мы поможем в написании вашей работы!