
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Практическое применение электрохимических процессов. Химические источники тока. Аккумуляторы. Свинцовый аккумулятор. Топливные элементы. Водородно-кислородный топливный элемент
|
|
|
|
Особенности кинетики электрохимических процессов. Стадии электрохимической реакции. Поляризация электродов и ее виды (концентрационная, химическая и газовая). Перенапряжение: водородное перенапряжение. Влияние поляризации электродов на ЭДС гальванического элемента и потенциал разложения электролита в электролизе.
Электролиз. Последовательность заряда ионов в расплавах и водных растворах при электролизе. Вторичные процессы при электролизе. Электролиз с растворимыми анодами. Потенциал разложения. Законы Фарадея. Выход по току. Электрохимический эквивалент. Применение электролиза в технике. Расчет толщины металлического покрытия, наносимого методом электролиза.



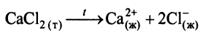

В водных растворах электролитов появляется второе вещество – вода. И при рН<>7, соли могут подвергаться гидролизу. 





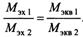
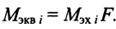

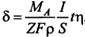




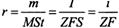










Любая электрохимическая реакция протекает минимум в 3 стадии: 1 - подвод реагентов к электроду; 2 - собственно электрохимическая реакция; 3 - отвод продуктов реакции от электродов
Так как поляризация может наблюдаться как на катоде, так и на аноде, то различают катодную и анодную поляризации Dj К, Dj А. Изменение потенциала при прохождении тока также называется «перенапряжением» Графическую зависимость потенциала от плотности тока называют поляризационной кривой
Изменение потенциала электрода вследствие изменения концентрации реагентов в приэлектродном слое при прохождении тока называется концентрационной поляризацией.
Изменение потенциала, обусловленное замедленностью собственно электрохи-мических стадий реакций, называется электрохимической поляризацией (перенапряжением).
.Изменение потенциала электрода при прохождении тока называется поляризацией:
 |
где Dj - поляризация, Dj i -потенциал электрода при прохождении тока, Dj Р - равновесный потенциал.
Изменение потенциала при прохождении тока также называется «перенапряжением». Этот термин обычно употребляют, когда известна причина изменения потенциала. Его также относят к некоторым процессам, например к катодному выделению (водородное перенапряжение).





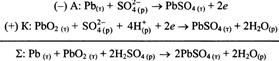
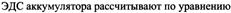


Коррозия. Классификация коррозийных процессов. Скорость равномерной коррозии.
Коррозия - самопроизвольное разрушение материалов вследствие их физико-хим. взаимодействия с окружающей средой. Если разрушение произошло из-за мех. причины - эрозия. Процесс коррозии железа - ржавление











|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1252; Нарушение авторских прав?; Мы поможем в написании вашей работы!