
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ингибиторная защита
|
|
|
|
Снижение агрессивности коррозионной среды
Значительное изменение состава коррозионной среды может быть достигнуто одним из перечисленных способов:
а) удалением кислорода при помощи деаэрации раствора, насыщения его азотом или добавления в него поглотителей кислорода;
б) удалением кислот путем нейтрализации раствора гашеной известью или едким натром;
в) удалением солей из воды, идущей на питание паровых котлов, путем обработки ее ионообменными смолами;
г) вакуумированием.
В случае металлов, пассивирующихся в данной среде, присутствие в ней кислорода или других окислителей способствует процессу пассивации и ведет к торможению коррозии. Во всех остальных случаях окислители стимулируют коррозию металлов. Железо в аэрированных водных растворах корродирует с кислородной деполяризацией:
4Fe + 6Н2О + ЗО2 = 4Fe(OH)3.
Для снижения концентрации растворенного кислорода добавляют гидразин или сульфит натрия. Между гидразином и растворенным кислородом идет реакция
N2H4 + О2 = N2 + 2Н2О
Избыток гидразина разлагается на аммиак и азот
3N2H4 = N2 + 4NH3
Присутствие в воде аммиака ведет к увеличению щелочности и поэтому имеет положительный эффект.
Применение сульфита натрия менее эффективно, чем гидразина, т.к. увеличивает содержание солей в воде:
Na2SO3 + 1/2O2 = Na2SO4
.
Обработка водных растворов гашеной известью широко применяется в промышленности. Таким образом регулируют рН растворов, а также снижают содержание в них солей. При подщелачивании растворов образуются гидроксиды металлов, которые имеют более низкую растворимость, чем соответствующие соли. Часть гидроксидов выпадает в осадок, и содержание ионов металлов в растворе снижается.
Для глубокой очистки воды с целью предотвращения образования накипи в паровых котлах проводят ионообменную обработку. Как правило, применяют серию ионообменных аппаратов. Первоначально используют катионообменные смолы и воду очищают от катионов металла. На последующих стадиях проводят анионообменную очистку и освобождаются от анионов сильных и слабых кислот.
Ингибиторами коррозии (ИК) называют химические соединения, которые, присутствуя в коррозионной системе в достаточной концентрации, уменьшают скорость коррозии без значительного изменения концентрации любого коррозионного реагента. Ингибиторами коррозии могут быть и композиции химических соединений. Содержание ингибиторов в коррозионной среде должно быть небольшим.
Защиту ингибиторами применяют в системах с постоянным или мало обновляемым объемом коррозионной среды, например, в резервуарах, цистернах, паровых котлах, системах охлаждения, некоторых химических аппаратах, травильных ваннах для снятия окалины, а также при хранении и транспортировке металлических изделий.
Эффективность ингибиторов оценивается степенью защиты Z, %, и коэффициентом торможения γ (ингибиторный эффект) и определяется по формулам
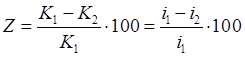 ,
,
где К1 и К2 [г/(м2·ч)] — скорость растворения металла в среде без ингибитора и с ингибитором соответственно; i1 и i2 [А/см] — плотность тока коррозии металла в среде без ингибитора и с ингибитором соответственно. При полной защите коэффициент Z равен 100%. Коэффициент торможения показывает, во сколько раз уменьшается скорость коррозии в результате действия ингибитора
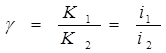 ;
;
Z и γ увязаны между собой:
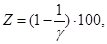
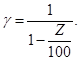
Ингибиторы подразделяются:
а) по механизму своего действия — на катодные, анодные и смешанные;
б) по химической природе — на неорганические, органические и летучие;
в) по сфере своего влияния — в кислой, щелочной и нейтральной среде.
Действие ингибиторов обусловлено изменением состояния поверхности металла вследствие адсорбции ингибитора или образования с катионами металла труднорастворимых соединений. Защитные слои, создаваемые ингибиторами, всегда тоньше наносимых покрытий.
Ингибиторы могут действовать двумя путями: уменьшать площадь активной поверхности или изменять энергию активации коррозионного процесса.
В результате адсорбции ингибитора происходит изменение структуры двойного электрического слоя. Экранирование части поверхности (Θ) сплошной пленкой ингибитора исключает ее из коррозионного процесса, который протекает на поверхности, равной (1 — Θ).
Катодные и анодные ингибиторы замедляют соответствующие электродные реакции, смешенные ингибиторы изменяют скорость обеих реакций. Адсорбция и формирование на металле защитных слоев обусловлены зарядом частиц ингибитора и способностью образовывать с поверхностью химические связи.
Катодные ингибиторы замедляют катодные реакции или активное растворение металла. Для предотвращения локальной коррозии более эффективны анионные ингибиторы. Часто для лучшей защиты металлов используют композиции ингибиторов с различными добавками.
Неорганические ингибиторы. Способностью замедлять коррозию металлов в агрессивных средах обладают многие неорганические вещества. Ингибирующее действие этих соединений обуславливается присутствием в них катионов (Са2+, Zn2+, Ni2+, As3+, Bi3+, Sb3+) или анионов (Cr2O42-, Cr2O72-, NO2-, SiO32-, РO43-).
Неорганические катодные ингибиторы уменьшают скорость коррозии вследствие снижения эффективности катодного процесса или сокращения площади катодов.
Снижение эффективности катодного процесса может быть достигнуто: а) при коррозии с кислородной деполяризацией — уменьшением содержания кислорода в жидкой коррозионной среде; б) при коррозии с водородной деполяризацией — повышением перенапряжения реакции выделения водорода.
Уменьшение содержания растворенного в коррозионной среде кислорода тормозит реакцию его восстановления, а следовательно, и скорость коррозии.
Перенапряжение водорода может быть повышено при введении в коррозионную среду солей некоторых тяжелых металлов — As Cl3, Bi2(SO4)3. Происходит контактное осаждение этих металлов, что затрудняет реакцию выделения водорода и тем самым - процесс коррозии, так как он протекает с водородной деполяризацией. На рис. 48 показано влияние небольшой добавки As2O3 (0.045% в пересчете на мышьяк) на скорость коррозии углеродистой стали в серной кислоте.
Сокращение площади катодов достигается добавлением экранирующих катодных ингибиторов, которые образуют на микрокатодах нерастворимые соединения, отлагающиеся в виде изолирующего защитного слоя. Для железа в водной среде такими соединениями могут быть Zn SO4, Zn CI2, а чаще Са(НСО3)2.
Бикарбонат кальция Са(НСО3)2 — самый дешевый катодный экранирующий ингибитор, применяемый для защиты стали в системах водоснабжения. Бикарбонат кальция в подщелоченной среде образует нерастворимые соединения СаСО3, осаждающиеся на поверхности, изолируя ее от электролита. Этим объясняется меньшая коррозия стали в жесткой воде по сравнению с умягченной.
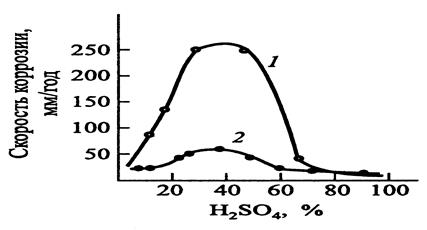
Рисунок - Зависимость скорости коррозии стали в растворах H2SO4:
1 – H2SO4; 2 – H2SO4 + As3+ (0,045%)
Катодные ингибиторы по защитному действию менее эффективны, чем анодные. Однако они совершенно безопасны, так как не вызывают усиления коррозии при их недостаточном содержании.
Анодные неорганические ингибиторы образуют на поверхности металла тонкие (~ 0,01 мкм) пленки, которые тормозят переход металла в раствор. К группе анодных замедлителей коррозии относятся химические соединения — пленкообразователи и окислители, часто называемые пассиваторами.
Катодно-анодные неорганические ингибиторы, например KJ, КВг в растворах кислот, тормозят в равной степени анодный и катодный процессы за счет образования на поверхности металла хемосорбционного слоя.
Пленкообразующие ингибиторы защищают металл, создавая на его поверхности фазовые или адсорбционные пленки. В их число входят некоторые соединения со щелочными свойствами: фосфаты; полифосфаты; силикаты; бораты и др.
Их ингибирующее действие проявляется только при наличии растворенного кислорода, который и играет роль пассиватора. Не являясь окислителями, эти вещества лишь способствуют адсорбции кислорода на поверхности металла. Кроме того, они тормозят анодный процесс растворения из-за образования защитных пленок, представляющих собой труднорастворимые продукты взаимодействия ингибитора с ионами переходящего в раствор металла. Так, например, фосфаты, адсорбируясь на поверхности стали, образуют с ионами железа экранирующие пленки, состоящие из смеси γ·Fe2О3 и FePO4·2H2O. Для большего защитного эффекта фосфаты часто используются в смеси с полифосфатами.
Чаще всего в качестве пассиваторов используют неорганические окислители: хроматы, нитриты, молибдаты, вольфраматы. Легко восстанавливаясь на катодных поверхностях, они ведут себя как деполяризаторы, вызывая появление на анодных участках плотностей тока, превышающих величины, необходимые для их пассивации. При этом стационарный потенциал облагораживается на несколько десятых вольта, а скорость анодного перехода в раствор ионов корродирующего металла резко снижается.
Пассиваторы тормозят анодную реакцию растворения металла благодаря образованию на его поверхности оксидов
Me + nН2О → Ме Оn + 2nН+ + 2nе
Эта реакция может протекать только на металлах, склонных к пассивации.
Анодные ингибиторы коррозии относятся к категории опасных, так как при определенных условиях они из замедлителей коррозии превращаются в ее стимуляторы. Это чаще всего происходит, когда коррозионный процесс протекает с катодным контролем, и по тем или иным причинам не обеспечивается пассивация анодных участков. В данном случае сильные окислители, являющиеся хорошими деполяризаторами, легко восcтанавливаются на катодных участках и увеличивают скорость коррозии. Для того чтобы этого не произошло, плотность коррозионного тока должна быть выше той, при которой достигается полная пассивация анодных участков. Поэтому концентрация ингибитора (пассиватора) не должна быть ниже определенной величины, иначе пассивация может не наступить или будет неполной.
Неполная пассивация также очень опасна, так как приводит к сокращению анодной поверхности, увеличению скорости и глубины разрушения металла на локализованных участках, т.е. появлению точечной коррозии.
Минимальная концентрация Cr O42-, NO22-, Mo O42-, используемых в качестве ингибиторов коррозии стали, приблизительно равна 10-4 —10-3 моль/л. При повышении температуры среды или наличии в ней активаторов, например хлор-ионов, необходимо увеличение концентрации ингибитора.
Анодные замедлители неокислительного типа (фосфаты, силикаты и др.), добавленные в незначительном количестве, также вызывают более глубокую местную коррозию из-за сильного увеличения соотношения катодной площади к анодной.
Таким образом, для обеспечения эффективной защиты необходимо поддерживать концентрацию анодного ингибитора выше предельного значения во всех участках защищаемого изделия (например, в резьбовых соединениях, щелях и других труднодоступных местах).
Анодные ингибиторы очень чувствительны и к рН среды.
Применение анодных ингибиторов разнообразно.
Хроматы и бихроматы натрия и калия используются как ингибиторы коррозии железа, оцинкованной стали, меди, латуни и алюминия в промышленных водных системах. В случае железа действие хроматов описывают реакциями:
2Fe + 2Na2Cr04 + 2Н2О = Сг2 О3 + Fe2O3 + 4Na OH,
6 Fe3 O4 + 2 Na2 Cr04 + 2H2O = Сг2 О3 + 9 Fe2 O3 + 4 Na OH
Оксидная пленка состоит из 25 % Сг2 О3 и 75 % Fe2O3.
Нитриты применяются в качестве ингибиторов коррозии многих металлов (кроме цинка и меди) при рН более 5. Они дешевы и эффективны в случае присутствия ржавчины.
Защитное действие нитритов состоит в образовании поверхностной оксидной пленки по уравнению
2 Fe + Na NO2 + 2H2O = Fe2 O3 + Na OH + NH3
.
Силикаты относятся к ингибиторам смешанного действия, уменьшая скорости как катодной, так и анодной реакций.
Общая формула силикатов — xSi O2·Me2O. Действие силикатов (рис. 49) состоит в нейтрализации растворенного в воде углекислого газа и в образовании защитной пленки на поверхности металла.
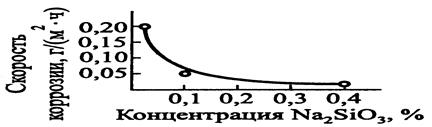
Рисунок - Зависимость скорости коррозии стали в нейтральных водных растворах от концентрации Na2 Si O3
Пленка не имеет постоянного состава. По структуре она напоминает гель кремниевой кислоты, в которой адсорбируются соединения железа и соли жесткости. Ее толщина обычно равна ≈ 0,002 мм.
Полифосфаты — растворимые в воде соединения метафосфатов общей формулы (Ме Р О3)n. Защитное действие полифосфатов состоит в образовании непроницаемой защитной пленки на поверхности металла. В водных растворах происходит медленный гидролиз полифосфатов, в результате образуются ортофосфаты:
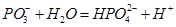 ,
,
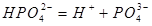 .
.
В присутствии Са2+ и Fe3+ на поверхности образуется непроницаемая защитная пленка:
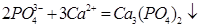 ,
,
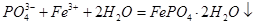
Наибольшее распространение в промышленности получил гексаметафосфат натрия. Фосфаты и полифосфаты находят применение в качестве замедлителей коррозии стали в воде и холодильных рассолах. Большой эффект достигается при совместном использовании фосфатов и хроматов.
|
|
|
|
|
Дата добавления: 2015-05-08; Просмотров: 710; Нарушение авторских прав?; Мы поможем в написании вашей работы!