
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рівняння Арреніуса
|
|
|
|
Взаємодія частинок відбувається при їх зіткненнях, але кількість зіткнень молекул є дуже великою і, якби кожне зіткнення вело б до хімічної взаємодії частинок, всі реакції відбувались би практично миттєво. Арреніус постулював, що зіткнення молекул будуть закінчуватися реакцією лише в тому випадку, коли ці молекули матимуть певний запас енергії – енергію активації.
Енергія активації – це мінімальна енергія, яку необхідно надати молекулам, щоб їх зіткнення вело до хімічної взаємодії.
Хімічна взаємодія частинок пов'язана з розривом старих хімічних зв'язків і утворенням нових, вважають, що будь-яка елементарна реакція проходить через утворення нестабільної проміжної сполуки, яку називають активним комплексом.
Оскільки температура є мірою середньої кінетичної енергії частинок, збільшення температури веде до збільшення кількості частинок, енергія яких дорівнює або більша енергії активації, що веде до збільшення константи швидкості реакції.
Залежність константи швидкості реакції від температури більш точно виражає рівняння Арреніуса:
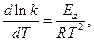
де Еа – енергія активації.
Для виведення рівняння Арреніуса було використано рівняння ізохори хімічної реакції
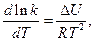
де К – константа рівноваги, ∆U – тепловий ефект реакції при V = const.
Як відомо, константа рівноваги дорівнює:
K = k1/k2,
де k1 та k2 – константи швидкості прямої та зворотної реакцій. Запишемо тепловий ефект як різницю: ∆U = Е1 – Е2, тоді передостаннє рівняння приймає вигляд:
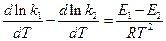
звідси: 
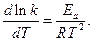
Якщо Еа = const то інтегрування цього рівняння дає інтегральну форму рівняння Арреніуса:
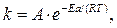

де А – передекспоненційний множник.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 4182; Нарушение авторских прав?; Мы поможем в написании вашей работы!