
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Приклади розв’язування задач. Задача 1. Перетворення пероксиду бензоілу на диетиловий ефір (реакція першого порядку) при 333 К пройшла за 10 хв на 75,2 %
|
|
|
|
Задача 1. Перетворення пероксиду бензоілу на диетиловий ефір (реакція першого порядку) при 333 К пройшла за 10 хв на 75,2 %. Обчисліть константу швидкості реакції.
Розв’язування. Запишемо рівняння константи швидкості першого порядку і підставимо в нього відповідні значення:
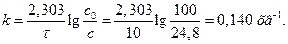
Відповідь: k = 0,140 хв-1.
Задача 2. При збільшенні концентрації речовини А в 1,6 рази швидкість хімічної реакції зростає в 2,56 рази. Який порядок реакції?
Розв’язування. У рівняння швидкості реакції підставляємо дані значення:
υ = k∙Cn ,
2,56 = 1,6n.
З одержаного рівняння визначаємо, що n = 2. Отже, реакція другого порядку.
Задача 3. Визначити час, за який прореагує 90 % мурашиного альдегіду, якщо змішати певну його кількість з еквімолярною кількістю розчину пероксиду водню, якщо константа швидкості цієї реакції k = 0,7544 л/(моль∙год).
Розв’язування. Із розмірності константи швидкості реакції видно, що реакція відноситься до реакції другого порядку і константа швидкості реакції описується рівнянням: 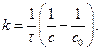
Із даного рівняння виводимо формулу для визначення часу:
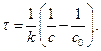
Визначаємо час за який прореагує 90 % мурашиного альдегіду, тобто поточна його концентрація буде: с = 0,1с0:
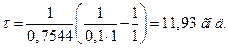
Відповідь: τ = 11,93 год.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 863; Нарушение авторских прав?; Мы поможем в написании вашей работы!