
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Приклади виконання завдань. Окиcно-відновні реакції окисно-відновні реакції -реакції, які відбуваються зі зміною ступенів окиснення елементів
|
|
|
|
ОСНОВНІ ПОНЯТТЯ ТА ВИЗНАЧЕННЯ
ОКИCНО-ВІДНОВНІ РЕАКЦІЇ
| Окисно-відновні реакції | -реакції, які відбуваються зі зміною ступенів окиснення елементів, що входять до складу реагуючих речовин. |
| Ступінь окиснення | - умовний заряд атома в молекулі, розрахований, виходячи з припущення, що молекула складається з іонів. |
| Окиснення | - процес віддачі електронів атомом, молекулою або іоном: 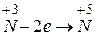 . .
|
| Відновлення | - процес приєднання електронів атомом, молекулою або іоном: 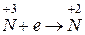
|
| Окисники | - атоми, молекули або іони, що приєднують електрони. До них належать сполуки, що містять атоми в найвищому ступені окиснення, наприклад: 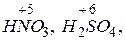 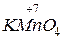 та ін. та ін.
|
| Відновники | - атоми, молекули або іони, що віддають електрони. До них належать сполуки, що містять атоми в найнижчому ступені окиснення, наприклад: 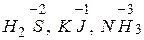 та ін. та ін.
|
Приклад 1. Виходячи зі ступенів окиснення азоту і марганцю в сполуках: 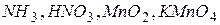 - визначити, які з них можуть бути тільки окисниками, тільки відновниками, а які виявляють як окисні, так і відновні властивості.
- визначити, які з них можуть бути тільки окисниками, тільки відновниками, а які виявляють як окисні, так і відновні властивості.
Відповідь. В окисно-відновних реакціях відновник віддає електрони (окиснюється), а окисник приєднує електрони (відновлюється).
Атом в найвищому ступені окиснення не може віддавати електрони і тому виявляє тільки окисні властивості, а в найнижчому ступені окиснення не може приймати електрони і тому виявляє тільки відновні властивості.
Ступені окиснення азоту у вищенаведених сполуках дорівнюють:
-3 (найнижчий) в сполуці 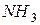 ;
;
+3 (проміжний) в сполуці 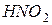 ;
;
+5 (найвищий) в сполуці 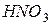 .
.
Ступені окиснення марганцю дорівнюють:
+4 (проміжний) в сполуці 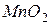 ;
;
+7 (найвищий) в сполуці 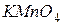 .
.
Тому 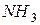 може бути тільки відновником;
може бути тільки відновником; 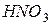 і
і 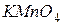 тільки окисниками;
тільки окисниками; 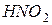 і
і 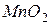 можуть бути як окисниками, так і відновниками, залежно від інших реагентів та умов перебігу реакції.
можуть бути як окисниками, так і відновниками, залежно від інших реагентів та умов перебігу реакції.
Приклад 2. Розставити коефіцієнти в рівнянні окисно-відновної реакції
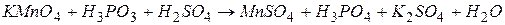
за допомогою методу електронного балансу:
Відповідь. Визначивши ступені окиснення всіх елементів, які входять до складу сполук, знаходимо, що ступені окиснення змінили атоми марганцю (від +7 до +2), та фосфору (від +3 до +5). Для них складаємо електронні схеми та визначаємо коефіцієнти перед окисником і відновником, виходячи з рівності числа відданих та приєднаних електронів:
 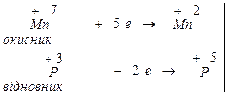
| 2 процес відновлення 5 процес окиснення |
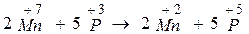
| |
Одержані методом електронного балансу коефіцієнти підставимо до відповідних членів у молекулярне рівняння і поступово знайдемо коефіцієнти для калію, сульфат-іонів і води:
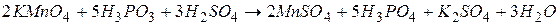
 Приклад 3. Розставити коефіцієнти в рівнянні окисно-відновної реакції
Приклад 3. Розставити коефіцієнти в рівнянні окисно-відновної реакції
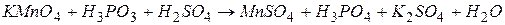
за допомогою методу електронно-іонного балансу:
Відповідь. Визначивши ступені окиснення всіх елементів, складаємо іонно-електронні схеми процесів окиснення та відновлення, зрівнявши число зарядів у лівій та правій частинах. Для цього додаємо (або віднімаємо) необхідну кількість електронів. Щоб прирівняти кількість електронів в обох напівреакціях, першу з них помножуємо на 2, а другу – на 5.
Складаємо скорочене іонне рівняння реакції, підсумовуючи рівняння процесів окиснення та відновлення
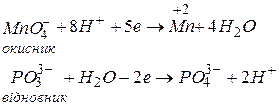
| 2 процес відновлення 5 процес окиснення |

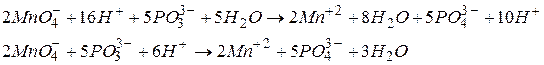
Одержані коефіцієнти переносимо в молекулярне рівняння
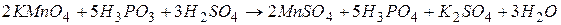 .
.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!