
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
C. А, Е 50 страница
|
|
|
|
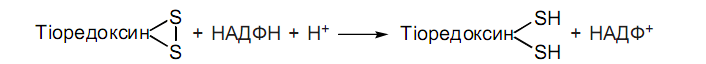
Тіоредоксинредуктаза
Тіоредоксинтрансфераза
Тирозиназа
Тирозинамінотрансфераза
Тіоредоксиндекарбоксилаза
ANSWER: A
Кінцевими продуктами №1 катаболізму урацилу є:

сечова кислота і СО2
β-уреїдпропіонова кислота
β-аланін і сечовина
рибоза і СО2
гіпоксантин і ФАДН2
ANSWER: С
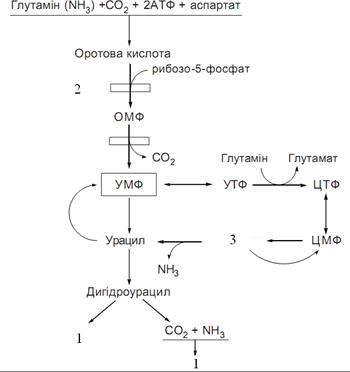
Спадковий дефект ферменту №2 на рис. характеризується наступними ознаками: затримка росту і розумового розвитку дітей у ранньому віці, мегалобластична анемія. Назвіть цей фермент:
Карбамоілфосфатсинтетаза
Аспартаткарбомоїлтрансфераза
Оротатфосфорибозилсинтетаза
Оротатфосфорибозилтрансфераза
Орнітинкарбамоїлтрансфераза
ANSWER: D
Номером 3 на рис. позначено:

Цитозин
Тимін
Аденін
Гуанін
Уридил
ANSWER: А
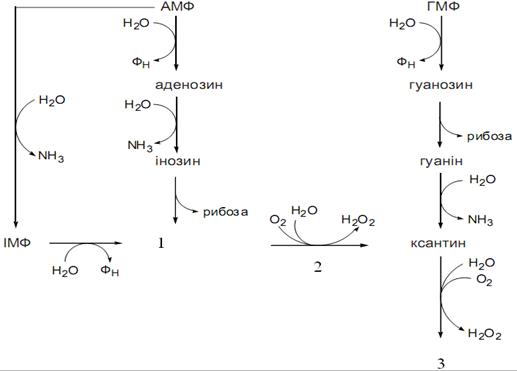
Назвіть проміжний продукт перетворення ІМФ та АМФ, позначений №1 на рисунку:
Аденін
Гуанін
Гуанозин
Гіпоксантин
Інозитол
ANSWER: D
Який фермент №2 на рисунку здійснює перетворення речовини №1 у ксантин?
Ксантинпероксидаза
Аденозиндезаміназа
Ксантиноксидаза
Інозингідратаза
Гіпоксантинамінотрансфераза
ANSWER: С
Назвіть кінцевий продукт №3 на рисунку перетворення АМФ та ГМФ:
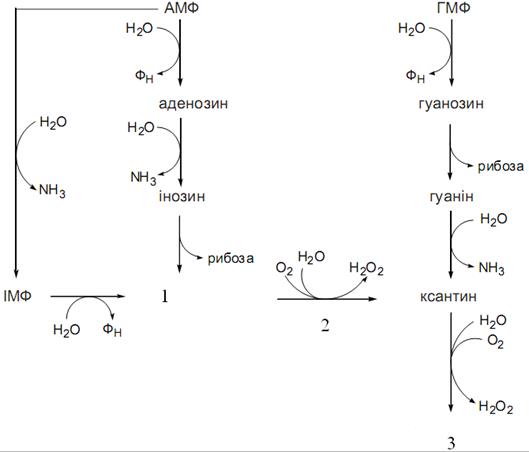
Гіпоксантин
Сечовина
СО2 і NH3
Аміноізобутират
Сечова кислота
ANSWER: Е
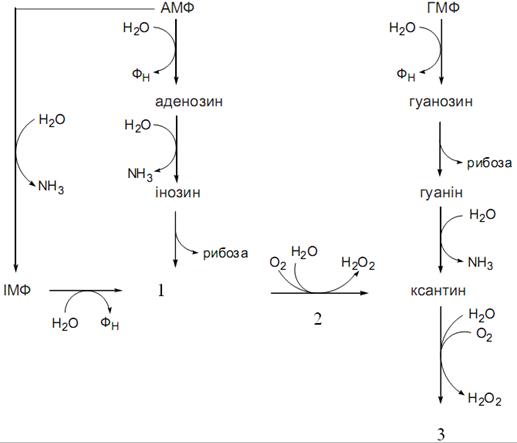
Кінцевим продуктом №1 на рисунку перетворення інозинмонофосфату (ІМФ) є:
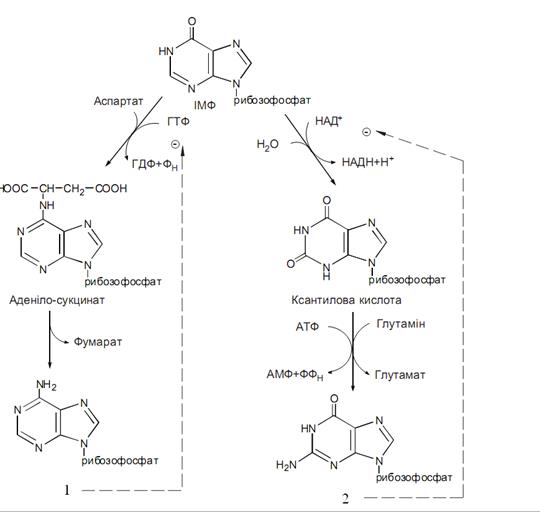
ГМФ
АМФ
ЦМФ
УМФ
ТМФ
ANSWER: В
Вкажіть кінцевий продукт №2 на рисунку перетворення інозинмонофосфату (ІМФ):
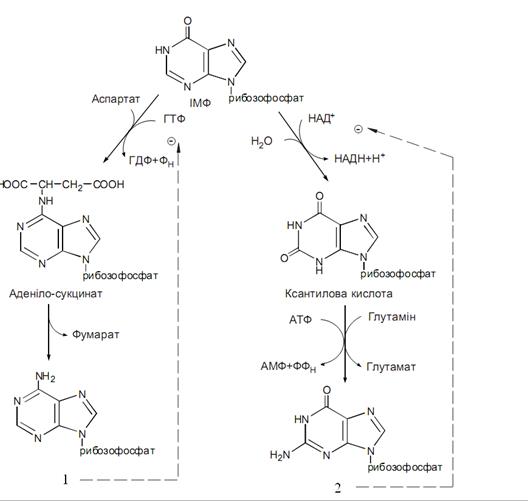
ГМФ
ТМФ
ЦМФ
УМФ
АМФ
ANSWER: А
На рисунку зображена схема синтезу:
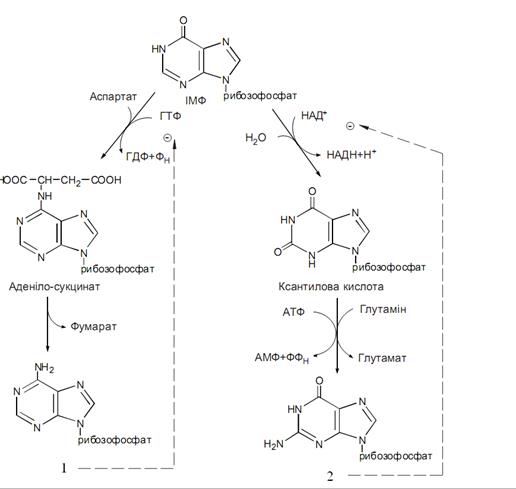
Сечовини
Сечової кислоти
АМФ
ГМФ
Тиміну
ANSWER: В
Назвіть речовину, зображену на рисунку №1:
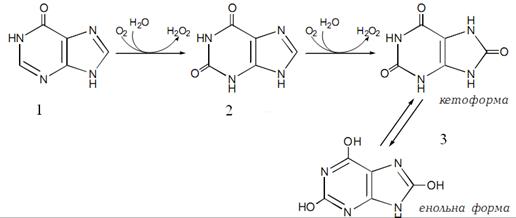
Ксантин
Гуанозин
Гіпоксантин
Інозит
Аденін
ANSWER: С
Назвіть речовину зображену на рисунку №2:

Гіпоксантин
Гуанін
Інозин
Ксантин
Аденін
ANSWER: D
Назвіть кінцевий продукт №3 зображеного на рисунку перетворення:

Гіпоксантин
Сечовина
Сечова кислота
Інозит
Гуанін
ANSWER: С
Першим продуктом №2 на рисунку синтезу піримідинових нуклеотидів є:
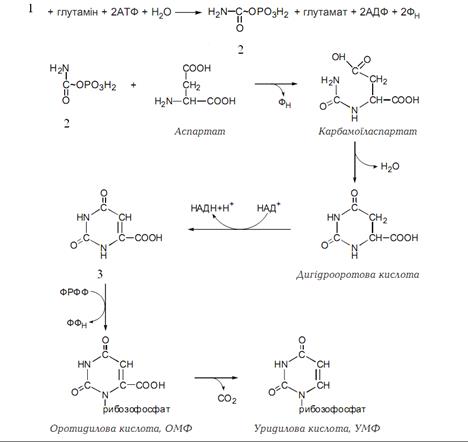
Карбамідфосфат
Карбамоїлфосфат
Карбамоїласпартат
Карбоангідрид
Карбоксипептид
ANSWER: В
Для синтезу піримідинових основ необхідний один із вихідних продуктів, зазначений №1 на рисунку:

Сечовина
СО2
О2
Аспартат
Гліцин
ANSWER: В
Біохімічним показником, який характеризує спадкове порушення синтезу уридилової кислоти(УМФ), є проміжний продукт №3 на рисунку:

Гомогентизинова кислота
Карбамоїлфосфат
Цитозин
Дигідрооротова кислота
Оротова кислота
ANSWER: Е
Спадкове порушення синтезу піримідинів (УМФ), зображеного на рисунку,відоме як:

Аспартатацидурія
Алкаптонурія
Урацилурія
Оротацидурія
Цитозинурія
ANSWER: D
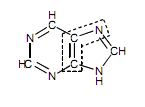
Пуринове ядро містить 4 атоми азоту. Вказати походження 1 атома азоту на даному рисунку:
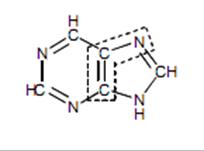
Глутамін
Гліцин
Аспартат
Триптофан
Метіонін
ANSWER: C
Вказати походження 7 атома азоту в пуриновому ядрі нуклеотиду:
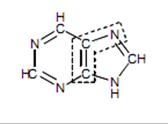
Глутамін
Гліцин
Аспартат
Триптофан
Метіонін
ANSWER: B
Відомо, що пуринове ядро містить 4 атоми азоту. Вкажіть походження 3 атома азоту на даному рисунку:

Глутамін
Гліцин
Аспартат
Триптофан
Метіонін
ANSWER: A
Вкажіть походження 9 атома азоту в пуриновому ядрі:

Глутамін
Гліцин
Аспартат
Триптофан
Метіонін
ANSWER: A
Пуринове ядро містить 5 атомів вуглецю. Вкажіть походження 4 атома вуглецю на даному рисунку:
СО2
Гліцин
Аспартат
НСО3-
-СООН
ANSWER: B
Вкажіть походження 5 атома вуглецю в гетероциклічному ядрі пурину:

СО2
Гліцин
Аспартат
НСО3-
-СООН
ANSWER: B
Вкажіть походження 6 атома вуглецю в гетероциклічному ядрі пурину:

СО2
СО
–СН3
НСО3-
-СООН
ANSWER: A
Вказати походження 2 атома вуглецю пурину:

СО2
Формілтетрагідрофолієва кислота
Пантотенова кислота
НСО3-
Метенілтетрагідрофолієва кислота
ANSWER: B
Вказати походження 8 атома вуглецю пурину:

СО2
Формілтетрагідрофолієва кислота
Пантотенова кислота
НСО3-
Метенілтетрагідрофолієва кислота
ANSWER: E
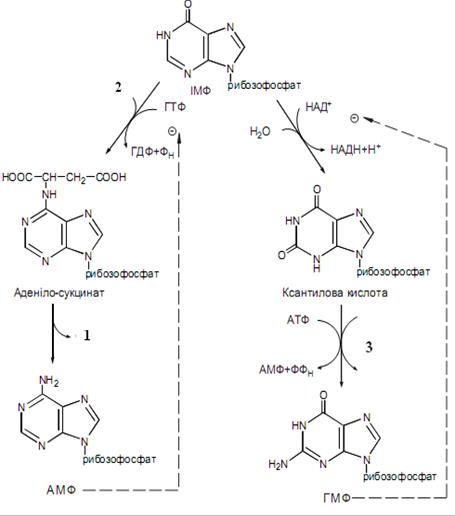
Назвіть сполуку №1 на схемі синтезу пуринових нуклеотидів, яка утворюється в процесі розщеплення аденілосукцинату:
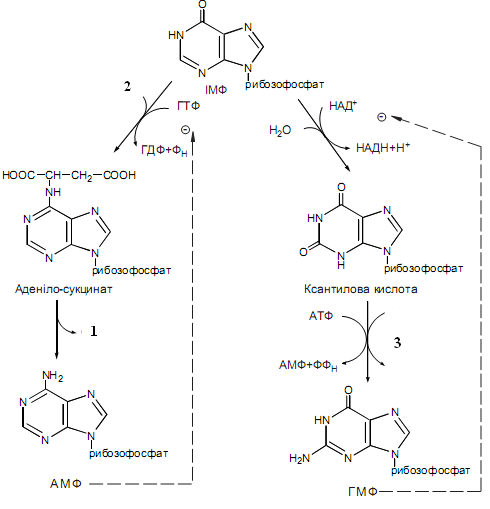
Сукцинат
Піруват
Лактат
Фумарат
Глутамат
ANSWER: D
Яка сполука №2 є донором аміногрупи на шляху синтезу аденозинмонофосфату?
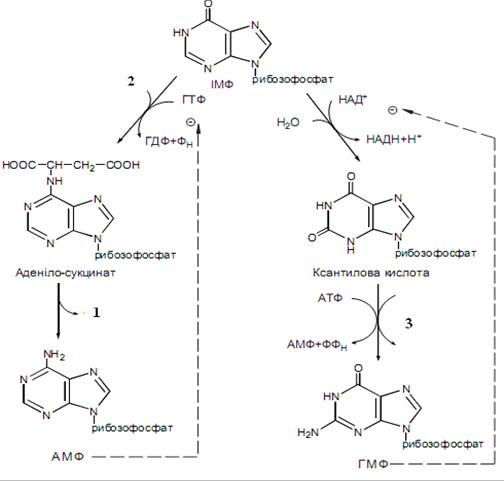
Глутамін
Аспарагінова кислота
Аргінін
Гліцин
Фенілаланін
ANSWER: B
Друга стадія на шляху синтезу гуанозинмонофосфату супроводжується заміщенням кисню на аміногрупу. Вкажіть сполуку №3, яка виступає донором амідної групи:
Аланін
Аспартат
Глутамін
Лейцин
Лізин
ANSWER: C
Перша стадія синтезу гуанозинмонофосфату супроводжується окисненням вуглецю в кільці пурину з утворенням ксантинмонофосфату. Назвіть сполуку №4, яка є акцептором водню в даному випадку:
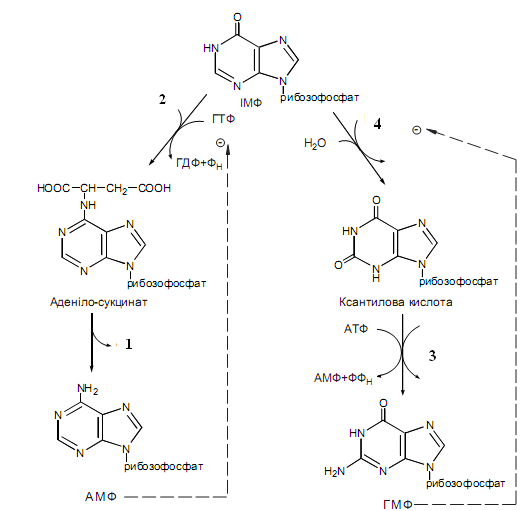
ФАД
ПАЛФ
НАД+
ТГФК
Ацетил-КоА
ANSWER: C
Назвіть сполуку №1 на рисунку, яка гальмує реакцію синтезу аденілосукцинату з інозинмонофосфату:
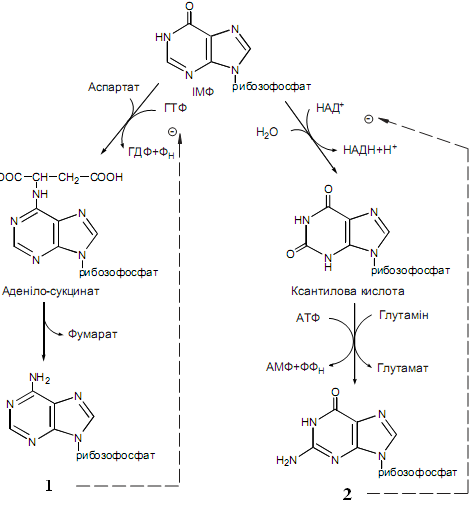
АТФ
ГМФ
ГТФ
ГДФ
АМФ
ANSWER: E
Яка сполука №2 на рисунку гальмує реакцію синтезу із інозинмонофосфату ксантилової кислоти?
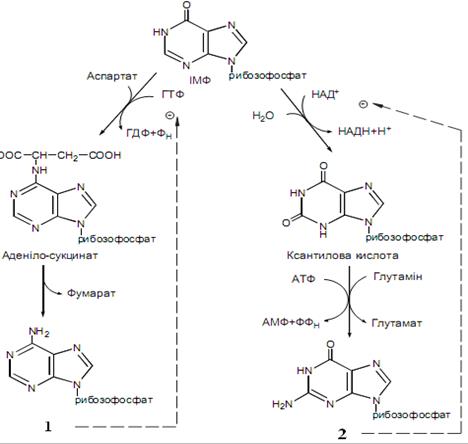
АМФ
АТФ
УМФ
ІМФ
ГМФ
ANSWER: E
Назвіть фермент, який каталізує зображене на рисунку перетворення:
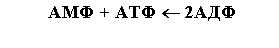
Аденілосукцинатсинтетаза
Амінотрансфераза
Аденілаткіназа
Аденілатциклаза
Аконітаза
ANSWER: C
Біоенергетика як розділ науки про енергетичні перетворення в організмі вивчає:
джерела енергії
способи запасання енергії
механізми енергоперетворення
шляхи використання енергії
*всі відповіді правильні
Біологічне окиснення органічних речовин до СО2 і Н2О з виділенням енергії - це згоряння цих же речовин, що може відбутися поза організмом. В чому відмінність між згорянням поза організмом і біологічним окисненням?
В організмі процес згоряння (окиснення) відбувається без значного підвищення температури тіла.
Здійснюється за участю ферментів.
Відбувається без виділення диму і полум’я.
Не розсіюється в довкілля через воду, наявну в тканинах.
*Все назване характерне для біологічного окиснення.
Енергія, що звільняється в процесі біологічного окиснення (тканинного дихання), тобто енергія розірваних хімічних зв’язків, використовується головним чином:
спершу перетворюється на теплову енергію, яка далі передається на механічну;
*запасається у вигляді макроергічних зв’язків;
вивітрюється у вигляді електромагнітного випромінювання;
акумулюється в клітинах;
нагромаджується у вигляді тепла.
Біологічне окиснення каталізується ферментами і може здійснюватись такими шляхами, крім:
приєднання кисню до субстрату;
відщеплення водню від субстрату;
відщеплення електронів;
приєднання вільних радикалів кисню;
*відщеплення води від субстрату.
Енергія гідролізу макроергічної сполуки АТФ використовується на всі потреби клітини, крім:
реакції біосинтезу білків, ліпідів, вуглеводів, нуклеїнових кислот;
механічної роботи – скорочення скелетних і гладеньких м’язів, міокарду, руху хромосом при мітозі;
активного транспорту речовин (осмотична робота) через мембрани;
генерація біопотенціалів;
* розщеплення НОН на іони.
Зміна вільної енергії біохімічних реакцій може збільшуватись або зменшуватись, тобто перебігати за енд- або екзергонічним характером. Який зв’язок між цими перетвореннями притаманний біосистемам?
Екзергонічні процеси не пов’язані з ендергонічними.
*В час екзергонічних процесів звільняється енергія, що використовується ендергонічних перетворень.
Ендергонічні служать основою для перебігу екзергонічних процесів.
Екз- і ендергонічні процеси перебігають в різний час.
Екзергонічні процеси призводять до виділення теплової енергії.
АТФ, як і інші нуклеозидтрифосфати, належить до макроергічних сполук, при гідролізі яких звільняється багато енергії макроергічних зв’язків. Енергії макроергічного зв’язку відповідають такі величини:
10 кДж/моль;
15 кДж/моль;
7 кДж/моль;
19 кДж/моль;
*21-30 кДж/моль.
До макроергічних сполук відносяться всі, крім:
АТФ, ЦТФ, ГТФ, ТТФ;
фосфоенолпіруват, 1,3-дифосфогліцерат;
креатинфосфат;
ацетил КоА, сукциніл КоА;
*глюкозо-6-фосфат.
В організмі людини міститься всього 50 г АТФ, а утилізується близько 60 кг АТФ. Виберіть обгрунтоване пояснення цього стану:
Утворений АТФ швидко розкладається на АМФ і Фн.
*Значеа кількість АТФ (60 кг) характеризує не загальну її масу, а швидкість перетворення АТФ до АДФ із виділенням теплоти.
Частина утвореного АТФ вилучається з організму нирками.
Надлишок утвореної АТФ просто руйнується до нуклеозиду і трифосфату.
Кількість утвореної АТФ важко підраховується.
З нижченаведених варіантів вибрати головні шляхи утворення АТФ із АДФ і Фн :
*субстратне і окиснювальне фосфорилювання АДФ;
аденілаткіназна реакція;
креатинфосфокіназне перетворення АДФ;
перетворення глюкозо-1-фосфату;
перетворення-6-фосфату.
Під тканинним диханням розуміють процес окиснювального розщеплення органічних речовин їжі. Воно відбувається в 3 стадії: 1а-шлунково-кишкова, 2а відбувається в цитоплазмі клітин, 3я-в мітохондріях. У якій із них виділяється найбільше енергії у вигляді АТФ?
У першій стадії.
У другій стадії.
У першій і другій разом.
*У третій стадії.
У всіх стадіях однаково.
В процесі катаболізму харчових продктів можна виділити два типи шляхів – специфічний і загальний. Які речовини утворюються на специфічному шляху?
*Специфічним шляхом із білків, ліпідів та вуглеводів утворюється ацетил КоА і піруват.
Жирні кислоти і холестерин.
Нікотинамід.
Лимонна кислота.
Сукциніл КоА.
Загальний шлях катаболізму – це окиснювальне декарбоксилювання ПВК та цикл Кребса. Основним їх призначення є:
*забезпечувати дихальний ланцюг субстратами окиснення (донорами водню);
вилучати енергію АТФ;
завершувати окиснення молочної та піровиноградної кислот;
використовувати як коферменти вітаміни В1, В2, В3 і В5;
активувати цитохромоксидазу.
Основні функції цитратного циклу – всі, крім:
об’єднує катаболізм білків, ліпідів та вуглеводів;
виконує як катаболітичну, так і анаболітичну функцію (деякі субстрати циклу йдуть на синтетичні процеси);
енергетична функція – утворюється 1 молекула АТФ;
основний генератор водню для дихального ланцюга;
*служить джерелом теплової енергії.
Термінальною стадією тканинного дихання є дихальний ланцюг. Тут відбувається доокиснення судстратів, а виділена енергія використовується на утворення АТФ. Яким способом відбувається тут окиснененя?
Приєднанням атомів кисню до субстратів.
Приєднанням цілої молекули кисню.
Відщепленням протонів.
*Відщепленням атомів водню і перенесенням протонів і електронів на молекулярний кисень.
Приєднання кисню до субстрату.
Ферменти, що каталізують окиснення субстратів шляхом дегідруавння називають дегідрогеназами. Розрізняють нікотинамідні і флавінові дегідрогенази. Перші характеризуються такими особливостями за винятком:
коферментом у них є НАД+ або НАДФ+;
нікотинаміддинуклеотиди знаходяться в дисоційованій формі;
зв’язуються з апоферментом тільки в ході реакції;
більшість НАД-залежних дегідрогеназ локалізовані в матриксі мітохондрій;
*утворені під час окиснення субстратів НАДН переносяться безросередньо на цитохром С.
НАДФ-залежним дегідрогеназам притаманні такі властивості, крім:
перебувають у дисоційованому стані;
під час реакцій зв’язуються з апоферментом;
локалізуються переважно в цитоплазмі;
утворений НАДФН не віддає е- до дихального ланцюга, а використовується як відновник;
*утворений НАДФН передається убіхінону.
Флавінові дегідрогенази постачають до дихального ланцюга відновлені коферменти ФМН або ФАД. Для цих коферментів характерним є все, за винятком:
вони міцно зв’язані з апоферментом;
в процесі дегідрування субстратів вони перетворюються на відновлені форми (ФМН)Н2 чи ФАДН2;
флавінові коферменти приєднують по два протони і два електрони;
ФМН і ФАД є простетичною групою НАДН-дегідрогенази;
*ФМН і ФАД можуть знаходитись у дисоційованому стані.
Убіхінон – низькомолекулярна органічна ліпофільна речовина, що вільно переміщається у внутрішній мембрані мітохондрій. У дихальному ланцюзі він бере участь у таких процесах:
приймає електрони і протони від НАДН;
приймає електрони і протони від ФАДН2;
*віддає електрони і протони на цитохром „в”;
переносить електрони на цитохром „в”;
служить акцептором атомів водню і донором „е” для цитохрому „в” та протонів для середовища.
Цитохроми – гемвмісні білки внутрішньої мембрани мітохондрій, що переносять електрони по дихальному ланцюгу від убіхінону послідовно через атоми заліза цитохромів в, с1, с, а1 і а3 на кисень. В основі передачі електронів через цитохромну систему лежить:
*зростання окисно-відновного потенціалу кожного наступного переносника в порівнянні з попереднім;
близьке сусідство – контакт між окремими цитохромами;
зростання спорідненості окремих цитохромів – переносників до кисню;
локальне зменшення в’язкості мембрани між сусідніми цитохромами;
зменшення ОВП між сусідніми цитохромами кожного наступного переносника.
В дихальному ланцюзі розрізняють 4 функціональні комплекси (I, II, III, IV), кожен з яких каталізує певну частину реакцій ланцюга. В цих комплексах здійснюються такі перетворення, крім:
перенос електронів від НАДН до убіхінону;
перенос „е” від сукцинату до убіхінону;
перенос „е” від убіхінону до цитохрому с;
перенос „е” від цитохрому с до кисню;
*перенос „е” від цитохрому „в” до кисню.
Існує ряд речовин, що блокують перенос „е” у дихальному ланцюгу. Так, барбітурати і ротенон інгібують перенос „е” на рівні:
*НАДН - КоQ;
сукцинат – КоQ;
КоQ – цитохром в;
цитохром с – кисень;
цитохром в - цитохром с.
Антибіотик антиміцин А призупиняє транспорт „е” на рівні:
НАДН – КоQ;
сукцинат – КоQ;
КоQ – цитохром в;
*цитохром в - цитохром с;
цитохром с – кисень.
Інгібіторами цитохромоксидази є:
трифторацетон;
антиміцин;
барбітурати;
холестерин;
*ціаніди, СО, сірководень.
При перенесенні 2х „е” від НАДН до О2 ОВП зростає до +0,82 В,при цьому зміна вільної енергії становить 220 кДж, що достатньо для синтезу не менше 4 АТФ, а при переносі „е” від ФАДН2 до О2 кількість вільної енергії менша на 50 кДж/м. Це вказує на те, що:
енергія окиснення виділяється порціями;
наявність трьох ділянок в ланцюзі транспорту „е”, де перепад енергії достатній для утворення 1 молекули АТФ;
частина енергії транспорту „е” витрачається у вигляді тепла;
в міру зростання величини ОВП компонентів дихального ланцюга відбувається розсіювання (зменшення) вільної енергії відщеплених „е”;
*кількість утворених молекул АТФ залежить від виду кофермкнтів дегідрогеназ.
При переносі „е” від НАДН до кисню синтезується 3 молекули АТФ. Вкажіть ділянки дихального ланцюга, де перенос вільної енергії електронів недостатній для утворення 1 молекули АТФ:
НАДН → ФМН;
цитохром в → цитохром с1;
НАДН → ФМН;
цитохроми а1, а3 → кисень;
*ФАДН2 → КоQ.
Кількість АТФ утвореного у дихальному ланцюгу виражають відношенням Р/О (коефіцієнт фосфорилювання), яке відповідає кількості Фн, включеного у АТФ із розрахунку на один атом спожитого кисню. Коефіцієнт фосфорилювання буде менший 2 при окисненні таких субстратів:
ФАДН2;
*аскорбат;
КоQН2;
сукцинат;
НАДН.
До тканинного дихання мають відношення всі речовини, крім:
пантотенова кислота;
тіаміндифосфат;
рибофлавін;
ніацин;
*піридоксальфосфат.
Субстратами тканинного дихання можуть бути всі речовини, крім:
сукцинат;
*лактат;
ізоцитрат;
малат;
α-кетоглутарат.
Потрапляння в організм ціаніду калію викликає смерть протягом кількох хвилин внаслідок утворення міцного комплексу з двовалентним залізом у складі ферменту:
*цитохромоксидази;
АТФ-синтетази;
каталази;
гемоглобіну;
пероксидази.
Дихальний ланцюг у мітохондріях виконує функції:
перенос електронів на цитохроми;
окиснення речовин до СО2 і Н2О;
перетворення речовин і енергії;
забезпечення клітин НАД+ і ФАД;
*перенос електронів від НАДН2 на кисень з утворенням АТФ.
Послідовність компонентів дихального ланцюга визначається:
вибірковою здатністю акцептувати і передавати електрони;
подібністю в структурі сусідніх переносників електронів;
розчинністю у воді;
прагненням пар окиснення-відновлення до розсіювання вільної енергії;
*збільшенням величини окисно-відновного потенціалу між сусідніми компонентами ланцюга.
Для багатьох патологічних процесів характерним є виникнення стану гіпоксії, під час якої при неповному відновленні кисню утворюється пероксид водню. Який фермент розщеплює його?
*Каталаза.
Цитохромоксидаза.
Лактатдегідрогеназа.
Еластаза.
Фосфогексокіназа.
Процес окиснювального фосфорилювання (утворення АТФ із АДФ і Фн) поєднаний із переносом „е” по дихальному ланцюгу. Про це засвідчують такі факти, крім:
окиснення НАДН супроводжується утворенням АТФ;
окиснення у мітохондріях ФАДН2 веде до утворення АТФ;
у присутності інгібіторів дихального ланцюга (ротенон, антиміцин, чадний газ) утворення АТФ зменшується;
у присутності роз’єднувачів дихання і фосфорилювання (вільні жирні кислоти, динітрофенол та ін) транспорт електронів по дихальному ланцюгу не порушується, але АТФ не утворється;
*фосфопіридоксаль та лактат не впливають на утворення АТФ.
Хворий протягом тривалого часу піддавався впливу радіації, внаслідок чого в нього встановлено посилення вільнорадикального пероксидного окиснення. Як це впливає на окисне фосфорилювання АТФ?
зовсім не впливає;
підсилить окисне фосфорилювання;
викличе незначне підсилення окисного фосфорилювання;
*пригнітить окисне фосфорилювання;
в різних тканинах будуть різні зміни в процесі фосфорилювання.
Субстратами дихального ланцюга є продукти, що утворюються переважно:
в цитоплазмі;
в процесі гліколізу;
*в циклі трикарбонових кислот;
в ендоплазматичній сітці;
в ході глюконеогенезу.
До піруватдегідрогеназного шляху входять три ферменти:
піруваткарбоксилаза, лактатдегідрогеназа, цитратсинтаза;
*піруватдегідрогеназа, дигідроліпоілацетилтрансфераза, дигідроліпоілдегідрогеназа;
цитратсинтаза, піруваткарбоксилаза, карбангідраза;
дигідроліпоілдегідрогеназа, сукцинілтіолаза, аргіназа;
ацетилтрансфераза, лактатдегідрогеназа, аконітаза.
При гіпоксичних станах енергопостачання клітин і тканин здійснюється за допомогою:
каталізу;
глюконеогенезу;
окиснення жирних кислот;
пентафосфатного циклу;
*гліколізу.
Найменш енергетичним субстратом дихального ланцюга є:
сукцинат;
НАДН2;
КоQН2;
ФАДН2;
*аскорбат.
Скільки молекул АТФ утворюється при повному окисненні оцтової кислоти до СО2 і Н2О?
1 молекула АТФ;
24 молекули АТФ;
*12 молекул АТФ;
3 молекули АТФ;
38 молекул АТФ.
Скільки молекул АТФ утворюється при повному окисненні піровиноградної кислоти до СО2 і Н2О?
24 молекули АТФ;
12 молекул АТФ;
*15 молекул АТФ;
28 молекул АТФ;
1 молекула АТФ.
Скільки молекул АТФ утворюється при повному окисненні глутамінової кислоти до СО2 і Н2О?
3 молекули АТФ;
6 молекул АТФ;
*9 молекул АТФ;
12 молекул АТФ;
24 молекули АТФ.
Інтенсивність дихання (транспорту електронів) в клітині залежить від співвідношення АДФ:АТФ. Швидкість дихання збільшується за таких умов:
при зростання вмісту АТФ;
при зменшенні вмісту АТФ;
при зменшенні вмісту АДФ;
*при збільшенні вмісту АДФ;
при рівності АДФ=АТФ.
Витрачання в клітині АТФ призводить до зростання рівня АДФ, що автоматично викликає:
пригнічення дихання;
*стимуляцію дихання;
посилення анаболізму вуглеводів, ліпідів, білків;
роз’єднання процесів дихання і фосфорилювання;
не впливає на метаболізм.
Енергетичний заряд клітини знаходиться в межах від 0 до 1.0. В стані спокою величина його близька 0.8. Підвищення величини енергетичного заряду вказує на:
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 2448; Нарушение авторских прав?; Мы поможем в написании вашей работы!