
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Практична робота №1. Дано: N(NaON)=0,15н V(HCl)=21,0мл N(HCl)=0,113н Знайти:V(NaOH)-?
|
|
|
|
168.
166.
Дано: N(NaON)=0,15н V(HCl)=21,0мл N(HCl)=0,113н Знайти:V(NaOH)-?
Розв’язання:  =
= 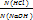 ; V(NaOH) =
; V(NaOH) = 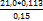 =15,82 мл.
=15,82 мл.
167. Характектерна реакція на катіони Fe2+
Калій гексаціаноферат (III) K3[Fe(CN)6] (фармакопейна реакція) утворює з йонами Fe2+синій осад Fe3[Fe(CN)6]2, так звану турнбулеву синь:
3Fe2++ 2[Fe(CN)6]3–= Fe3[Fe(CN)6]2¯
3FeCl2 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2¯ + 6KCl
Характерна реакція на аніон SO42–
Барій хлорид (фармакопейна реакція), взаємодіючи з сульфат-йонами, утворює білий кристалічний осад, який майже не розчиняється у воді й кислотах:
SO42–+ Ba2+= BaSO4¯
FeSO4 + BaCl2 = BaSO4¯ + FeCl2
Дано: N(NaON)=0,12н V( )=25,0мл N(
)=25,0мл N( )=0,2н Знайти:V(NaOH)-?
)=0,2н Знайти:V(NaOH)-?
Розв’язання: 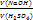 =
= 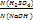
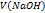 =
= 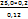 =41,6 мл.
=41,6 мл.
169. Характерна реакція на Сu2+
Водний розчин аміаку (фармакопейна реакція), доданий у надлишку, утворює з іонами Cu2+ комплексну сполуку інтенсивно-синього кольору:
2CuCl2 + 2NH4OH = (CuOH)Cl¯ + (NH4)Cl
Характерна реакція на аніон Cl–
Аргентум нітрат осаджує білий осад AgCl, який не розчиняється в розведених кислотах, але добре розчиняється у водному розчині NH3, утворюючи добре розчинну у воді комплексну сполуку – Аргентум аміакат:
Ag+ + Cl–= AgCl¯;
AgCl + 2NH3= [Ag(NH3)2]++ Cl–
CuCl2 + 2AgNO3 = 2AgCl¯ + Cu(NO3)2
171. Характерна реакція на Сu2+
Водний розчин аміаку (фармакопейна реакція), доданий у надлишку, утворює з іонами Cu2+ комплексну сполуку інтенсивно-синього кольору:
2CuSO4 + 2NH4OH = (CuOH)2SO4¯ + (NH4)2SO4
Характерна реакція на аніон SO42–
Барій хлорид (фармакопейна реакція), взаємодіючи з сульфат-йонами, утворює білий кристалічний осад, який майже не розчиняється у воді й кислотах:
SO42–+ Ba2+= BaSO4¯
CuSO4 + BaCl2 = BaSO4¯ + CuCl2
172. Характерна реакція на катіон Ва2+
Калій дихромат осаджує з розчинів Ва2+ у вигляді осаду BaCrO4жовтого кольору:
2BaCl2+ K2Cr2O7+ 2CH3COONa + H20 = 2BaCrO4 ¯ + 2KCl + 2NaCl + 2CH3COOH
|
|
|
Характерна реакція на аніон Cl–
Аргентум нітрат осаджує білий осад AgCl, який не розчиняється в розведених кислотах, але добре розчиняється у водному розчині NH3, утворюючи добре розчинну у воді комплексну сполуку – Аргентум аміакат:
Ag+ + Cl–= AgCl¯;
AgCl + 2NH3= [Ag(NH3)2]++ Cl–
BaCl2 + 2AgNO3 = 2AgCl¯ + Ba(NO3)2
173. Метод нейтралізації застосовується для визначення концентрації кислот,основ,а також солей,які піддаються гідролізу. Так цей мето лежить в основі визначення кислотного числа олій, кислотності молока, маргарину та деяких інших продуктів.
Тема: Аналіз особливостей історичних етапів взаємодії суспільства і природи
Мета. З’ясувати особливості впливу людського суспільства на біосферу на різних етапах взаємодії людини і природи; розвивати вміння встановлювати причинно-наслідкові зв’язки
Обладнання: інструкції до виконання, роздатковий дидактичний матеріал
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 608; Нарушение авторских прав?; Мы поможем в написании вашей работы!