
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структура. Диаграмма водяного пара
|
|
|
|
Справочный материал
Диаграмма водяного пара
Практическое занятие № 9
Цель работы: изучить процесс парообразования и представления в h-s диаграмме.
H, s-диагра́мма (чит. «аш-эс-диаграмма») (написание строчными буквами:«h,s-диаграмма»,) — диаграмма теплофизических свойств жидкости и газа (в основном воды и водяного пара), показывающая характер изменения различных свойств, в зависимости от параметров состояния.
В основном большое применение получили h, s-диаграммы воды и водяного пара, так как в качестве рабочего тела втеплотехнике чаще всего применяются именно вода и водяной пар, из-за их сравнительной дешевизны и доступности, причём наиболее пристальное внимание оказывается именно той части диаграммы, в которой вода впарообразном состоянии, так как в жидком состоянии она практически несжимаема.
Ещё в 1904 году немецкий теплофизик Рихард Молье разработал специальную диаграмму для упрощения и облегчения решений практических задач по теплотехнике, в которой в координатах энтальпии (h) и энтропии (s) графически отображаются сведения из таблиц состояний. В 1906 году в Берлине была издана его книга «Новые таблицы и диаграммы для водяного пара». Впоследствии такая диаграмма получила название Диаграмма Молье. В СССР некоторое время было принято название i, s-диаграмма, а в настоящее время - h, s-диаграмма.
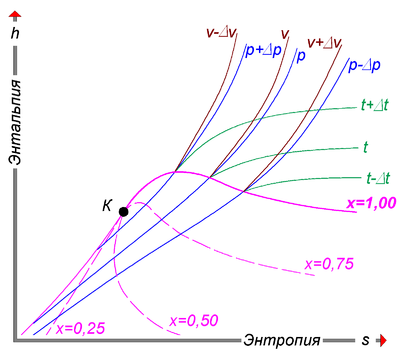
Структура h, s-диаграммы
H, s-диаграммы чаще всего содержат в себе данные о свойствах воды в жидком и газообразном состояниях, так как они представляют наибольший интерес с точки зрения теплотехники.
§ Степень сухости - это параметр, показывающий массовую долю насыщенного пара в смеси воды и водяного пара. Значение x = 0 соответствует воде в момент кипения (насыщения). Значение х = 1, показывает, что в смеси присутствует только пар. При нанесении соответствующих точек в координатах (h,s), взятых из таблиц насыщения справочников свойств воды и водяного пара, при их соединении получаются кривые, соответствующие определённым степеням сухости. В таком случае, линия х = 0 является нижней пограничной кривой, а х = 1 - верхней пограничной кривой. Область, заключённая между этими кривыми, является областью влажного пара. Область ниже кривой х = 0, которая стягивается практически в прямую линию (не показана), соответствует воде. Область выше кривой х = 1 - соответствует состоянию перегретого пара.
§ Критическая точка (К). При определённом, достаточно высоком давлении, называемом критическим, свойства воды и пара становятся идентичными. То есть исчезают физические различия между жидким и газообразным состояниями вещества. Такое состояние называют критическим состоянием вещества, которому соответствует положение критической точки. Следует заметить, что она на пограничной кривой лежит гораздо левее максимума этой кривой.
§ Изотерма - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённой температуре. Изотермы пересекают пограничные кривые с изломом и, по мере удаления от верхней пограничной кривой, асимптотически приближаются к горизонтали. На схеме для упрощения представлены только три изотермы: t + Δt; t; t - Δt.
§ Изобара - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённому давлению. Изобары не имеют изломов при пересечении пограничных кривых. На схеме представлены только три изобары:
§ p + Δp; p; p - Δp.
§ Изохора - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённому объёму. Изохоры на h, s-диаграмме в области перегретого пара, всегда проходит круче, чем изобары, и это облегчает их распознавание на одноцветных диаграммах. Построение изохор требует более кропотливой работы с таблицей состояний. На схеме представлены только три изохоры:
§ v - Δv; v; v + Δv.
Изотермы и изобары в области влажного пара совпадают по причине линейной зависимости в состоянии насыщения.
Определение параметров жидкости и пара по таблицам и h-s диаграмме
Таблицы для определения термодинамических свойств веществ различаются в зависимости от того, какое состояние рассматривается: однофазное или двухфазное. В таблицах для состояния насыщения приводятся удельные значения объема, энтальпии и энтропии воды и водяного пара (см. табл. 7 приложения); хладона R-22 (см. табл. 5 приложения); аммиака (см. табл. 6 приложения).
Параметры насыщенной жидкости (х = 0) отмечаются одним штрихом, Параметры сухого насыщенного пара (х = 1) отмечаются двумя штрихами.
Для определения свойств каждой из фаз в состоянии насыщения надо знать только один параметр – давление или температуру, так как при этих условиях параметры однозначно связаны между собой. В этих же таблицах приводится удельная теплота парообразования r.
Для расчета параметров влажного пара необходимо знать дополнительно степень сухости пара х.
Энтальпия h, энтропия s и удельный объем v влажного пара определяются по формулам: h = h˝·x + h΄·(1–x) = h΄+ r · x,
s = s˝∙x + s΄·(1–x) = s΄+ r·x/ТS,
v = v˝· x + v΄· (1–x).
Степень сухости пара определяется по одной из следующих формул:
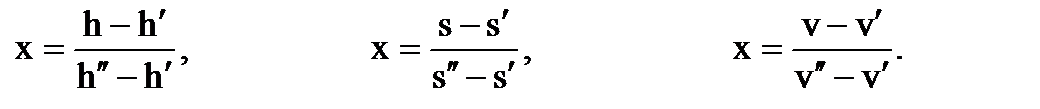
Для определения свойств ненасыщенной жидкости и перегретого пара (однофазное состояние) нужно знать два параметра (обычно давление и температуру). В ячейке таблицы, соответствующей данному состоянию, помещены удельные значения объема v, энтальпии h и энтропии s.
На h-s диаграмме обычно изображаются:
линии изобар (p = const);
| t = const |
| x =1 |
| h |
| v |
| Рис. 1. h-s диаграмма |
| p |
| s |
| x =const |
линии изотерм (t = const); в области влажного пара изотермы не представлены, так как они совпадают с изобарами; изохоры (v = const) – пунктирной линией или линией другого цвета;линии постоянной степени сухости влажного пара (x = const) ‑ в области влажного насыщенного пара.
| hА=2480 кДж/кг |
| А |
| sА =6,58 кДж/(кг·К) |
| x =1 |
| h |
| xА=0,9 |
| pА=2 бар |
| tн =120ºС |
| Рис. 2. |
Решение: по h-s диаграмме:
Решение по таблице:из таблицы водяного пара находим параметры кипящей воды «′» и сухого насыщенного пара «″» при 2,0·105 Па
| р | tн | v′ | v″ | h′ | h″ | r | s′ | s″ |
| Па | ºC | м3/кг | м3/кг | кДж/кг | кДж/кг | кДж/кг | кДж/ (кг·К) | кДж/ (кг·К) |
| 2,0·105 | 120,23 | 0,0010608 | 0,8859 | 504,7 | 2706,9 | 2202,2 | 1,5301 | 7,1286 |
По этим данным определяются энтальпия пара h и энтропия s:
h = h΄+ r·x = 504,7 + 2202,2·0,9 = 2486,68 кДж/кг.
s = s΄+ (r·x)/TS = 1,5301 + (2202,2·0,9)/(120,23+273) = 6,57 кДж/(кг·К).
Температура насыщения: tS = 120,23 ºС.
Задание: изучить структурудиаграммы состояния водяного пара
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 2681; Нарушение авторских прав?; Мы поможем в написании вашей работы!