
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретические сведения. В данной работе изучается зависимость парциально-молярных объемов компонентов раствора вода - этиловый спирт от химического состава
|
|
|
|
Работа № 5. ОПРЕДЕЛЕНИЕ ПАРЦИАЛЬНО-МОЛЯРНЫХ ОБЪЕМОВ КОМПОНЕНТОВ БИНАРНОГО РАСТВОРА
В данной работе изучается зависимость парциально-молярных объемов компонентов раствора "вода - этиловый спирт" от химического состава.
Подготовка к работе требует усвоения следующих разделов теоретического курса: понятие парциально-молярного свойства компонента раствора, уравнение Гиббса-Дюгема и следствия из него, идеальные растворы и причины отклонений от свойств идеальных растворов в реальных системах.
Любое экстенсивное свойство раствора при фиксированных температуре и давлении зависит от числа молей компонентов, составляющих раствор. Так, для бинарного раствора экстенсивное свойство 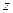 является функцией внешних параметров
является функцией внешних параметров 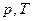 и чисел молей
и чисел молей 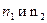 , то есть
, то есть
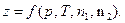
| (51) |
Полный дифференциал свойства может быть выражен через частные производные и приращения независимых переменных. Поэтому при постоянных 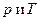 :
:

| (52) |
Частную производную экстенсивного свойства раствора 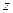 по числу молей данного компонента при постоянных
по числу молей данного компонента при постоянных 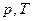 и числах молей остальных компонентов называют парциально-молярным свойством компонента. То есть парциально-молярное свойство
и числах молей остальных компонентов называют парциально-молярным свойством компонента. То есть парциально-молярное свойство 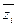 это приращение общего молярного свойства
это приращение общего молярного свойства 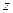 раствора, получающегося в результате добавления в раствор заданного состава бесконечно малого количества растворенного вещества при p, T = const и постоянном составе раствора, пересчитанное на 1 моль растворенного вещества:
раствора, получающегося в результате добавления в раствор заданного состава бесконечно малого количества растворенного вещества при p, T = const и постоянном составе раствора, пересчитанное на 1 моль растворенного вещества:
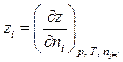
| (53) |
Представим уравнение (52) в виде
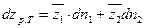
| (54) |
или для многокомпонентного раствора:
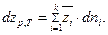
| (55) |
Парциально-молярные свойства компонентов раствора зависят от 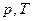 и химического состава, причем их изменения взаимно связаны. Эта связь при
и химического состава, причем их изменения взаимно связаны. Эта связь при 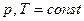 устанавливается уравнением Гиббса-Дюгема
устанавливается уравнением Гиббса-Дюгема
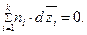
| (56) |
В случае бинарного раствора уравнение (55) может быть записано в форме
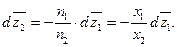
| (57) |
Из уравнения (57) следует, что приращения свойств 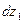 и
и 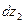 противоположны по знаку, то есть, если с увеличением концентрации одного из компонентов его парциально-молярное свойство растет, то для другого оно обязательно уменьшается. Анализ уравнения (57) показывает также, что интенсивнее с составом раствора меняется свойство компонента, концентрация которого в растворе меньше.
противоположны по знаку, то есть, если с увеличением концентрации одного из компонентов его парциально-молярное свойство растет, то для другого оно обязательно уменьшается. Анализ уравнения (57) показывает также, что интенсивнее с составом раствора меняется свойство компонента, концентрация которого в растворе меньше.
В данной лабораторной работе исследуются парциально-молярные свойства раствора на примере определения парциально-молярных объемов компонентов бинарного раствора, то есть общее молярное свойство z – это молярный объем Vm. И применяя приведенные выше выражения для системы «вода-спирт» получим:
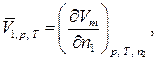 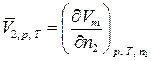
| (58) |
Уравнение Гиббса-Дюгема для парциально-молярных объемов компонентов бинарного раствора:
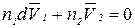
| (59) |
Поскольку любое свойство раствора складывается аддитивно из парциально-молярных свойств компонентов, то мольный объем бинарного раствора
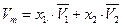
| (60) |
В этом выражении 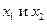 - мольные доли компонентов, равные отношению числа молей данного компонента к общему числу молей всех компонентов раствора.
- мольные доли компонентов, равные отношению числа молей данного компонента к общему числу молей всех компонентов раствора.
Часто для определения величин 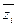 компонентов бинарного раствора используют графический метод, требующий знания зависимости мольного свойства
компонентов бинарного раствора используют графический метод, требующий знания зависимости мольного свойства 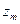 от мольной доли одного из компонентов.
от мольной доли одного из компонентов.
Допустим, эта зависимость для молярного объема известна и представлена на рис. 10.
Докажем, что отрезок Оа, отсекаемый касательной AM, проведенной к кривой 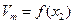 в точке М, численно равен парциально-молярному объему первого компонента в растворе состава
в точке М, численно равен парциально-молярному объему первого компонента в растворе состава 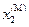 .Из рисунка следует, что для любой выбранной мольной доли второго компонента (
.Из рисунка следует, что для любой выбранной мольной доли второго компонента (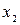 ), в том числе и для
), в том числе и для 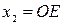 , справедливо равенство:
, справедливо равенство:
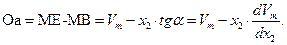
| (61) |
В бинарном растворе
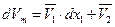 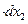 , ,
| (62) |
a 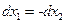 , т.к.
, т.к. 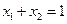 .
.

Рис. 10 – к определению парциально-молярных объемов раствора
Учитывая это обстоятельство и соотношение (57), запишем равенство (58) в виде:

| (63) |
Таким образом, отрезок Оа, отсекаемый касательной на оси ординат при 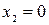 , равен парциально-молярному объему первого компонента. Аналогично отрезок, отсекаемый этой касательной аb на оси ординат справа, то есть при
, равен парциально-молярному объему первого компонента. Аналогично отрезок, отсекаемый этой касательной аb на оси ординат справа, то есть при 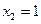 , соответствует величине
, соответствует величине 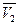 .
.
Кривая 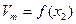 на рис. 10 проходит ниже аддитивной прямой (пунктир), характерной для идеальных растворов, где
на рис. 10 проходит ниже аддитивной прямой (пунктир), характерной для идеальных растворов, где
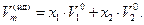
| (64) |
Причиной отклонения молярного объема реального раствора от такового для идеального является различие в энергиях связи между различными частицами раствора. Если энергия связи разноименных частиц (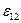 ) больше средней энергии связи одноименных (
) больше средней энергии связи одноименных (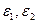 ), то есть
), то есть
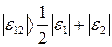 , ,
| (65) |
и образование раствора сопровождается его уплотнением.
Подобная зависимость характерна для растворов с отрицательными отклонениями от идеального раствора. При значительных различиях в энергиях связи парциально-молярный объём компонента может оказаться отрицательным, что говорит об уменьшении общего объема раствора при добавлении к нему данного компонента.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 818; Нарушение авторских прав?; Мы поможем в написании вашей работы!