
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоемкость идеального газа
|
|
|
|
Элементы термодинамики
Теплоемкость тела - физическая величина равная производной от количества тепла по температуре.

Теплоемкость вещества из которого изготовлено тело подразделяют на удельную(с) –для 1 кг и молярную (С) – для 1 моля 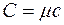
Для газа различают, в зависимости от условий в которых происходит нагрев газа, следующие теплоемкости:
1.  - молярная теплоемкость при постоянном объеме V=const
- молярная теплоемкость при постоянном объеме V=const
2.  - молярная теплоемкость при постоянном давлении Р=const
- молярная теплоемкость при постоянном давлении Р=const
 =
=  - уравнение Майера
- уравнение Майера
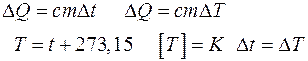
(градус Кельвина)  (градус Цельсия)
(градус Цельсия)

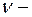 количества вещества в молях, С- молярные теплоемкости.
количества вещества в молях, С- молярные теплоемкости.
| 0С | -18 | -10 | |||||||
| 0F |
Количество теплоты, которое нужно подвести к газу при постоянном давлении больше чем при постоянном объеме связано это с тем что при постоянном давлении часть теплоты передаваемой газу переходит не во внутреннюю энергию, а идет на совершение работы при расширении газа.
Для идеального газа внутренняя энергия складывается исключительно из кинетической энергии поступательного движения бесконечно малых молекул идеального газа.
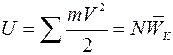 где N - число молекул.
где N - число молекул.
Число степеней свободы механической системы - это количество независимых координат, с помощью которых может быть задано положение системы в пространстве. Если молекула рассматривается как бесконечно малый шарик, то её положение в пространстве задается координатами (x, y, z).
i - степень свободы.
Если молекула двухатомная, то i=5, помимо трех координат поступательного движения эту молекулу будут определять еще две координаты вращательного движения.
Если же от идеального газа мы переходим к реальному газу, то есть, учитываем конечные размеры молекул или учитываем, что молекулы взаимодействуют дуг с другом, то к внутренней кинетической энергии поступательного или вращательного движения нужно добавить энергию взаимодействия молекул или энергию колебательного движения.
ЗАКОН О РАВНОРАСПРЕДЕЛЕНИИ ЭНЕРГИИ МОЛЕКУЛ ПО СТЕПЕНЯМ СВОБОДЫ:
1. На каждую степень свободы приходится одинаковая энергия равная 
2. Молекула одноатомная  - три поступательные степени свободы:
- три поступательные степени свободы:
3. 
4. Молекула двухатомная- РИС!!!!- три поступательные степени свободы и две вращательные:
5. 
6. 
7. Молекула трехатомная- РИС!!!!- три поступательные степени свободы и три вращательные:
8.
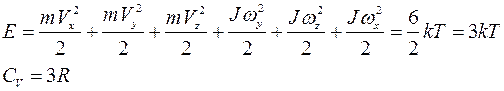
Равновесное состояние термодинамической системы определяется постоянством значений макроскопических величин, характеризующих это состояние.
 P=const
P=const
T=const
Параметры состояния
V=const
U=const
Обратимым называют такой термодинамический процесс перехода системы из состояния А в состояние В который, будучи проведен в обратном направлении, возвращает систему в исходное состояние, проходя через те же промежуточные состояния в обратной последовательности, а состояние тел вне термодинамической системы остались неизменными.
Обратимый процесс - процесс, при котором система переходит из состояния А в В и возможно вернуть ее хотя бы одним способом в исходное состояние А и при том так, чтобы во всех остальных телах не произошло никаких изменений.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 568; Нарушение авторских прав?; Мы поможем в написании вашей работы!