
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Неинвазивный мониторинг газов крови
|
|
|
|
Кроме прямого определения PaO2, PaCO2, SaO2, широко используются методы неинвазивного контроля газов крови: оксиметрия, OK-сигемография, чрескожное определение PO2, капнография и др.
Оксиметрия — оптический метод определения насыщения гемоглобина крови, основанный на специфических различиях спектральных свойств оксигемоглобина и восстановленного гемоглобина.
Пульсоксиметрия. Фотоэлемент на пульсоксиметре способен принимать изменения преходящего света вследствие артериальной пульсации и неизмененный свет от вен и других непульсирующих элементов. Обрабатывается только измененный входящий свет. На данные пульсоксиметрии не влияют толщина тканей, их плотность или пигментация. В ряде сообщений отмечается высокая точность пульсовой оксиметрии, однако точность измерения при SaO2 ниже 70 % сильно варьирует.
В настоящее время пульсоксиметрия — рутинный метод, применяемый в ОРИТ. Однако необходимо помнить, что пульсоксиметрия имеет довольно высокую точность измерения при отсутствии гемодинамических нарушений и снижении SaO2 до 70 % и ниже.
Чрескожное измерение PO2. Для этой цели используют чрескожные кислородные электроды, представляющие собой миниатюрный аналог электрода Кларка. Доказана надежность этого метода у новорожденных. Однако у взрослых этот показатель варьирует, что ограничивает его применение. Точность

Рис. 8.1. Капнограмма. Изменения PCU2 в начале и конце выдоха.
чрескожного измерения PO2 определяется адекватностью периферического кровообращения. При снижении периферического кровотока PO2 снижается более значительно, чем PaO2.
Следует иметь в виду, что данные оксиметрии могут быть недостоверными у больных с выраженной недостаточностью правых отделов сердца или резкой артериальной гипотензией. Насыщение оксигемоглобина менее 85 % при FiO2>0,6 с одновременной гиперкапнией или без нее подтверждают клиническую симптоматику дыхательной недостаточности, требующей ИВЛ.
Измерение минутной вентиляции во время ИВЛ в сочетании с измерением PCO2 и PO2 в крови и дыхательной смеси дают возможность рассчитать физиологическое МП, выделение CO2 и потребление кислорода.
Капнография — метод непрерывной графической регистрации, осуществляемый с помощью инфракрасного анализатора концентрации CO2 в выдыхаемом воздухе. При капнографии неинвазив-ным путем определяют уровень артериального PCO2. В основу метода положена способность CO2 поглощать инфракрасное излучение пропорционально содержанию CO2.
Нормальная кривая элиминации CO2 в выдыхаемом воздухе представляет собой постепенное увеличение концентрации CO2, достигающее своего максимума в конце выдоха (рис. 8.1). При этом капнограмма приобретает форму плато. Этот максимум концентрации CO2 остается до начала следующего вдоха. При нормальной функции легких PCO2 в выдыхаемом воздухе в конце спокойного выдоха (EjCO2) эквивалентно PCO2 в дистально-ка-пиллярной (артериальной) крови.
В норме PaCO2 и FiCO2 в конце спокойного выдоха могут отличаться друг от друга всего на несколько миллиметров ртутного столба. Таким образом, имеется тесная взаимосвязь между ЕТСО2 и PaCO2. Прогрессирующее увеличение уровня CO2 в конце выдоха, независимо от причины, характерно для вентиляционной дыхательной недостаточности. У больных ХНЗЛ величина PCO2 в конце выдоха приближается по своему значению к таковой в смешанной венозной крови, но и в этих случаях различия PaCO2 и FiCO2 не превышают нескольких миллиметров ртутного столба. При выраженной сердечно-легочной патологии EjCO2 обычно ниже, чем PaCO2. Увеличение градиента PaCO2/FiCO2 связано с неперфузи-руемыми альвеолами, низким сердечным выбросом или увеличением физиологического мертвого пространства. Превышение показателя FiCO2 по сравнению с PaCO2 нетипично, но может наблюдаться при чрезмерной альвеолярной вентиляции, высоком FiO2, чрезмерном образовании CO2. Внезапное снижение FiCO2 возможно при эмболии легочной артерии, ателектазе, сепсисе и пневмонии. Обычно причиной возрастания FiCO2 является гиповентиляция, нередко на фоне анаэробного обмена и метаболического ацидоза.
Капнография и измерение FiСО2 находят широкое применение при ИВЛ, во время отключения больного от респиратора, используются для выявления осложнений ИВЛ (отсоединение трубок, негерметичность дыхательного контура и т.д.). Мониторинг FiСО2 помогает поддерживать необходимый уровень гипервентиляции у больных с черепно-мозговой травмой или в случаях, когда установленный уровень гипервентиляции необходим для контроля внутричерепного давления. Этот метод используют также для оценки эффективности СЛР. При этом снижение PeCO2 (PCO2 в выдыхаемом воздухе) ниже 10 мм рт.ст. является плохим прогностическим признаком. Применение капнографии в последнее время стало своеобразным эквивалентом уровня развития анестезиолого-реа-нимационной службы.
Эффекты мертвого пространства (МП). Измерить объем физиологического МП во время ИВЛ можно с помощью уравнения Бора:
VD/VJ = (PaCO2 - РЕСО2)/РаСО2,
где VD — физиологическое мертвое пространство; VT —· дыхательный объем; РкСО2 — давление CO2 в выдыхаемом воздухе. Остальные показатели известны.
Для определения PeCO2 выдыхаемый воздух собирают в большой мешок и с помощью инфракрасного анализатора измеряют среднее PCO2 [Марино П., 1998].
При возрастании объема физиологического МП исходный режим ИВЛ с нормальными значениями PaO2 и PaCO2 будет сопровождаться постепенным снижением PaO2 и возрастанием PaCO2. Этот феномен обусловлен вентиляцией увеличен-
ного объема МП, что связано с увеличением числа неперфузируемых альвеол.
Эффекты шунта и венозного примешивания. Истинный шунт указывает на отсутствие газообмена между кровью и альвеолярным газом. Венозное примешивание — это кровь, которая не полностью уравновешивается с альвеолярным газом, т.е. не подвергается в легких полноценной оксигенации. Эффекты шунта и венозного примешивания обусловлены главным образом падением PaO2. При этом изменений PCO2 не происходит до тех пор, пока величина шунта не достигнет 50 % от величины CB. Для того чтобы определить фракцию венозного примешивания непосредственно у постели больного, необходимо точное и одновременное измерение параметров PaO2 и FiO2. Если шунт меньше 10 %, что соответствует норме, любое, даже незначительное, увеличение фракции кислорода во вдыхаемом воздухе будет способствовать повышению PaO2. При возрастании величины шунта увеличение FiO2 сопровождается меньшим повышением PaO2. Так, при величине шунта 20 % от величины CB потребуется увеличить FiO2 до 0,6, чтобы поддержать оксигенацию на нормальном уровне. Если же величина шунта достигнет 50 %, PaO2 уже не реагирует на дальнейшее повышение FiO2. Исходя из этого, не следует применять токсические концентрации кислорода, а нужно использовать другие методы уменьшения фракции шунта (например, ПДКВ) (рис. 8.2).
Фракция шунта (QS/QT) может быть вычислена по следующей формуле:
Qs/QT = CcO2 - СаО2/(СсО2 - CvO2),
где CaO2 — содержание кислорода в артериальной крови; CvO2 — содержание кислорода в смешанной венозной крови; CcO2 — содержа-
ние кислорода в легочной капиллярной крови; QT — сердечный выброс; Qs — фракция шунта.
В норме отношение QS/QT = 0,1.
В связи с тем, что CcO2 непосредственно измерить невозможно, рекомендуют дышать чистым кислородом (FiO2 = 1,0), чтобы полностью насытить им гемоглобин крови легочных капилляров. Тогда ScO2 будет равно 100 %. Этот метод позволяет определить фракцию истинного шунта [Марино П., 1998].
При тяжелой патологии легких (пневмония, отек легких, тромбоэмболия легочной артерии) нарушение в них газообмена больше напоминает истинный легочный шунт.
Вычисление отношения PaO2/FiO2 — простой способ расчета показателя, который достаточно хорошо коррелирует с изменениями фракции шунта. Так, если PaO2/FiO2<200, то величина шунта более 20 % величины CB. Если же PaO2/FiO2>200, то величина шунта менее 20 % величины общего кровотока.
Альвеолярно-артериальная разница по кислороду. РАО2 в альвеолярном газе можно рассчитать по следующей упрощенной формуле:
РА02 = PiO2 - (PaC02/RQ),
где PiO2 — парциальное давление кислорода во вдыхаемом газе; RQ — дыхательный коэффициент (отношение между продукцией CO2 и потреблением кислорода).
Значение А/а-градиента PO2 у здоровых людей зависит от изменений FiO2. Так, при FiO2 0,21 (атмосферный воздух) этот градиент составит от 10 до 20 мм рт.ст. При FiO2 1,0 А/а-градиент PO2 от 60 до 70 мм рт.ст. Происходит увеличение А/а-градиента PO2 на 5—7 мм рт.ст. на каждые 10 % возрастания FiO2. При тяжелой легочной патологии РА02/РаО2 значительно превышает нормальные значения. Атмосферное
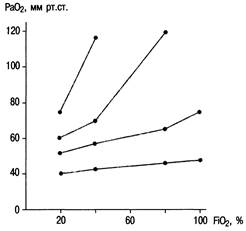
Рис. 8.2. Определение фракции шунта по соотношению FiU2 и PaU2 [D'Alon-zoG.E., 1983].
давление в норме составляет около 760 мм рт.ст., поэтому применение положительного давления при ИВЛ приведет к возрастанию PiO2. Для более точного расчета следует величину среднего давления в дыхательных путях добавлять к величине атмосферного давления.
Соотношение PaO2/FiO2 дает важную информацию о кислородном обмене. Снижение этого показателя до 150 и ниже свидетельствует о крайней степени легочной недостаточности и сопровождается высокой летальностью.
Постоянное измерение насыщения смешанной венозной крови позволяет характеризовать доставку и потребление кислорода и эффект терапии у большинства больных с нарушением газообмена и гемодинамики.
Податливость (растяжимость) легких можно определить при измерении ДО и давления дыхательного плато. По разнице между пиковым давлением на вдохе и давлением во время дыхательного плато можно рассчитать сопротивление дыхательных путей. Современные автоматизированные системы мониторинга выводят эти производные показатели при помощи компьютера в виде цифровых или графических изображений. В настоящее время мы не располагаем экспресс-методиками оценки работы дыхания при спонтанной вентиляции.
Указанные параметры вентиляции и газообмена очень часто бывают недостаточными для оценки дыхательной функции легких и других взаимозависимых систем. Расчет параметров кислородтранспортной системы невозможен без динамического определения MOC и СИ, содержания кислорода в артериальной и венозной крови. Поскольку функция легких во многом зависит от состояния водного баланса, проводят динамическое исследование водных секторов, КОД плазмы, ЦВД. У больных с сердечной недостаточностью измеряют давление в легочной артерии. Строго учитывают количество введенной и выделенной жидкости. Немаловажное значение имеют показатели реологических свойств и состояния свертывающей и антисвертывающей систем крови.
Глава 9 Острая обструкция дыхательных путей
Обструкция дыхательных путей — нарушение их проходимости — развивается вследствие воспалительных процессов (острый ларинготрахеобронхит), отека и спазма голосовой щели, аспирации, травмы. В некоторых случаях это чрезвычайно опасно, так как возможны тотальная обструкция дыхательных путей и быстрый смертельный исход.
Обструкции верхних и нижних дыхательных путей (ВДП и НДП) характеризуются разной симптоматикой и дифференцированным подходом к лечению.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 944; Нарушение авторских прав?; Мы поможем в написании вашей работы!