КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Семинар 3. Второе начало термодинамики. Энтропия
|
|
|
|
Ответы
Задачи
|
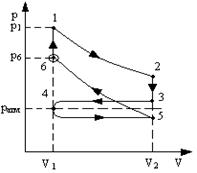
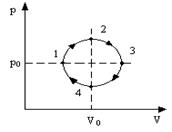 2.1. Циклический процесс представлен в координатах (p,V) в форме окружности с центром в точке (p0,V0), максимальный объем и давление равны соответственно Vmax и pmax. (рис.8) Изобразить на графике работу расширения, сжатия. Найти:
2.1. Циклический процесс представлен в координатах (p,V) в форме окружности с центром в точке (p0,V0), максимальный объем и давление равны соответственно Vmax и pmax. (рис.8) Изобразить на графике работу расширения, сжатия. Найти:
а) работу расширения;
б) работу сжатия;
|
 2.2. У тепловой машины, работающей по циклу Карно, температура нагревателя в α раз больше температуры холодильника. За один цикл машина производит работу А. Какая работа за цикл затрачивается на изотермическое сжатие? Решить эту же задачу, считая α=1,6; А=12 кДж.
2.2. У тепловой машины, работающей по циклу Карно, температура нагревателя в α раз больше температуры холодильника. За один цикл машина производит работу А. Какая работа за цикл затрачивается на изотермическое сжатие? Решить эту же задачу, считая α=1,6; А=12 кДж.
2.3. В каком случае КПД цикла Карно повысится больше: при увеличении температуры нагревателя на ∆Т или при уменьшении температуры холодильника на такую же величину?
2.4. Найти КПД цикла, проводимого с идеальным газом и состоящего из двух изотерм с температурами Т1 и Т2 и двух изохор с объемами V1 и V2.(Т1>T2, V1>V2)
|
|
2.6. Идеальный газ совершает цикл, состоящий из чередующихся изотерм и адиабат (рис.10). Температуры, при которых происходят изотермические процессы, равны Т1, Т2, Т3. Найти КПД такого цикла, если при каждом изотермическом расширении объем газа увеличивается в одно и тоже число раз.
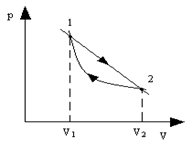
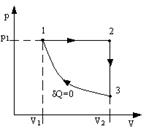
2.7. Определить КПД цикла, изображенного на рис.11. Переход 2-1 адиабата. Известны V1, V2, T1 и Cv=const.
|
|
случае цикл идеальный, считаем, что 5 совпадает с 3, путь 3-4 совпадает с 4-5 и работа на 4-5 не совершается.
2.9. Тепловую машину, работавшую по циклу Карно с КПД η=10%, используют при тех же тепловых резервуарах как холодильную машину. Найти ее КИЭ.
2.10. В помещении необходимо поддерживать температуру 25˚С, когда температура наружного воздуха 35˚С. Обеспечит ли требуемую температуру кондиционер, который при работе по циклу Карно в качестве тепловой машины имеет η=5%; на основе теоремы Карно оценить КИЭ данной машины.
2.11. Сделайте оценку (сверху) КИЭ бытового холодильника, если температура морозильной камеры - 20˚С.
2.1. 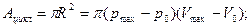
2.2. 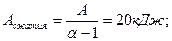
2.3. во втором;
 |
2.4.
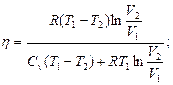
2.5. 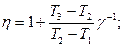
2.6. 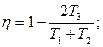
2.7. 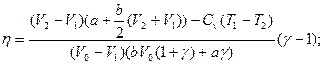
2.8. 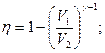
2.9. 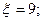
2.10. да;
2.11. 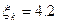
Второе начало термодинамики имеет особый статус не только фундаментального закона физики, но и универсального принципа естествознания в целом.
Второе начало дает информацию о направлении процессов, которые могут происходить в действительности. Оно, совместно с первым началом, позволяет установить множество точных количественных соотношений между различными макроскопическими параметрами тел в состоянии термодинамического равновесия. Это оказывается возможным благодаря определению такой величины как энтропия через теплоту. Энтропия (греч. – поворот, превращение) служит мерой преобразования или эволюции системы.
Существует несколько десятков различных формулировок второго начала. В большинстве из них термин «энтропия» не используется (см. формулировки Кельвина, Клаузиуса и Оствальда).
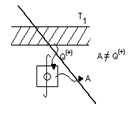
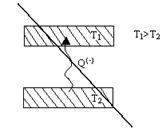
Такие процессы невозможны. Они запрещены вторым началом.
|
|
|
Часть первая. Каждая термодинамическая система обладает функцией состояния, называемой энтропией. Энтропия вычисляется следующим образом. Система переводится из произвольно выбранного начального состояния в соответствующее конечное состояние через последовательность состояний равновесия. Вычисляются все подводимые при этом к системе порции тепла 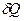 , делятся каждая на соответствующую ей абсолютную температуру Т и все полученные таким образом значения суммируются.
, делятся каждая на соответствующую ей абсолютную температуру Т и все полученные таким образом значения суммируются.
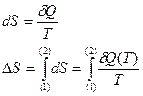 (13)
(13)
Часть вторая. При реальных (не идеальных) процессах энтропия замкнутой системы возрастает.
Содержание второй части формулировки А.Зоммерфельда в большинстве учебников рассматривается как самодостаточная формулировка второго начала, или как закон возрастания
энтропии:
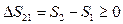 (14)
(14)
Энтропия не убывает только в процессах изолированной системы, в неизолированной системе энтропия может и возрастать,
и убывать, и оставаться неизменной. Рост энтропии в изолированной системе означает приближение системы к состоянию термодинамического равновесия; в этом состоянии S – максимальна, а dS=0. 
Расчет изменения энтропии в различных процессах изучаемых систем зачастую является актуальной внутренней подзадачей разнообразных задач термодинамики, химии биологии, лингвистики. В частности, изменение энтропии служит мерой изменения качества энергии. Важнейшим условием для тепловых машин, работающих по произвольному циклу, является условие их максимально допустимой эффективности:
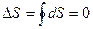 (за цикл) (15)
(за цикл) (15)
Большинство процессов, происходящих в природе, необратимы, например: диффузия, расширение, растворение. Для таких процессов вычисление энтропии основывается на том, что S – функция состояния. Если система перешла из одного состояния в другое необратимым образом, то можно мысленно заменить необратимый процесс обратимым, причем начальное и конечное состояния этого процесса должны быть равновесны, рассчитанное в этом случае изменение энтропии будет равно изменению энтропии при реальном необратимом процессе.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 1538; Нарушение авторских прав?; Мы поможем в написании вашей работы!