
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение Клапейрона-Клаузиуса
|
|
|
|

Все вещества могут существовать в различных агрегатных состояниях или в различных модификациях одного агрегатного состояния в зависимости от условий (Т, р и т.д.). Переход вещества из одного агрегатного состояния в другое, или изменение модификации агрегатного состояния вещества называется фазовым переходом первого рода. Фазовые переходы 1-го рода сопровождаются выделением или поглощением теплоты.
|
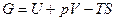 . (25)
. (25)
При динамическом равновесии выполняется уравнение:
 , (26)
, (26)
где g1 и g2 – удельные (относящиеся к единице массы вещества) термодинамические потенциалы 1-й и 2-й фаз.
Уравнение, связывающее между собой давление и температуру, при которых осуществляется фазовый переход первого рода, имеет вид

где  - удельный объем. Две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, зависящем от температуры.
- удельный объем. Две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, зависящем от температуры.
Максимально возможное число фаз вещества, находящихся в равновесии друг с другом равно трем, если это изобразить на плоскости p, T, то она получится разделена на три области: твердую фазу (т), жидкую (ж) и газообразную (г), рис.20
Границами соприкасающихся фаз являются кривые сублимации (испарение твердого тела), испарения и плавления, характеризующие двухфазные равновесные состояния.
|

|

|
|
|
Подобные диаграммы строят экспериментально для разных веществ, они позволяют предсказывать в каких равновесных состояниях может находиться вещество при тех или иных значениях давления и температуры, а также когда и какие оно будет испытывать фазовые превращения при том или ином процессе. Например, кривая испарения заканчивается в критической точке К, поэтому возможен непрерывный переход вещества из жидкого состояния в газообразное и обратно путем обхода точки К «сверху», в этом случае такой переход не сопровождается двухфазным состоянием.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 576; Нарушение авторских прав?; Мы поможем в написании вашей работы!