
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внебрюшинный, люмбоскопический доступ
|
|
|
|
Приоритет в разработке и клиническом внедрении внебрюшинных эндовидеоскопических доступов принадлежит урологам. Так, еще в 1979 г Wlckharn сообщил о люмбоскопической уретеролитотомии. Однако, впервые упоминание о непосредственной визуализации органов и тканей забрюшинного пространства с диагностической и лечебной целью мы нашли в работах M.Bartel (1969), выполнявших поясничную симпатэктомию. Анатомическое обоснование внебрюшинного доступа к почкам и мочеточникам в нашей стране было разработано М. Зильберманом и Б. Баевым (1978), дополнено В. Рублевским (1990) и Э. Перкиным. Они исследовали возможности внебрюшинного оперативного доступа к органам забрюшинного пространства методом прямой ретроперитонеоскопии. Авторы разработали методику прямой ретроперитонеоскопии с лечебной и диагностической целью. Метод заключается в том что с помощью специально созданного комплекса инструментов — ретроперитонеоскопа осуществлялись диагностические и лечебные манипуляции на органах забрюшинного пространства, и, в частности, на почках и мочеточниках. Несмотря на малую травматичность, высокую диагностическую ценность и реальные перспективы в развитии, по данным литературы этот метод не получил широкого распространения. Те же авторы в 1996 г. опубликовали результаты эндоскопической уретерокутанеостомии с применением разработанного ими инструментария.
С приходом эры эндовидеохирургических технологий появилась новая возможность совершенствования ретроперитонеоскопии (люмбоскопии) в диагностических и лечебных целях.
В 1993 г. D.D.Gaur с соавт. (1993) сообщили о ретроперитонеальной эндовидеоскопической нефрэктомии больному с калькулезным пиелонефри-том. Затем IS- Gill с соавт. (1994) используют люмбоскопический подход при нефрэктомии. В этом же году появляются сообщения JJ. Rassweiler с соавт. (1993) о 12 урологических операциях, включающих нефрэктомию, нефропексию и марсупилизацию кист почек. Аналогичный по количеству опыт обобщен в публикации Е.М. McDougall с соавт. (1994). Авторы также использовали баллонный способ создания ретропневмоперитонеума. В 1995 г. D.A.Diamond с соавт. сообщили о 3-ех успешных эндовидеоскопическкх нефрэктомиях у детей с использованием ретроперитонеального доступа, а H.Barreto с соавт. (1995) о 6 успешных люмбоскопических нефрэктомиях, 1 биопсии почки, и 1 операции иссечения кисты почки.
Принципиально «люмбоскопические«операции отличаются от лапароскопических тем, что не повреждается париетальная брюшина, что имеет важное значение при вскрытии мочевых путей во время оперативного пособия и наличии гнойных поражений органов и тканей забрюшинного пространства. Таким образом, значительно снижается риск послеоперационного перитонита, т.к. инфицированная моча или гной не попадают в брюшную полость во время операции и в послеоперационном периоде. Кроме того, практически полностью отсутствует травматизация органов брюшной полости, что уменьшает явления пареза и облегчает течение послеоперационного периода в целом.
Накопив начальный опыт люмбоскопических урологических операции, нами впервые в России была использована данная методика при выполнении адреналэктомии.
Теоретически, также как и при лапароскопической адреналэктомИИ, больной мажет находиться в положении на спине, на боку и на животе. Так, A. Mandressi с соавт. (1S95) сообщил о 6 успешных внебрюшинных адреналэктомиях при положении больного на спине. В начале освоения метода мы попытались выполнить подобную операцию, однако потерпели неудачу на этапе создания ретропневмоперитонеума, вследствие перфорации брюшины и истечения газа в брюшную полость. Оказалось очевидным, что для создания полости в забрюшинном пространстве приходится увеличивать показатель давления на инсуффляторе с целью создания так называемого газового забрюшинного купола, поднимающего достаточно большую массу органов брюшной полости. В результате очень сложно избежать перфорации брюшины.
Перевод больного в латеропозицию явился ключевым в разрешении этой проблемы. С одной стороны, мы вернулись к традиционной для открытых операций позиции больного. С другой стороны, «спонтанная ретракция» органов брюшной полости как бы снимает напряжение с париетальной брюшины. Достаточную для манипуляций полость в ретроперитонеальной клетчатке удается создать при минимальных цифрах давления инсуффлируемого газа. Даже в случае перфорации брюшины полость никогда полностью не спадается и ее объем зависит, главным образом, от физических свойств забрюшинной клетчатки. Таким образом, фактор латеропозиции, облегчавший выполнение трансабдоминальных вмешательств на надпочечнике, сыграл решающую роль при люмбоскопическом доступе.
Среди возможных способов создания ретроперитонеальной полости следует отметить:
— с использованием иглы Вереша;
— с использованием баллона;
создание полости через открытую минилюмботомию с последующей ее герметизацией «на троакаре»;
— с использ ованием тубуса лапароскопа.
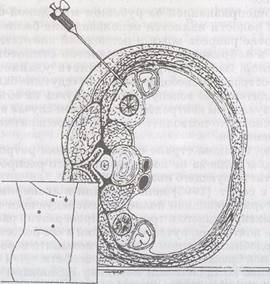
Рис.104. Создание ретропневмоперитонеума путем пункции иглой Вереша забрюшинного пространства (по de Can-mere L. et al., 1995)
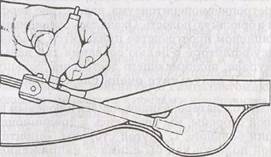
Рис.105. Создание ретпроперитонеальной полости с помощью баллона (по A.Heintz et al., 1994).
Ряд авторов [Mandressi A. et al., 1993; tie Canniere L. et al., 1995] создают ретропкевмоперитонеум в соответствии с классической техникой, принятой при выполнении лапароскопических операций. При этом игла Вереша вводится в забрюшинное пространство (рис.104). Некоторые авторы используют для этой цели ультразвуковой контроль.
В соответствии с данной методикой используют более щадящие режимы инсуффляции. Главным недостатком предложенного метода является опасность неконтролируемого распространения газа в забрюшинном пространстве с развитием пневмомедиастинума и пневмоперикардиума, С другой стороны, в связи с особенностями строения забрюшинной клетчатки, создать адекватную ретроперитонеальную полость с помощью иглы Вереша достаточно сложно.
Наиболее общепризнанной за рубежом методикой создания ретро-перитонеальной полости является использование баллонных троакаров (рис.105, 106}. После разреза кожи и подкожной клетчатки производится проникновение в забрюшинное пространство стилетом, содержащим сложенный баллон. Затем покрышка стилета удаляется, оставляя в забрюшинном пространстве свободно лежащий «сдутый» баллон. Раздувание баллона производится либо вслепую, ориентируясь на объем нагнетаемого газа, либо под визуальным контролем, В последнем случае в полость баллона вводится лапароскоп, что позволяет придать ретро перитонеальной полости элемент направленности.
К сожалению, в нашей стране способ создания ретроперитонеальнов полости с помощью баллона не получил широкого распространения из-за дороговизны соответствующего инструментария.
H.Shiozawa с соавт. (1995) использовали в эксперименте пальцевое создание ретроперитонеальнои полости с последующим введением в не презерватива, фиксированного к троакару. Презерватив раздувался под ла-пароскопическим контролем, путем нагнетания в его полость физиологического раствора. Подобным приемом удается уменьшить вероятность повреждения париетальной брюшины при создании полости.
Мы попытались воспроизвести методику H.Shiozawa с соват. (1995), соответствие с которой своеобразный баллон создавали путем фиксации эластичной резиновой полусферы на троакаре, однако нашли ее излишне усложняющей выполнение хирургического доступа.
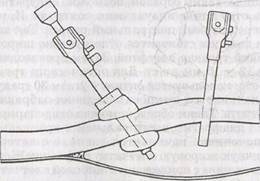
Рис.106. Установка дополнительного троакара после создания ретроперитонеальной полости (по A.Heintz et al., 1994).
Полость в забрюшинном пространстве через люмботомический доступ может быть создана пальцами кисти рук, тупфером, диссектором или любым другим инструментом. Особенно рационален данный способ для создания так называемой первичной ретроперитонеальнои полости. Под этим термином мы понимаем пространство в забрюшинной клетчатке до введения инструментальных троакаров. Мануальное создание первичной полости выгодно его относительной безопасностью вследствие постоянного тактильного контроля манипуляций. Инструментальные троакары могут быть также безопасно установлены под мануальным контролем.
М.К.Waltz с соавт. (1995) используют комбинированный способ создания ретропневмоперитонеума, при котором первоначальная полость создается открытым способом мануально или с помощью тупфера, с последующим увеличением ее объема раздуванием баллона. Вмешательство начинается с поперечного разреза длиной около 1,5 см на 2 см ниже 12 ребра, несколько латеральнее. Кожа, подкожная клетчатка и мышечная фасция рассекаются остро. Дальнейшая препаровка в направлении ретроперитонеального пространства осуществляется пальцами. Так без трудностей достигается фасция Жерота, которая прощупывается как тонкая пластинка. Она раскрывается кончиком пальца, как при пункции. Таким образом достигается забрюшинная жировая ткань. Непосредственно ниже фасции Жерота пальцем тупо, раздвигая жировую клетчатку, создается небольшая полость, которая затем с помощью баллонного троакара под эндоскопическим контролем в течение нескольких минут расширяется до размеров 6-8 см. Затем забрюшинная жировая клетчатка отодвигается вентрально и частично обнажаются каудально задние отделы диафрагмы.
После удаления баллонного троакара возникшая полость в забрюшинной клетчатке обследуется пальцем и под соответствующим контролем пальца Изнутри в эту полость вводится 10-мм троакар на 3 - 4 см латеральнее первого Разреза в краниальном направлении. При этом нужно иметь в виду, что между первым и вторым разрезом на фасции и мышечном слое должен быть оставлен Мостик ткани размером 3 см, соответствующий расстоянию на коже. Далее вводится 10-мм троакар в краниальном, слегка медиальном направлении На 3 — 4 см медиальнее первого разреза под контролем пальца, введенного Через первый разрез. При этом пальпируются латеральные отделы краниальной части m. iliopsoas и троакар вводится в образованную полость латерально от мышцы. Таким образом, возможно аккуратное введение троакара, несмотря на отсутствие визуального контроля. И, наконец, вводится третий троакар через первый центральный разрез. Так как первый доступ после препаровки пальцем становится относительно широким здесь применяется блокирующий троакар с муфтой. Затем производится инсуффляция газа до давления 12 - 15 мм рт ст. Для оптического троакара избирается медиальный разрез и используется оптика с углом 30 градусов.
Препаровка начинается с тупого отведения забрюшинной клетчатки задней фасции Жерота. Таким образом, можно отпрепарировать на большом протяжении купол диафрагмы в латеральном и краниальном направлении. Препаровка надпочечника начинается вначале с латеральной стороны включая и пограничную жировую клетчатку от фасции Жерота. Вентральная поверхность надпочечника с прилежащей жировой клетчаткой мобилизуется легко. Здесь рекомендуется тупая препаровка, например, тупфером на длинной рукоятке. Кроме того, этим приемом предупреждается перфорация брюшины или повреждение вентрально расположенных органов (справа — печень, слева — поджелудочная железа).
Недостатки данной методики связаны с большей агрессивностью и продолжительностью выполнения минилюмботомии по сравнении с люмбоскопией. С другой стороны, не всегда удается достичь надежной герметизации полости в связи с многочисленностью слоев мышц и не выраженностью апоневроза. В половине случаев мы наблюдали развитие обширных подкожных эмфизем, когда надежное ушивание поверхностного слоя мышц создавало предпосылки для распространения газа по межмышечным пространствам.
Мы в своей практике перешли к более простой и «дешевой» методике, предусматривающей создание направленной полости с помощью тубуса лапароскопа при медленной инсуффляции. В результате под постоянным визуальным контролем создается минимальная полость в забрюшинном пространстве, достаточная для выполнения оперативного приема. Методика заключается в следующем. Положение больного на здоровом боку с валиком и опущенным ножным концом операционного стола. Кожа в области разреза обрабатывается с соблюдением всех правил асептики и антисептики. В максимально верхней точке, ниже XII ребра, обычно по средней подмышечной линии или несколько кзади, производится разрез кожи и подкожной клетчатки длиной 1 см. Затем надсекается апоневроз. Тупым проводником через разрез кожи и апоневроза преодолевается мышечный слой. При этом инструмент как бы «проваливается» в забрюшинное пространство. По проводнику в забрющинное пространство вводится 10-мм троакар для лапароскопа. Тубусом лапароскопа создается первичная ретроперитонеальная полость. Цель создания этой полости не столько визуализировать зону основного оперативного приема, сколько создать условия для установки инструментальных троакаров. Поэтому параметры первичной полости определяются поставленной хирургической задачей, с точки зрения ее инструментального обеспечения. Исходя из величины угла осей оперативного действия, задается ширина полости, определяемая расстоянием между наиболее удаленными друг от друга троакарами перпендикулярно основной оптической оси. Под визуальным контролем отслаивается париетальная брюшина с прилежащей жировой клетчаткой при медленной инсуффляции газа (1~2 л/мин) при заданном давлении инсуффлятора 12 - 14 мм Не-Полость распространяется также на область предполагаемого введения других инструментальных троакаров. Все манипуляции необходимо выполнять весьма деликатно, так как в противоположном случае может возникнуть повреждение париетальной брюшины, что в свою очередь ухудшит параметры ретропневмоперитонеума и потребует введения дополнительных ретракторов. В случае если нарушения целостности брюшины избежать не удалось, рационально осуществить десуффляцию, что позволит переместить газ из брюшной полости и затем, при минимально возможном потоке и давлении инсуффлируемого газа, герметизировать полость клипированием или ушиванием дефекта брюшины. Если это не удается, то возможно либо перевести операцию в трансабдоминальный вариант, либо установить дополнительные ретракторы, которые возьмут на себя функцию поддержания объема ретроперитонеальной полости.
После создания первичной полости под визуальным контролем устанавливаются рабочие троакары. При выполнении адреналэктомии располагать порты предпочтительно в максимально верхней позиции, обычно по краю реберной дуги. Особенности проекционных точек для урологических операций будут рассмотрены ниже.
Общее число троакаров для левосторонней люмбоскопической адреналэктомии обычно включает:
— 10-мм троакар для лапароскопа, устанавливаемый по средней подмышечной линии;
— 11-мм троакар для инструментов правой руки оператора располагающийся в проекции задней подмышечной линии;
— 5 или 10-мм троакар для инструментов левой руки оператора, который целесообразно устанавливать по передней подмышечной линии;
— дополнительный инструментальный 5 мм троакар для ретрактора. вводимый максимально медиально.
При выполнении правосторонней адреналэктомии расположение троакаров диаметрально противоположное, однако, целесообразнее поменять местами 5-мм и 11-мм троакары, используемые оперирующим хирургом. В технически сложных случаях устанавливается дополнительный 5-мм троакар для введения аспиратора-ирригатора с целью выполнения манипуляций в условиях «сухого» оперативного поля.
В условиях внебрюшинного доступа, в связи с малым объемом ретропневмоперитонеума, очень сложно осуществлять визуальный контроль введения дополнительных троакаров, что может привести к неудобному расположению инструментов относительно друг друга и создавать неудобства для дальнейших манипуляций. В своей практике мы пришли к следующей схеме установки троакаров. Первый порт для лапароскопа вводится по средней подмышечной линии, и после создания ретроперитониального пространства с максимальной направленностью кпереди, под контролем зрения устанавливается второй 11-12 мм троакар по передней подмышечной линии ближе к реберной дуге. Затем лапароскоп перемещается из 1-го во 2-ой порт, что позволяет добиться лучшей визуализации зоны введения третьего и его оптимальное расположение относительно первого.
Следующим этапом является создание направленного ретропневмоперитонеума. Цель этого этапа — обеспечение визуализации зоны основного оперативного приема. Термин «направленный» подчеркивает ориентацию расширения полости. Рационально стремиться создать минимальную, но достаточную для выполнения манипуляций полость. Необходимо помнить, что объем ретропневмоперитонеума является одним из существенных факторов хирургической агрессивности люмбоскопических операций.
При выполнении адреналэктомии ориентиром направления продвижения тубуса лапароскопа являются XI, XII грудной, I поясничный позвонки Целесообразно избегать преждевременного нарушения целостности фасции Жерота. На начальном этапе создания направленного ретропневмо-перитонеума весь пласт забрюшинной клетчатки отводится в направлении передней брюшной стенки. При этом латеральная стенка полости представлена мышцами боковой стенки туловища, а дно или наиболее удаленная стенка — диафрагмой.
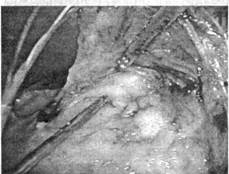
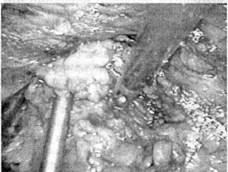

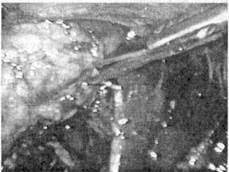
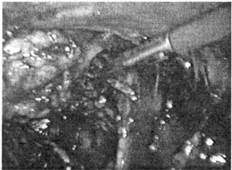
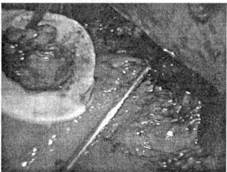
Рис. 107. Лапароскопическая адренааэктомия справа
Основные манипуляции при выполнении оперативного приема включают механическую диссекцию, резание, электродиссекцию, коагуляцию и клипирование. Для лучшей диссекции железы и паранефральной клетчатки Takeda с соавт. (1994) использовали ультразвуковой аспиратор, особенно у пациентов с гиперкортизолизмом. Они также рекомендуют аргоновый коагулятор в случае, если надпочечник окружен тканью печени. С использованием аргонового коагулятора осуществляется частичная резекция печени.
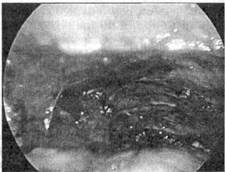

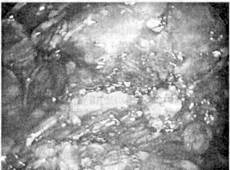
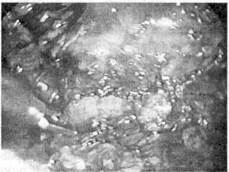
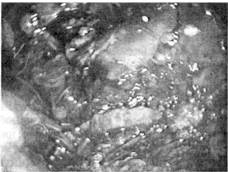
Рис.108. Люмбоскопическая адреналэктомия слева
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 1759; Нарушение авторских прав?; Мы поможем в написании вашей работы!