
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Частные случаи первого закона термодинамики для изопроцессов
|
|
|
|
Первый закон термодинамики
Первый закон термодинамики (закон сохранения энергии для тепловых процессов) определяет количественное соотношение между изменением внутренней энергии системы дельта U, количеством теплоты Q, подведенным к ней, и суммарной работой внешних сил A, действующих на систему.
Первый закон термодинамики - Изменение внутренней энергии системы при ее переходе из одного состояния в другое равно сумме количества теплоты, подведенного к системе извне, и работы внешних сил, действующих на нее:
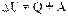
Первый закон термодинамики - количество теплоты, подведенное к системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами:

При изохорном процессе объем газа остается постоянным, поэтому газ не совершает работу. Изменение внутренней энергии газа происходит благодаря теплообмену с окружающими телами:
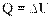
При изотермическом процессе количество теплоты, переданное газу от нагревателя, полностью расходуется на совершение работы:
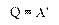
При изобарном расширении газа подведенное к нему количество теплоты расходуется как на увеличение его внутренней энергии и на совершение работы газом:
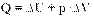
Адиабатный процесс - термодинамический процесс в теплоизолированной системе.
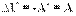
Теплоизолированная система - система, не обменивающаяся энергией с окружающими телами.
Формула КПД теплового двигателя:

Здесь Q1 - количество теплоты, полученное рабочим телом,
Q2 - количество теплоты, отданное холодильнику.
A - полезная работа.
Формула Карно для оценки максимального КПД теплового двигателя:
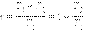
T1 - температура нагревателя, T2 - температура холодильника.
Вопрос 5
Калорические параметры состояния
К калорическим параметрам состояния относятся, как уже отмечалось, внутренняя энергия, энтальпия и энтропия. Своим названием эти параметры обязаны тому, что ранее измерялись в калориях.
Внутренняя энергия. Любая термодинамическая система в каждом состоянии обладает запасом полной энергии, которая состоит из внутренней энергии, зависящей от внутреннего состояния тела, и внешней энергии, связанной с движением тела как целого и положением его в каком-либо внешнем поле сил (например в поле сил тяжести), т. е
Если тело не движется, а влиянием внешнего поля сил можно пренебречь, то полная энергия будет представлять собой только внутреннюю энергию.
Любая термодинамическая система (рабочее тело) обладает запасом внутренней энергии, которая состоит из энергии хаотического (теплового) движения и взаимодействия молекул. Поскольку внутренняя энергия рабочего тела зависит от его массы, обычно интересуются значением внутренней энергии, отнесенной к 1 кг массы тела, — удельной внутренней энергией
В общем случае удельная кинетическая энергия теплового движения состоит из удельной кинетической энергии поступательного, вращательного и колебательного движений молекул, зависящей только от температуры рабочего тела, и удельной потенциальной энергии взаимодействия молекул между собой, которая, в свою очередь, зависит от среднего расстояния между молекулами, т. е. от занимаемого рабочим телом объёма. Следовательно, в общем случае удельная внутренняя энергия рабочего тела зависит от его температуры и удельного объема, являясь однозначной функцией этих параметров состояния:, или
Таким образом, важнейшим свойством удельной внутренней энергии рабочего тела является то, что она представляет собой однозначную функцию состояния тела, определяемого любой парой его основных параметров (,,), и сама может служить параметром состояния. Из этого свойства следует, что изменение удельной внутренней энергии не зависит от характера процесса, а определяется лишь начальным и конечным состояниями рабочего тела. Следовательно, бесконечно малое приращение удельной внутренней энергии является полным дифференциалом.
В идеальном газе силы взаимодействия между молекулами отсутствуют и удельная потенциальная энергия его равна нулю. Поэтому удельная внутренняя энергия идеального газа состоит только из удельной кинетической энергии движения молекул и определяется его температурой:, или
В замкнутом (круговом) процессе, в котором начальное и конечное состояния совпадают, изменение удельной внутренней энергии равно нулю.
Определять абсолютное значение удельной внутренней энергии в большинстве технических расчетов не требуется, так как обычно необходимо знать только ее изменение. Поэтому условно приписывают некоторому состоянию рабочего тела нулевое значение удельной внутренней энергии, а все расчеты ведут относительно этого значения.
Энтальпия. Рассмотрим полную энергию газа, находящегося под давлением, создаваемым грузом массой (рис. 1.1). В этом случае полная энергия системы состоит из внутренней энергии газа и потенциальной энергии груза, равной, где - площадь поперечного сечения поршня. Т. е.. Величина, зависящая от сил, действующих на поршень, получила название потенциальной энергии давления.
Таким образом, если газ находится в среде с давлением, то с любым состоянием его связана некоторая энергия, получившая название энтальпии газа в данном состоянии. Выражение энтальпии для 1 кг газа (т. е. удельной энтальпии) имеет вид
Следовательно, удельная энтальпия, будучи зависимой от параметров состояния, и, также является параметром состояния. Поэтому изменение, как и изменение, не зависит от характера процесса, а определяется только начальным и конечным состояниями, т. е.
Как однозначная функция состояния удельная энтальпия может быть представлена в виде функции любой пары основных параметров состояния.
Удельная энтальпия идеального газа, как и его удельная внутренняя энергия, является функцией только температуры. Действительно:
Удельная энтальпия, как и удельная внутренняя энергия, выражается в джоулях на килограмм (Дж/кг).
Энтропия. Кроме рассмотренных параметров, в термодинамике широко используется еще один калорический параметр состояния — энтропия, введенный Клаузиусом в 1865 г. при анализе круговых процессов.
Энтропия — параметр состояния, дифференциал которого равен отношению бесконечно малого количества теплоты в элементарном обратимом процессе к абсолютной температуре, постоянной на бесконечно малом участке процесса, т. е.
Если количество теплоты отнести к 1 кг вещества (), то получим удельную энтропию
которая выражается в джоулях на килограмм-кельвин [Дж/(кг • К)].
Вопрос 6
Процесс изменения характеристических функций под воздействием термодинамических параметров называют термодинамическим процессом.
Используется несколько типов классификации термодинамических процессов:
по мониторингу за изменением параметров термодинамические процессы подразделяются на:
1) изотермический (Т = const.);
2) изобарический (Р = const.);
3) изохорический (V = const.);
4) адиабатный (А = const.);
5) неравновесный (ΔР ≠ ΔТ ≠ ΔV ≠ 0);
6) равновесный (ΔР = ΔТ = ΔV = 0)
по направлению термодинамического процесса
1) обратимый процесс (допускающий возможность возвращения системы в исходное состояние без того, чтобы в окружающей среде остались какие-либо изменения.);
2) необратимый процесс (идет только в одном направлении).
по характеру взаимодействия с окружающей средой:
1) самопроизвольный процесс (совершается под воздействием внутренней энергии системы);
2) вынужденный процесс (совершается под воздействием энергии окружающей среды).
Вопрос 7
Первое начало термодинамики по балансу рабочего тела:  , где
, где  - полный или приведённый теплообмен. Полное количество теплоты
- полный или приведённый теплообмен. Полное количество теплоты  , полученное телом, равно сумме теплоты, подведенной извне
, полученное телом, равно сумме теплоты, подведенной извне  , и теплоты внутреннего теплообмена
, и теплоты внутреннего теплообмена 
Первое начало термодинамики по балансу рабочего тела справедливо для любых процессов протекающих в системе.
В условиях обратимого процесса, то есть 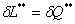 , первое начало термодинамики по балансу рабочего тела переходит в первое начало термодинамики по внешнему балансу. Для использования этого уравнения нужно уметь его интегрировать. При интегрировании получится:
, первое начало термодинамики по балансу рабочего тела переходит в первое начало термодинамики по внешнему балансу. Для использования этого уравнения нужно уметь его интегрировать. При интегрировании получится:  для необратимых процессов и
для необратимых процессов и  для обратимых процессов.
для обратимых процессов.
Уравнения баланса тепловых потоков имеют следующий вид:
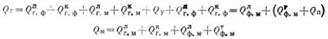
где Qr — общее количество тепла, отдаваемое потоком газов, кВт; Qr ф— количество тепла, отдаваемое потоком газов лучеиспусканием открытой поверхности футеровки, кВт; ^ — то же конвекцией, кВт; Q% м— количество тепла, отдаваемое потоком газов лучеиспусканием открытой поверхности материала, кВт;
м~" т0 же конвекцией» кВт; Qy — количество тепла, отдаваемое потоком газов и твердыми частицами, выделяющимися из материала, кВт; м — количество тепла, отдаваемое лучеиспусканием открытой поверхностью футеровки открытой поверхности материала, кВт; (?Jj, м — количество тепла, отдаваемое закрытой материалом поверхности футеровки закрытой поверхности материала, кВт; <?п ~ количество тепла, отдаваемое поверхностью печи окружающей среде, кВт; QM — общее количество тепла, получаемое материалом, кВт.
Составляющие уравнений балансов определяют по следующим формулам:
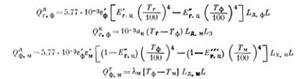
где Тг — средняя по длине печи абсолютная температура газа, К; Тф — средняя по длине печи температура, К; £д< ф— длина дуги футеровки, м; LA м — длина дуги материала, м; L3 — длина зоны лучистого нагревания печи, м; Lx м — длина хорды материала, м; Тм — средняя по длине печи температура материала, К.
Учитывая, что температура поверхности материала всегда будет выше его средней, фактическое количество тепла, передаваемого материалу, будет меньше рассчитанного по описанным выше формулам.
В этом случае необходимо вводить в правую часть уравнений поправочный коэффициент К (меньше единицы), характеризующий степень равномерности температуры материала.
Количество тепла, передаваемое потоком газов непосредственно открытой поверхности материала, определяется по формулам, аналогичным указанным выше, в которые вместо температуры и коэффициента излучения поверхности футеровки представляются аналогичные их значения для материала. Суммируя количество тепла, передаваемое материалу потоком газов непосредственно и через футеровку по всей длине печи, получим общее количество, которое должно соответствовать заданному тепловым балансом.
Приведенная методика теплового расчета печи содержит ряд условностей и упрощений. Например, температуры материала, потока газов и футеровки принимаются постоянными на всем протяжении печи и равными полусумме начальных и конечных температур; потери тепла в окружающую среду определяются на основании средних опытных данных в процентном отношении к общему его расходу, при определении количества тепла, передаваемого материалу футеровкой, не учитывается влияние на интенсивность теплопередачи вращения печи ч периодичность изменения температуры футеровки. Однако, как показали сравнительные подсчеты и сопоставления их с фактическими данными, полученные результаты не дают резких отклонений, выходящих за пределы обычно допускаемых при практическом их применении.
Диаметр муфеля рассчитывают по производительности печи и коэффициенту его заполнения материалом, пользуясь следующей формулой:
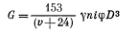
где G — производительность муфеля, кг/ч; у — насыпная масса материала, кг/м3; и — угол естественного откоса материала, градусы; i — наклон печи, % к длине; п — число оборотов печи, об/мин; ср — коэффициент заполнения муфеля:
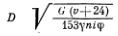
Задаваясь произведением числа оборотов лечи на ее наклон, при известной производительности и принятом коэффициенте заполнения, по указанной выше формуле определяют диаметр муфеля.
Для определения суммарной площади поперечного сечения каналов, по которым движется поток газов, необходимо задаться скоростью движения в них газов (обычно она равна 6—8 м/с). Зная общее сечение этих каналов, толщину их стенок и стенок муфеля, легко найти наружный диаметр печи.
Остальные размеры определяются методом, аналогичным для пламенных печей.
ВОПРОС 8
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 3336; Нарушение авторских прав?; Мы поможем в написании вашей работы!