
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методические находки
|
|
|
|
Пишем ионное уравнение гидролиза, определяем среду
Алгоритм написания уравнений гидролиза.
Когда школьники поняли суть реакции гидролиза, даем (а лучше составляем вместе с ними) алгоритм написания уравнений гидролиза. Рассмотрим его на конкретных примерах.
1. Определяем тип гидролиза. На этом этапе школьники могут написать уравнение диссоциации соли. Можно дать им “правило цепочки”: цепочка рвется по слабому звену, гидролиз идет по иону слабого электролита.
Пример 1. Гидролиз сульфата меди(II): CuSO4 = Cu 2+ + SO42–
Соль образована катионом слабого основания (подчеркиваем) и анионом сильной кислоты. Гидролиз по катиону.
Cu2+ + H-OH «CuOH+ + H+;
образуется катион гидроксомеди(II) и ион водорода, среда кислая
3. Составляем молекулярное уравнение. Надо учитывать, что составление такого уравнения есть некоторая формальная задача. Из положительных и отрицательных частиц находящихся в растворе, мы составляем нейтральные частицы, существующие только на бумаге. В данном случае мы можем составить формулу (CuOH)2SO4, но для этого наше ионное уравнение мы должны мысленно умножить на два. Получаем:
2CuSO4 + 2H2O «(CuOH)2SO4 + H2SO4
Обращаем внимание, что продукт реакции относится к группе основных солей. Названия основных солей, как и названия средних, следует составлять из названия аниона и названия катиона, в данном случае соль назовем сульфат гидроксомеди(II). (Приставка “ди” не нужна, не говорим же мы “сульфат динатрия”). Называть эту соль “гидроксосульфат меди”, на наш взгляд, значит нарушать всю логику номенклатуры солей. Разве есть в растворе, или в узлах кристаллической решетки частица “гидроксосульфат”? Нет! А катион гидроксомеди есть. В дальнейшем этот подход распространяется на номенклатуру комплексных солей.
В школьной программе появилось новое понятие. Это pH - водородный показатель кислотности среды. Ну и правильно, ведь про этот загадочный " пэ аш " то и дело вещает телевизор - то в рекламе зубной пасты, то в сообщениях о самой лучшей косметике, то в экологических новостях ("кислотные дожди"). Важнейшее понятие химии, количественно описывающее кислотность или щелочность растворов...
Конечно, школьники должны знать, что это такое. Вот только незадача: для определения рН требуется знание логарифмов. А в программе по математике эта тема отнесена обычно на второе полугодие 11-го класса.
Ну как тут быть учителю химии???
Возможный выход указывает глава из учебника химии Савинкиной и Логиновой, который скоро выйдет в свет в издательстве АСТ-ПРЕСС. Эта глава так и называется:
Водородный показатель (рН)
В воде всегда присутствует немного катионов водорода и гидроксид-ионов, которые образуются в результате обратимой диссоциации:
H2O  H+ + OH-
H+ + OH-
В 1 л чистой воды при комнатной температуре содержится 1 . 10-7 моль катионов водорода и 1 . 10-7 моль гидроксид-ионов.
Поскольку оперировать числами такого порядка неудобно, для количественной характеристики кислотности среды используют так называемый водородный показатель рН ("пэ аш", от латинского "pundus hydrogenium" - "вес водорода"). Каждое значение рН отвечает определенному содержанию катионов водорода в 1 л раствора.
В чистой воде и в нейтральных растворах, где в 1 л содержится 1 . 10-7 моль катионов водорода, значение рН равно 7.
В растворах кислот содержание катионов водорода увеличивается, а содержание гидроксид-ионов уменьшается, в растворах щелочей наблюдается обратная картина. В соответствии с этим меняется и значение водородного показателя (рН).
Кислоты, попадая в воду, диссоциируют, и содержание катионов водорода в расчете на 1 л раствора становится больше 1 . 10-7 моль.
Сильные кислоты в водной среде диссоциируют необратимо. Например, хлороводородная кислота полностью превращается в катионы водорода H+ и хлоридные анионы Cl-:
HCl = H+ + Cl-
Если в 1 л водного раствора содержится 1 . 10-2 моль HCl, то катионов водорода H+ в этом объеме тоже 1 . 10-2 моль. Значение водородного показателя (рН) для этого раствора оказывается равным 2. Когда в том же объеме раствора содержится 1 . 10-3 моль HCl, то катионов H+ становится уже 1 . 10-3 моль (рН = 3), если хлороводородной кислоты 1 . 10-4 моль, то содержание H+ - 1 . 10-4 моль (рН = 4), и т.д.
Диссоциация слабых кислот, например угольной, протекает обратимо:
H2CO3  H+ + HCO3-
H+ + HCO3-
Далеко не все присутствующие в растворе молекулы H2CO3 превращаются в катионы H+ и анионы HCO3-. Тем не менее катионов H+ в растворах таких кислот больше, чем в чистой воде (например, 1 . 10-5 или 1 . 10-6 моль в каждом литре раствора).
Таким образом, в растворах кислот катионов водорода в 1 л раствора содержится всегда больше, чем 1 . 10-7, а рН оказывается меньше 7. Водородный показатель рН, меньший 7, отвечает кислотной среде раствора.
Если рН находится в интервале 5-7, то среда раствора считается слабокислотной, если рН меньше 5, то сильнокислотной: чем сильнее кислота, тем ниже значение рН.
В результате диссоциации оснований в водном растворе появляются гидроксид-ионы, которые связывают катионы водорода, присутствующие в чистой воде, и уменьшают их количество в щелочном растворе:
NaOH = Na+ + OH-
H+ + OH- = H2O
Растворение в 1 л воды 1 . 10-2 моль сильного основания - гидроксида натрия NaOH - приводит к появлению 1 . 10-2 моль гидроксид-ионов. Содержание катионов водорода в полученном растворе оказывается равным 1 . 10-12 моль, а рН принимает значение 12.
Если в 1 л воды растворить 1 . 10-3 моль NaOH, то гидроксид-ионов получится 1 . 10-3 моль (1 . 10-11 моль катионов H+, рН = 11).
Растворение в том же объеме 1 . 10-4 моль NaOH даст 1 . 10-4 моль OH- (1 . 10-10 моль катионов H+, рН = 10), и т.д.
Таким образом, в растворах оснований содержание катионов водорода всегда меньше 1 . 10-7 моль в 1 л, а водородный показатель (рН) - больше 7. Среда в таких растворах щелочная.
Для растворов сильных оснований, диссоциация которых идет необратимо, значение рН будет существенно выше 7. Диссоциация слабых оснований, например, гидрата аммиака, протекает лишь частично, гидроксид-ионов в этом случае образуется меньше, и рН не столь заметно превышает значение, характерное для нейтральной среды. Раствор считается слабощелочным при рН от 7 до 9 и сильнощелочным при рН выше 9.
Значения водородного показателя (рН) водных растворов распространенных веществ обычно находятся в интервале от 1 до 13. Приближенно оценить рН растворов можно с помощью кислотно-основных индикаторов. Для более точного измерения водородного показателя используют приборы - рН-метры.
42. Окисли́тельно-восстанови́тельные реа́кции, ОВР, редокс (от англ. redox ← reduction-oxidation — окисление-восстановление) — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем. Описание [править]
В процессе окислительно-восстановительной реакции восстановитель отдаёт электроны, то есть окисляется; окислитель присоединяет электроны, то есть восстанавливается. Причём любая окислительно-восстановительная реакция представляет собой единство двух противоположных превращений — окисления и восстановления, происходящих одновременно и без отрыва одного от другого.
Окисление [править]
Окисление — процесс отдачи электронов, с увеличением степени окисления.
При окисле́нии вещества в результате отдачи электронов увеличивается его степень окисления. Атомы окисляемого вещества называются донорами электронов, а атомы окислителя —акцепторами электронов.
В некоторых случаях при окислении молекула исходного вещества может стать нестабильной и распасться на более стабильные и более мелкие составные части (см. Свободные радикалы). При этом некоторые из атомов получившихся молекул имеют более высокую степень окисления, чем те же атомы в исходной молекуле.
Окислитель, принимая электроны, приобретает восстановительные свойства, превращаясь в сопряжённый восстановитель:
окислитель + e− ↔ сопряжённый восстановитель.
Восстановление [править]
Восстановле́нием называется процесс присоединения электронов атомом вещества, при этом его степень окисления понижается.
При восстановлении атомы или ионы присоединяют электроны. При этом происходит понижение степени окисления элемента. Примеры: восстановление оксидов металлов до свободных металлов при помощи водорода, углерода, других веществ; восстановление органических кислот в альдегиды и спирты; гидрогенизация жиров и др.
Восстановитель, отдавая электроны, приобретает окислительные свойства, превращаясь в сопряжённый окислитель:
восстановитель — e− ↔ сопряжённый окислитель.
Несвязанный, свободный электрон является сильнейшим восстановителем.
43. Зако́н де́йствующих масс устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии, а также зависимость скорости химической реакции от концентрации исходных веществ.
Закон действующих масс в химической кинетике [править]
Закон действующих масс в кинетической форме (основное уравнение кинетики) гласит, что скорость элементарной химической реакции пропорциональна произведению концентраций реагентов в степенях, равных стехиометрическим коэффициентам в уравнении реакции[1]. Это положение сформулировано в 1867 году норвежскими учёными К. Гульдбергом и П. Вааге. Для элементарной химической реакции:
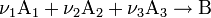
закон действующих масс может быть записан в виде кинетического уравнения вида:
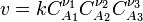
где  — скорость химической реакции,
— скорость химической реакции,  — константа скорости реакции.
— константа скорости реакции.
Для сложных реакций в общем виде это соотношение не выполняется. Тем не менее, многие сложные реакции условно можно рассматривать как ряд последовательных элементарных стадий с неустойчивыми промежуточными продуктами, формально эквивалентный переходу из начального состояния в конечное в «один шаг». Такие реакции называют формально простыми [2]. Для формально простых реакций кинетическое уравнение может быть получено в виде:

(для трех исходных веществ, аналогично приведённому выше уравнению). Здесь 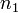 ,
, 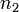 ,
,  — порядок реакции по веществам
— порядок реакции по веществам 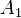 ,
,  ,
, 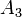 соответственно, а сумма
соответственно, а сумма 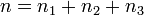 — общий (или суммарный) порядок реакции.
— общий (или суммарный) порядок реакции. 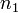 ,
, 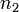 ,
,  могут быть не равны стехиометрическим коэффициентам и не обязательно целочисленные.
могут быть не равны стехиометрическим коэффициентам и не обязательно целочисленные.  при определённых условиях может быть равно и нулю.
при определённых условиях может быть равно и нулю.
Закон действующих масс в химической термодинамике [править]
В химической термодинамике закон действующих масс связывает между собой равновесные активности исходных веществ и продуктов реакции, согласно соотношению:
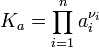
где
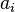 — активность веществ. Вместо активности могут быть использованы концентрация (для реакции в идеальном растворе), парциальные давления (реакция в смеси идеальных газов), фугитивность (реакция в смеси реальных газов);
— активность веществ. Вместо активности могут быть использованы концентрация (для реакции в идеальном растворе), парциальные давления (реакция в смеси идеальных газов), фугитивность (реакция в смеси реальных газов);
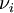 — стехиометрический коэффициент (для исходных веществ принимается отрицательным, для продуктов — положительным);
— стехиометрический коэффициент (для исходных веществ принимается отрицательным, для продуктов — положительным);
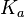 — константа химического равновесия. Индекс «a» здесь означает использование величины активности в формуле.
— константа химического равновесия. Индекс «a» здесь означает использование величины активности в формуле.
На практике в расчётах, не требующих особой точности, значения активности обычно заменяются на соответствующие значения концентраций (для реакций в растворах) либо парциальных давлений (для реакций между газами). Константу равновесия при этом обозначают  или
или 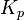 соответственно. Впервые закон действующих масс был выведен из кинетических представлений Гульдбергом и Вааге, а термодинамический вывод его дан Вант-Гоффом в 1885 году[3].
соответственно. Впервые закон действующих масс был выведен из кинетических представлений Гульдбергом и Вааге, а термодинамический вывод его дан Вант-Гоффом в 1885 году[3].
Пример: для стандартной реакции
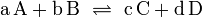
константа химического равновесия определяется по формуле
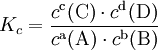
44. Буферные растворы (англ. buffer, от buff — смягчать удар) — растворы с определённой устойчивой концентрацией водородных ионов; смесь слабой кислоты и её соли (напр., СН3СООН и CH3COONa) или слабого основания и его соли (напр., NH3 и NH4CI). Величина рН буферного раствора мало изменяется при добавлении небольших количеств свободной сильной кислоты или щёлочи, при разбавлении или концентрировании. Буферные растворы широко используют в различных химических исследованиях.
Буферные растворы имеют большое значение для протекания процессов в живых организмах. Например, в крови постоянство водородного показателя рН поддерживается буферными смесями, состоящими из карбонатов и фосфатов. Известно большое число буферных растворов (ацетатно-аммиачный буферный раствор, фосфатный буферный раствор, боратный буферный раствор, формиатный буферный раствор и др.).
Значение pH буферного раствора можно рассчитать по формуле: 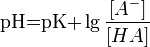 , где
, где 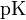 это отрицательный десятичный логарифм от константы диссоциации кислоты
это отрицательный десятичный логарифм от константы диссоциации кислоты  .
.
По сути  .
.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 346; Нарушение авторских прав?; Мы поможем в написании вашей работы!