
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрофизиология сердца
|
|
|
|
Первые исследования клеточных электрофизиологических проявлений интоксикации сердечными гликозидами были проведены Woodbury и соавт. [5, 6] в начале 50-х годов. Они обнаружили, что под влиянием гликозидов процесс реполяризации сначала замедляется, а затем ускоряется и амплитуда потенциала действия снижается без изменения потенциала покоя (рис. 6.2). В течение следующего десятилетия проводились многочисленные исследования, посвященные действию сердечных гликозидов на различные участки проводящей системы сердца. При воздействии токсических концентраций сердечных гликозидов было отмечено снижение диастолического трансмембранного потенциала в клетках АВ-узла, волокнах Пуркинье, а также в миокардиальных клетках предсердий и желудочков. Это сопровождалось уменьшением амплитуды потенциала действия и скорости его нарастания (Vmax), а также ускорением процесса реполяризации во всех исследованных типах клеток. Однако, по-видимому, наиболее существенным эффектом токсических доз сердечных гликозидов является развитие или ускорение спонтанной деполяризации в фазу 4 потенциала действия (рис. 6.3). Этот эффект легко возникает в клетках АВ-узла и волокон Пуркинье, но не в клетках рабочего миокарда. Последнее указывает на «иерархическое» действие сердечных гликозидов, так как проводящая система более чувствительна к этим соединениям, чем рабочий миокард. Наконец, при продолжительном действии токсических доз сердечных гликозидов развивается полная электрическая невозбудимость миокарда [7—10].
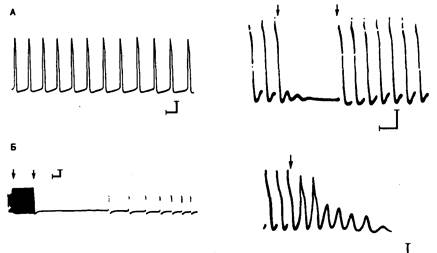
Рис. 6.3. Сравнение автоматической активности и задержанной постдеполяризации в волокнах Пуркинье у собаки.
А — автоматически активное волокно с деполяризацией в фазу 4 (слева) и активность в волокне, подвергнутом действию токсической концентрации препарата наперстянки (справа). После остановки стимуляции (первая стрелка) наблюдаются колебания мембранного потенциала. После возобновления стимуляции (вторая стрелка) потребовалось несколько возбуждений для восстановления полной амплитуды задержанных постдеполяризаций. Б — влияние стимуляции с высокой частотой на автоматический ритм. Слева: отмечено начало (первая стрелка) и окончание (вторая стрелка) высокочастотной стимуляции; при высокой частоте стимуляции возникает гиперполяризация; затем, после продолжительной паузы наблюдается автоматическая активность. Справа: остановка стимуляции после нанесения трех стимулов; затем два потенциала действия возникают вследствие того, что задержанная постдеполяризация достигает порогового уровня потенциала. Впоследствии наблюдалась подпороговая постдеполяризация, которая через некоторое время также прекратилась.
Считается, что внутриклеточные механизмы действия токсических доз сердечных гликозидов связаны с аккумуляцией калия во внеклеточном пространстве при одновременном повышении внутриклеточной концентрации ионов натрия [11] вследствие ингибирования Na—K АТФазы (см. выше). Более того, уменьшение внутриклеточной концентрации калия и повышение его внеклеточной концентрации имеют непосредственное отношение к потере трансмембранной разности потенциалов, которая еще больше усиливается из-за частичного угнетения тока электрогенного Na—К-насоса, вносящего определенный вклад в мембранный потенциал. При повышении внеклеточной концентрации калия увеличивается калиевая проницаемость мембраны, что вызывает ускорение реполяризации и угнетение фазы плато потенциала действия (фаза 2). Уменьшение скорости нарастания и амплитуды потенциала действия, а также потеря мембранного потенциала покоя могут непосредственно вы зывать замедление и блокаду проведения. Поскольку сердечные гликозиды, кроме того, обладают способностью усиливать высвобождение ацетилхолина (см. ниже), они сильнее угнетают проведение в тканях, более чувствительных к парасимпатическому влиянию (например, синусовый узел, АВ-узел и миокард предсердий). Тахиаритмия, вызванная избытком сердечных гликозидов, в большинстве случаев связана с увеличением наклона деполяризации в фазу 4 (см. рис. 6.3 и табл. 6.1) [8—10]. Подобное усиление деполяризации в фазу 4 до некоторой степени может быть обусловлено возрастанием симпатического влияния на сердце вследствие действия гликозидов на центральную нервную систему (см. ниже).
Таблица 6.1. Сравнительные характеристики ритмической желудочковой активности, вызванной сердечными гликозидами у интактных животных, и задержанной постдеполяризации в препаратах миокарда
| Ритмическая желудочковая активность | Задержанная постдеполяризация |
| Запускается преждевременным возбуждением в момент появления зубца Т (после уязвимого периода) или в начале диастолы | Легче всего запускается стимуляцией с высокой частотой или преждевременным стимулом с коротким интервалом сцепления |
| При повышении интоксикации уменьшается сила тока, необходимого для индукции ритмической активности желудочков | При повышении интоксикации уменьшается сила тока, необходимого для достижения задержанной постдеполяризацией порогового потенциала |
| При повышении интоксикации увеличивается вероятность появления более длинных цепочек ритмической активности желудочков | При повышении интоксикации цепочки триггерной активности, вызванной задержанной постдеполяризацией, становятся длиннее |
За последние десять лет накоплено большое количество данных о том, что сердечные гликозиды влияют не только на деполяризацию в фазу 4, они способны также вызывать осцилляторную активность, т. е. задержанную постдеполяризацию или осцилляторные следовые потенциалы (рис. 6.4; см. также рис. 6.3 и табл 6.1) [10, 12, 13]. Такая задержанная постдеполяризация, по-видимому, является следствием цепочки событий, которая начинается с ингибирования системы Na—К АТФазы. В результате происходит повышение внутриклеточной концентрации кальция по механизму Na—Са-обмена, которое, скорее всего, и запускает транзиторный входящий ток, переносимый преимущественно ионами натрия по каналам, не чувствительным к тетродотоксину (т. е. эти "каналы отличаются от быстрых натриевых каналов) [14]. Этот транзиторный ток, вероятно, является основным фактором, приводящим к развитию задержанной постдеполяризации. У человека такая задержанная постдеполяризация может играть особую роль и в развитии нарушений ритма, не связанных с интоксикацией сердечными гликозидами. Однако результаты детальных электрофизиологических исследований на миокардиальных препаратах свидетельствуют, что задержанная постдеполяризация является наиболее вероятным механизмом возникновения тахиаритмий при интоксикации сердечными гликозидами (см. табл. 6.1).
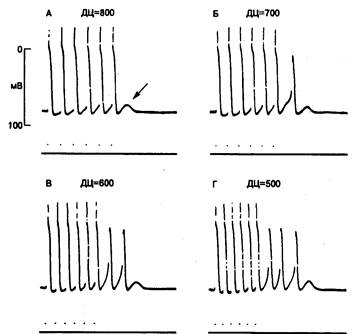
Рис. 6.4. Влияние частоты сердечных сокращений на амплитуду задержанной постдеполяризации и триггерный автоматизм волокон Пуркинье у собаки при действии токсической концентрации сердечных гликозидов (А-Г).
В нижней части, каждого фрагмента — серия из 6 стимулов. Обратите внимание; при уменьшении длительности цикла (ДЦ) подпороговая постдеполяризация количественно возрастает, в результате чего увеличивается число триггерных потенциалов действия [31].
Изменение внеклеточной концентрации калия, несомненно, влияет на электрофизиологические проявления интоксикации сердечными гликозидами. При низком внеклеточном уровне калия повышается вероятность связывания гликозидов с рецепторами. Кроме того, снижение внеклеточной концентрации калия как таковое (безотносительно к действию сердечных гликозидов) ускоряет развитие спонтанной деполяризации в фазу и усиливает автоматизм. И наоборот, при повышении внеклеточной концентрации калия связывание сердечных гликозидов с Na—K АТФазой уменьшается. Однако при уровнях, превышающих верхнюю границу нормы, увеличение внеклеточного содержания калия ускоряет реполяризацию и уменьшает трансмембранную разность потенциалов в покое, а также амплитуду и скорость нарастания потенциала действия. В конце концов это может послужить причиной значительного замедления проведения [10]. Любое отклонение внеклеточной концентрации калия, выходящее за пределы нормального диапазона, в сочетании с избытком сердечных гликозидов может вызвать и усилить нарушения проведения и ускорить развитие эктопической активности в предсердиях и желудочках.
Другим ионом, изменяющим реакцию миокарда на сердечные гликозиды, является кальций. Повышение внеклеточного уровня кальция приводит к смещению порогового потенциала в сторону более положительных потенциалов и, что более важно, способно увеличить транзиторный входящий ток, вызывающий задержанную постдеполяризацию. И наоборот, уменьшение внеклеточного содержания кальция приближает пороговый потенциал к уровню потенциала покоя, повышая тем самым возбудимость миокарда [10].
Таким образом, повышение внеклеточных концентраций ионов калия и кальция может иметь неблагоприятные последствия в условиях интоксикации сердечными гликозидами; поэтому при интоксикации следует предпринять необходимые условия для поддержания нормального уровня как этих ионов, так и ионов магния.
Возраст, по-видимому, тоже влияет на электрофизиологические эффекты сердечных гликозидов. Экспериментально было показано, что в сердце новорожденных необходимы более высокие концентрации сердечных гликозидов для проявления эффектов, типичных для интоксикации. И наоборот, в миокардиальных препаратах, полученных у более старых животных, токсические эффекты сердечных гликозидов вызываются намного легче [15]. И наконец, наибольшей чувствительностью к сердечным гликозидам обладают пораженные ткани сердца, где интоксикация развивается особенно быстро [16].
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 569; Нарушение авторских прав?; Мы поможем в написании вашей работы!