
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Язвенная болезнь
|
|
|
|
Язвенная болезнь (ЯБ) — широко распространённое заболевание, ей страдает приблизительно 10% населения земного шара. Частота язвенной болезни двенадцатиперстной кишки в 4–13 раз больше, чем язвенной болезни желудка, причём мужчины болеют в 2–7 раз чаще женщин.
В последние годы происходит уменьшение заболеваемости ЯБ в развитых странах, а с 50-х годов ХХ в. — постепенное снижение смертности. Это связано с применением новых фармакологических препаратов, снижением числа курящих, уменьшением инфицированности населения развитых стран H. pylori. Исследователи объясняют динамику смертности «феноменом когорты»: люди, родившиеся в последней четверти ХIХ в., имели максимальный риск смерти от ЯБ к середине ХХ в.; смертность от ЯБ стала ниже, когда состарилась когорта высокого риска. Данный феномен связывают с ранней фазой урбанизации, а также с особенно тяжёлыми стрессовыми ситуациями, пережитыми этим поколением.
Язвенная болезнь — хроническое, циклически текущее заболевание. Его основное морфологическое выражение — хроническая рецидивирующая язва желудка или двенадцатиперстной кишки.
Помимо язвы как проявления язвенной болезни желудка и двенадцатиперстной кишки существуют так называемые симптоматические язвы, т.е. изъязвления желудка и двенадцатиперстной кишки при других заболеваниях. Таковы язвы при эндокринных заболеваниях (синдром Золлингера-Эллисона, гиперпаратиреоз), при острых и хронических нарушениях кровообращения (дисциркуляторно-гипоксические язвы), при экзо- и эндогенных интоксикациях (токсические язвы), аллергии (аллергические язвы), хронических инфекциях (туберкулёзные, сифилитические язвы), после операций на желудке и кишечнике (послеоперационные пептические язвы), в результате медикаментозного лечения (стероидные язвы), а также при критических ситуациях (стрессовые язвы) или некоторых заболеваниях внутренних органов (гепатогенные язвыпри циррозе печени).
Язвенная болезнь — чисто человеческое страдание, в её развитии основную роль играют стрессовые ситуации, что объясняет высокую заболеваемость язвенной болезнью во всех странах мира.
Факторы риска. ЯБ широко распространена. Её диагностируют, в основном, у лиц молодого и среднего возраста, чаще у мужчин, нередко как семейное заболевание с генетически наследуемой большой массой париетальных клеток. Нередко у больных обнаруживают группу крови I, дефицит α1-антитрипсина, отсутствие антигенов гистосовместимости, отвечающих за выработку гликопротеинов желудочной слизи (статус несекреторов).
Этиология. Со времен начала изучения проблемы ЯБ существовало множество гипотез. Впервые ЯБ была описана Ж. Крювелье, сторонником воспалительной теории болезни. К старым теориям относят сосудистую, пептическую, механическую, кортиковисцеральную, теорию обратной диффузии водородных ионов и другие, имеющие сегодня лишь исторический интерес. Ни одна из этих теорий не может полностью объяснить развитие ЯБ, все они — составные части общей схемы патогенеза.
Открытие H. pylori заставило пересмотреть взгляды на теорию язвенной болезни. Оказалось, что при язвенной болезни двенадцатиперстной кишки H. pylori обнаруживают у всех больных, а при язвенной болезни желудка — в 75–85%. Кроме того, независимо от локализации пептической язвы всегда присутствует хронический гастрит. Выяснение этиологической роли H. pylori заставило на качественно новом уровне вернуться к «гастритической» концепции возникновения ЯБ. Воспалительные и дисрегенераторные изменения слизистой оболочки, составляющие сущность хронического гастрита, снижают резистентность слизистой к воздействию факторов пептической агрессии и способствуют образованию язвы. Наличие антрального гастрита десятикратно увеличивает риск развития ЯБ. При выраженном атрофическом гастрите риск образования язвы выше в 20–30 раз.
Геном H. pylori содержит 1600 генов, 10% из них жизненно необходимы бактерии. Продукты генов, кодирующих синтез СagA, VacA, ice, bab и уреазы, активно участвуют в развитии процесса воспаления. Штаммы I типа, обладающие наибольшей цитолитической активностью, чаще всего обнаруживают при ЯБ. Наличие островка патогенности в геноме бактерии, маркёром которого является Сag, связано с более выраженным воспалением. Любой фактор, усиливающий воспаление, увеличивает риск возникновения ЯБ.
Важнейшее открытие в патогенезе ЯБ — обнаружение влияния H. pylori на желудочную секрецию. Кроме прямого влияния на регуляцию секреции, H. pylori воздействует и опосредованно, вызывая хронический гастрит. Образующийся под влиянием уреазы аммиак способствует увеличению pH слизистого слоя эпителия желудка, вмешиваясь в физиологический механизм отрицательной обратной связи между секрецией гастрина и хлористоводородной кислоты.
Развитие ЯБ двенадцатиперстной кишки связано со следующими важными факторами:
гиперсекреция соляной кислоты, в том числе, наследственно обусловленная, приводящая к желудочной метаплазии слизистой оболочки двенадцатиперстной кишки;
миграция H. pylori с током слизи из желудка в двенадцатиперстную кишку и последующее заселение её.
H. pylori влияет на секрецию и синтез гастрина путём воздействия на D -клетки. Известен дефицит D -клеток у больных ЯБ двенадцатиперстной кишки, т.е. бактерии влияют не только на G -клетки, но и на соматостатиновое звено регуляции. Это ведёт к характерному для больных ЯБ изменению концентрации гастрина, соматостатина в крови и количества эндокринных клеток в антральном отделе. Вырабатываемая микроорганизмом уреаза обладает сильными иммуногенными свойствами, способствует образованию цитокинов, свободных радикалов и цитотоксических продуктов (в первую очередь, вакуолизирующего цитотоксина VacA). Образование свободных радикалов связывают с секрецией H. pylori хемотаксического пептида и воспалительной реакцией в слизистой оболочке желудка в ответ на внедрение микроорганизма. Превращаясь в активные метаболиты кислорода, свободные радикалы оказывают непосредственное токсическое действие на эпителиоциты.
Уреаза способствует гидролизу мочевины в диоксид углерода и ион аммония. Аммиак взаимодействует с соляной кислотой, генерируемой нейтрофилами, образуя ряд цитотоксических продуктов, в том числе гидроксиамин (NH4OH) и монохлорамин (NH4Cl). Кроме того, липополисахариды и фосфолипазы А и C, выделяемые H. pylori, непосредственно повреждают эпителиоциты, снижают вязкость муцина и гидрофобные свойства слизистой оболочки, что способствует образованию микродефектов последней.
В 1995 г. доказаны постулаты Р. Коха о причинной роли H. pylori для язвенной болезни. И все же, если инфицированием H. pylori можно объяснить возникновение ЯБ двенадцатиперстной кишки и отчасти — пилороантральных язв желудка, то причина пептической язвы в теле желудка до конца не установлена. Обследование семей с генетической предрасположенностью к ЯБ показало, что наличия одного и того же вирулентного штамма бактерии недостаточно: ЯБ желудка оказалась не у всех родственников.
Локализация. ДляЯБ желудка характерная локализация хронической рецидивирующей язвы — тело желудка (медиагастральная язва) или пилороантральная область.
Для ЯБ двенадцатиперстной кишки характерна локализация язвы на передней или задней стенках луковицы двенадцатиперстной кишки. Обычно находят одну, реже две, крайне редко — три язвы.
Патогенезязвенной болезни зависит от локализацииязв. Для ЯБ желудка и ЯБ двенадцатиперстной кишки с пилороантральной язвой он сходен и полностью отличается от патогенеза ЯБ желудка с медиагастральной локализацией язвы. На этом основании при изучении патогенеза выделяют пилородуоденальные язвы и язвы тела желудка.
Многочисленные патогенетические факторы, влияющие на развитие ЯБ, условно делят на общие и местные.
● Общие факторы — нарушения соотношений между факторами агрессии желудочного сока и факторами защиты слизистой оболочки желудка.
● Местные факторы — нарушения нервной и гормональной регуляции гастродуоденальной системы.
● Общие факторы патогенеза.
◊ Неврогенные факторы нарушают координирующую роль коры головного мозга в отношении подкорковых структур (промежуточного мозга, гипоталамуса). Пилородуоденальные язвы возникают на фоне возбуждения центров гипоталамо-гипофизарной области, центра блуждающего нерва, повышение тонуса последнего под влиянием стресса или патологии внутренних органов. Повышение тонуса блуждающего нерва приводит к активации кислотно-пептического фактора, нарушению моторики желудка и двенадцатиперстной кишки. Язвы тела желудка имеют противоположный патогенез: кора головного мозга угнетает функции гипоталамо-гипофизарной области, что неизбежно ведёт к снижению тонуса блуждающего нерва, в последующем возможно снижение активности желудочной секреции.
◊ Гормональные факторы развития ЯБ включают различные расстройства гипоталамо-гипофизарно-адреналовой системы. Пилородуоденальные язвы существуют на фоне избыточной продукции АКТГ и глюкокортикоидов, что также способствует повышению тонуса блуждающего нерва. Медиагастральные язвы, наоборот, возникают при снижении уровня этих гормонов.
● Местные факторы патогенеза:
факторы агрессии желудочного сока— соляная кислота и пепсиноген;
фактор защиты слизистой оболочки желудка—слизистый барьер.
Нарушения баланса факторов агрессии и защиты связано с изменением местной гормональной регуляции, моторикой желудка и/или двенадцатиперстной кишки, состоянием кровотока.
Пилородуоденальные язвы. Характерно значительное преобладание кислотно-пептического фактора агрессии над факторами защиты слизистой оболочки. Гиперсекреция соляной кислоты — основной патофизиологический механизм развития язв двенадцатиперстной кишки и пилорического отдела желудка. Увеличение количества соляной кислоты как минимум вдвое обусловлено повышенным содержанием гастрина в связи с гиперплазией G -клеток и гистамина, влияющих на париетальные клетки. Важную роль при этом играют двигательные расстройства: при язве двенадцатиперстной кишки обычно ускорена эвакуация желудочного содержимого из-за повышенной моторики желудка или беспорядочного аритмичного функционирования привратника. При этом укорочено время связывания соляной кислоты буферными компонентами пищи и активный желудочный сок поступает в кишку. Возможны и двигательные нарушения со стороны самой двенадцатиперстной кишки. При этом эвакуация из желудка нормальна, но замедлено прохождение комка пищи по кишке (дуоденостаз), что увеличивает время контакта слизистой оболочки кишки с кислым содержимым желудка. В обоих случаях нарушения моторики происходит кислотно-пептическое повреждение слизистой оболочки.
Язвы тела желудка. Активность кислотно-пептического фактора нормальна или даже слегка понижена, а на первом плане — ослабление факторов защиты слизистой оболочки, когда слизистый барьер желудка повреждён из-за обратной диффузии водородных ионов. Моторная функция не существенна для развития язв тела желудка.
H. pylori участвует в патогенезе ЯБ, усиливая факторы агрессии желудочного сока и ослабляя факторы защиты слизистой оболочки.
Ослабление факторов защиты возможно при прямом контакте H. pylori с мембранами эпителиоцитов желудка или двенадцатиперстной кишки. Под действием ионов аммония (уреаза H. pylori разлагает мочевину с образованием ионов аммония и углекислого газа), цитотоксинов, бактериальных ферментов происходит повреждение микроворсинок эпителиоцитов, разрушение их цитоскелета, межклеточных связей, изменение вязкости слизи. Ферменты H. pylori действуют на слизь, способствуя первоначально её липолизу и протеолизу, а затем деградации гликопротеинов и липидов. Феномен повреждения слизистого барьера C.S. Goodwin назвал образно «протекающей крышей».
Когда защитный слой слизи истончён или разрушен, возникает обратная диффузия водородных ионов и покровный эпителий, первоначально повреждённый прямым действием микроорганизма, получает ещё большее повреждение под действием водородных ионов, пепсина. В результате возникает сначала эрозия, а затем язва.
Существует и другой механизм воздействия H. pylori на кислотно-пептический фактор: адгезия H. pylori к эпителиальным клеткам вызывает в них экспрессию гена, кодирующего синтез ИЛ-8. Последний активизирует иммуноциты, что приводит к секреции различных цитокинов, включая ИЛ-2, ФНО-α ИФ-γ. Это, в свою очередь, может приводить к активации гена гастрина и гипергастринемии с последующим усилением синтеза кислоты. Соматостатиновый механизм торможения при этом не действует из-за щелочной среды — аммиака, образованного с помощью H. pylori.
Морфологический субстрат ЯБ — хроническая рецидивирующая язва. При формировании она проходит стадии эрозии, острой язвы и хронической язвы.
● Эрозия— поверхностный дефект, обычно не проникающий за мышечный слой слизистой оболочки. Они возникают в результате отторжения некротических масс с образованием многочисленных дефектов конической формы. Микроскопически в дне эрозий находят солянокислый гематин и лейкоцитарный инфильтрат. Большинство эрозий эпителизируется, но при ЯБ деструкция стенки желудка продолжается, некрозу подвержена не только слизистая оболочка, но и более глубокие слои стенки, формируется острая язва.
● Острая язва обычно имеет неправильную форму и мягкие на ощупь неровные края. По мере очищения от некротических масс обнажается дно, образованное пучками мышечных волокон стенки желудка, язва приобретает воронкообразную форму с основанием воронки, обращенным к слизистой, а верхушкой — к серозной оболочке. Острые язвы располагаются по малой кривизне в пилорическом и антральном отделах, т.е. по «пищевой дорожке» в местах наибольшего травмирования стенки желудка.
● Хроническая язва желудка обычно единичная (изредка две, ещё реже три язвы), овальной или округлой формы (ulcus rotundum), разных размеров (от нескольких миллиметров до 3,5 см). Она проникает в стенку на различную глубину, доходя иногда до серозной оболочки. Дно язвы может быть гладким и шероховатым, края приподняты, плотные, омозолелые (каллёзная язва), при этом кардиальный край язвы подрыт, а край, обращенный к привратнику — пологий, иногда имеет вид террасы. Подобная конфигурация обусловлена постоянным смещением краёв при перистальтике желудка.
Микроскопическая картина хронической язвы желудка зависит от стадии заболевания: обострение или ремиссия.
● В период ремиссии в дне язвы видна рубцовая ткань, вытесняющая мышечную оболочку стенки желудка на определённую глубину. Среди рубцовой ткани — одиночные сосуды со склерозированными стенками и суженным просветом, иногда разрастания нервных волокон, напоминающие ампутационные невромы. На поверхности рубцовая ткань чаще всего покрыта слизистой оболочкой, хотя последняя обычно отсутствует при крупных язвах. В краях язвы — признаки гиперплазии эпителия, характерные для хронического гастрита.
● В период обострения в области дна и краёв заметна широкая зона фибриноидного некроза, прикрытая сверху фибринозно-гнойным экссудатом. Снизу эту зону обрамляет грануляционная ткань. В глубине дна язвы — зона грубоволокнистой рубцовой ткани. Об обострении язвы говорят не только экссудативно-некротические изменения дна язвы, но и фибриноидные изменения стенок сосудов. В связи с появлением в дне язвы свежих очагов некроза размеры язвы в период обострения увеличиваются в глубину и в ширину, создавая опасность развития тяжёлых деструктивных осложнений (рис. 13-4).
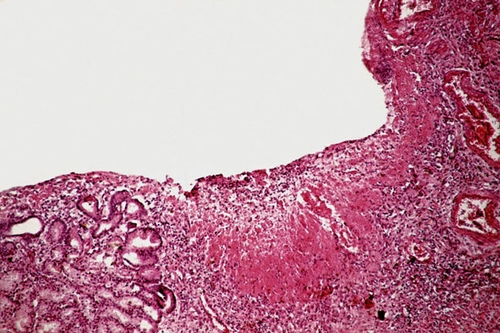
Рис. 13-4. Хроническая язва желудка с подрытым кардиальным и пологим пилорическим краями. Окраска гематоксилином и эозином (x100).
Заживление язвы начинается с постепенного очищения дна язвы от некротических масс и рассасывания экссудата. Зону некроза прорастает грануляционная ткань, она постепенно созревает в грубоволокнистую рубцовую ткань. Одновременно регенерирующий эпителий с краёв язвы начинает «наплывать» на дно. Процесс регенерации эпителия и соединительной ткани должен происходить синхронно. Эпителий стимулирует рост и созревание соединительной ткани, вырабатывая коллагеназу, необходимую для перестройки рубца. Когда эпителизация дна язвы задерживается, возникает преждевременный склероз грануляционной ткани. Это ещё более замедляет эпителизацию, создавая порочный круг. Эпителий, первоначально одним рядом закрывший дно язвы, продолжает регенерировать, и со временем в дне язвы формируется полноценная слизистая оболочка. Первоначально под новообразованной слизистой оболочкой видна грануляционная ткань с её многочисленными кровеносными сосудами (красный рубец). По мере созревания грануляционной ткани эндоскопическая картина меняется, возникает белый рубец.
Морфогенез и патологическая анатомия хронической язвы двенадцатиперстной кишки и желудка сходны, за исключением сроков заживления. Хроническая язва желудка заживает за восемь недель, язва двенадцатиперстной кишки — за шесть недель. Подслизистая основа и мышечная оболочка в области дна язвы не восстанавливаются, а замещаются рубцом. Таким образом, широко распространённый термин «рубец после язвы» имеет отношение к подслизистой основе и мышечной оболочке стенки желудка, тогда как слизистая оболочка регенерирует без формирования рубца. Поскольку полной регенерации в дне язвы желудка не происходит, заболевание протекает хронически, волнообразно, с обострениями и ремиссиями.
Прогрессирование язвенного процесса проявляется очередным расширением и углублением язвенного дефекта. При этом различают два варианта увеличения размеров язвы:
центрифугальный — за счёт разрушения краёв язвы;
центрипетальный — за счёт образования эрозий и острых язв около хронической язвы с последующим их слиянием; глубину язвы увеличивает некроз в области дна.
Осложнения язвенной болезни. При ЯБ желудка и двенадцатиперстной кишки возможны осложнения деструктивные (перфорация язвы, кровотечение, пенетрация); воспалительные (гастрит, перигастрит, дуоденит, перидуоденит) и рубцовые (стеноз входного и выходного отверстий желудка, стеноз и деформация луковицы двенадцатиперстной кишки, деформацияжелудка). Наиболее частые из этих осложнений — кровотечение и перфорация.
● Кровотечениенаблюдают у 16–37% больных с незажившими язвами. При дуоденальных язвах кровотечение возникает вдвое чаще. Летальность при кровоточащих дуоденальных язвах составляет 1–7%, при язвах желудка 1–16%. Особенно высока смертность от кровотечений у лиц пожилого возраста. У больных моложе шестидесяти лет она составляет 4%, старше семидесяти лет — 20%. Кровотечение связано с аррозией сосудов дна язвы, поскольку стенки сосудов за годы течения ЯБ склерозированы и гиалинизированы. В период обострения, когда в сосудах развивается фибриноидный некроз, они длительное время не спадаются, что приводит к фатальному кровотечению.
● Перфорация стенки с развитием перитонита занимает второе место среди осложнений. Это осложнение возникает всего в 5% случаев, однако ему принадлежит первое место среди причин смерти больных ЯБ — 2/3 всех случаев. Чаще всего перфорируют пилородуоденальные язвы — в шесть раз чаще, чем язвы тела желудка. Ежегодно частота перфорация язв составляет 7–10 случаев на 100 тыс. населения.
ОПУХОЛИ ЖЕЛУДКА
Опухоли желудка классификация ВОЗ (2000 г.) делит на следующие виды:
эпителиальные (интраэпителиальная неоплазия) — аденома, карцинома (рак);
неэпителиальные — все остальные опухоли, в желудке они крайне редки.
Рак желудка долгое время лидировал среди онкологических заболеваний. Несмотря на глобальное снижение заболеваемости, рак желудка по-прежнему одна из самых распространённых опухолей человека. Ежегодно в мире от рака желудка умирает около 1 млн. человек. Пятилетняя выживаемость за последние шестьдесят лет не изменилась и составляет 10%.
Эпителиальные опухоли. Интраэпителиальная неоплазия и аденома желудка в классификации опухолей ВОЗ и Венской классификации желудочно-кишечной эпителиальной неоплазии (дисплазии) стоят рядом и приравнены друг к другу. Таким образом, аденома — интраэпителиальная неоплазия. Не существует аденомы без дисплазии эпителия, причем дисплазия (она же — интраэпителиальная неоплазия) может быть выражена в разной степени — от низкой до высокой. Далее следует малигнизация — сначала неинвазивная (cancer in situ), а затем инвазивная карцинома. Аденома обычно имеет вид одиночного полипа на тонкой, реже на широкой ножке. На первых этапах роста она располагается в толще слизистой оболочки по типу плоской аденомы, в этих случаях её невозможно диагностировать даже эндоскопически. Из всех полипов желудка аденома (аденоматозный полип) составляет 5–10%. Опухоль обнаруживают преимущественно в антральном отделе. Частота её возникновения с возрастом возрастает, у мужчин в два раза чаще, чем у женщин.
Рак желудка
Основные факторы развития рака желудка — питание, билиарный рефлюкс и инфицирование H. pylori.
● Питание. Результаты эпидемиологических обследований доказали этиологическую роль особенностей питания в развитии рака желудка, особенно метаплазии по кишечному типу, в разных популяциях населения. Достаточное употребление свежих фруктов и овощей уменьшает риск развития рака желудка (антиоксидантный эффект аскорбиновой кислоты, каротиноидов, фолатов и токоферолов). Доказано, что употребление избытка соли повышает риск развития рака желудка и предраковых изменений. Другие продукты питания, повышающие риск развития заболевания в некоторых популяциях — копчёности, мясные и рыбные консервы, маринованные овощи, красный перец.
● Билиарный рефлюкс. Риск развития рака желудка возрастает через 5–10 лет после операций на желудке, особенно после операций по Бильроту II, способствующих развитию рефлюкса.
● Инфицирование Helicobacter pylori. Доказана этиологическая роль H. pylori в развитии рака желудка. H. pylori вызывает фенотипические изменения, приводящие к развитию рака: атрофию слизистой оболочки, кишечную метаплазию и дисплазию эпителия. Большинству случаев рака желудка предшествует длительный, в течение десятилетий предраковый процесс. Он включает следующую цепь событий: хронический гастрит, мультифокальную атрофию, кишечную метаплазию, интраэпителиальную неоплазию (процесс, называемый каскад Correa). H. pylori как патогенная бактерия отвечает за несколько этапов канцерогенного каскада.
Гастрит и атрофия слизистой оболочки нарушают продукцию соляной кислоты, что увеличивает значение pH в желудке. Изменяется желудочная микрофлора, и анаэробные микроорганизмы колонизируют слизистую оболочку. Эти бактерии синтезируют редуктазы — ферменты, способствующие превращению нитратов пищи в нитриты. Нитриты — активные молекулы, они могут реагировать с аминами, амидами и мочевиной с образованием канцерогенов, содержащих нитратную группу.
H. pylori — наиболее распространённая причина хронического гастрита. Этот микроорганизм приводит к снижению секреции соляной кислоты и пепсина, нарушает антиоксидантную функцию, уменьшая концентрацию аскорбиновой кислоты в желудке. H. pylori почти всегда находится в слое слизи, покрывающей желудочный эпителий, но не в фокусах кишечной метаплазии, где как раз и развивается рак. Таким образом, H. pylori осуществляет канцерогенное влияние на расстоянии через растворимые продукты своей жизнедеятельности и последующий воспалительный ответ на инфекцию.
Популяция H. pylori генетически неоднородна и, возможно, не все штаммы одинаково канцерогенны. Штаммы, имеющие группу генов саg, вызывают более выраженное воспаление, чем штаммы, не имеющие таких генов. Это связано с продукцией ИЛ-8 эпителиальными клетками. Доказана связь развития рака желудка именно с саg -позитивными штаммами H. pylori. H. pylori также может продуцировать вакуолизирующий цитотоксин (VасА) — канцероген, повреждающий эпителий. Этиологическая роль H. pylori в развитии рака желудка подтверждена в опытах на животных. При заражении животных саg - и vaс -позитивными штаммами H. pylori развивалась кишечная метаплазия и рак желудка.
Повышенная клеточная пролиферация, неотъемлемое звено канцерогенеза, потенцирует действие канцерогенов в отношении ДНК. Чем более интенсивно происходит репликация, тем выше вероятность закрепления ошибок репликации и их продолжения в последующих поколениях клеток. Спонтанные мутации ведут к последующей неопластической трансформации. При раке желудка выявлены некоторые мутации по типу делеций, приводящие к выпадению тумор-супрессорных генов (в регионах 3р, 4, 5q, 6q, 9p, 17p, 18q, 20q), амплификация генов (в регионах TGF, β-рецепторов, BAX, IGFR II, hMSH3, hMSH6, E2F4), амплификация и избыточная мутация с-met гена, кодирующего рецепторы тирозинкиназы фактора роста гепатоцитов, соматические мутации гена АРС. Существенная утрата аллелей в локусе АРС заставляет предположить, что там располагается тумор-супрессорный ген, ответственный или влияющий на канцерогенез в желудке.
Оксидантный стресс. При гастрите возрастает продукция оксидантов и активных соединений азота, в том числе оксида азота NO. Повышено образование определённых изоформ, например, оксидазотсинтазы, обусловливающей длительную продукцию больших количеств оксида азота. Последний также образуется в просвете желудка без участия энзимов. Окисление нитрита до оксида азота даёт активное соединение азота — динитрогендиоксида N2O3, из него образуются нитрозитиолы и нитрозоамины, имеющие доказанную канцерогенную активность.
Нарушение антиоксидантной защиты. Предположительный механизм антиоксидантного действия аскорбиновой кислоты — предотвращение повреждения ДНК оксидантами. У лиц, инфицированных H. pylori, концентрация аскорбиновой кислоты в крови ниже, чем у неинфицированных. После эрадикации H. pylori концентрация аскорбиновой кислоты приходит к норме.
Повреждение ДНК. Свободные радикалы, оксиданты и активные соединения азота вызывают повреждения ДНК. Обычно это приводит к появлению точечных мутаций, наиболее частые из них — G, C - АТ, связанные с воздействием химических канцерогенов. Пероксинитрит способствует образованию нитрогуанина, вызывающего повреждение ДНК, затем следует репарация или апоптоз. Последний выключает клетки, содержащие поврежденную ДНК, из пула делящихся клеток, чтобы удалить мутации из генома. При этом риск развития рака снижается. Оксид азота нарушает репарацию ДНК, воздействуя на белок Fpg, ответственный за её репарацию. Таким образом, оксид азота не только повреждает ДНК, но и нарушает механизм её репарации.
В присутствии бактерии H. pylori клеточная пролиферация усиливается и уравновешивается апоптозом. Вероятно, увеличение митозов возникает в ответ на повышенную гибель эпителиальных клеток. Тем не менее, уровень репликации превосходит уровень апоптоза у пациентов, инфицированных вирулентными штаммами H. pylori, содержащими саgA, vacA, s 1 a. Это говорит о том, что гибель эпителия обусловлена также воздействием токсинов H. pylori. У пациентов с H. pylori -ассоциированным гастритом при лечении антиоксидантами уровень апоптоза и образования пироксинитрита снижен. Очевидно, что пищевые нитриты, нитрозоамины и H. pylori -ассоциированный гастрит также оказывают канцерогенное действие. На фоне этих хронических процессов возможность критического повреждения генома клетки многократно возрастает.
Предраковые состояния. Исключительно редко опухоль возникает в практически здоровом желудке, на неизменённом фоне (de novo). Значительно чаще ему предшествуют предраковые состояния и предраковые изменения. Злокачественный потенциал их различен, суммарно они повышают вероятность возникновения рака по сравнению с общей популяцией на 20–100%. В настоящее время к предраковым состояниям относят аденому желудка (аденоматозный полип), хронический атрофический гастрит, пернициозную анемию, инфицирование H. pylori.
● Аденома желудка на начальных этапах роста располагается в толще стенки желудка (плоская аденома), но со временем по мере увеличения размеров приобретает форму экзофитного образования (аденоматозный полип). Дисплазия эпителия обязательна, она нарастает от слабой степени до тяжёлой с последующей малигнизацией примерно в одной трети случаев.
● Хронический атрофический гастрит составляет 75% в структуре предраковых заболеваний из-за своей распространённости. Установлено, что кишечный тип рака желудка имеет определённую эпидемиологическую связь с хроническим гастритом. Рак диффузного типа эпидемиологической связи с гастритом не имеет.
● Пернициозная анемия — заболевание, способствующее развитию рака желудка в 3–10 раз чаще, чем в общей популяции. Оно проявляется быстро прогрессирующим тяжёлым атрофическим гастритом тела желудка.
● Инфицирование H. pylori. Международное агентство по изучению рака (IARC) ВОЗ отнесла к канцерогенам I группы, т.е. факторам с доказанной канцерогенностью для человека. Рак желудка — результат длительного многоступенчатого и многофакторного процесса клеточных изменений на фоне нарушений микроокружения. Главная причина этих нарушений — H. pylori. Клеточное обновление в слизистой оболочке желудка происходит за счёт генеративной зоны, расположенной в дне ямок. Эта зона становится мишенью для канцерогенов при наличии H. pylori: он усиливает факторы агрессии желудочного сока и ослабляет факторы защиты слизистой оболочки. В результате клеточные пролиферации теряют управляемость. Клеточная репликация — непременное условие канцерогенеза, она потенцирует действие всех канцерогенов. «Хронический митогенез ведёт к мутагенезу» — это выражение полностью применимо к раку желудка при инфировании H. pylori.
Динамическое эндоскопическое исследование показало, что рак желудка развивается у 10% больных с тяжёлым атрофическим гастритом. В то же время, у больных раком желудка хронический гастрит вне опухоли обнаруживают только в 1/3 случаев. Поэтому эпидемиологическое значение хронического гастрита как предрака ограничено.
В последней международной классификации гастритов выделен ещё один вариант — мультифокальный гастрит, при нём бывает поражена область угла желудка, малая кривизна и интрамедиальная зона. Очаги воспаления со временем сливаются, захватывая тело желудка и антральный отдел. Этот тип гастрита преобладает в зонах высокого риска развития рака (Колумбия, Новый Орлеан).
Особая форма гастрита развивается у больных, перенёсших операции на желудке (по поводу полипоза, язвы и других заболеваний, но не рака). В культе желудка возможно нарушение процессов эвакуации и длительный заброс жёлчи вместе с панкреатическим содержимым, что ведёт к стойкому необратимому снижению кислотности желудочного сока. Гипо- и ахлоргидрия — условия для размножения бактериальной флоры, что способствует восстановлению и длительному пребыванию в желудке нитратов и/или нитритов, оказывающих мутагенное действие. Предраковые изменения в культе наступают не сразу, а как минимум через десять лет после операции: если через десять лет после резекции желудка рак культи развивается у 5–8,2% больных, то через двадцать лет эта цифра возрастает в 6–8 раз.
Пересмотрен взгляд на роль хронической язвы в патогенезе рака желудка. Совершенные эндоскопические методы установили, что частота малигнизации хронической язвы желудка не превышает 1%.
Предраковые изменения желудка. Согласно рекомендациям комитета экспертов ВОЗ, это тяжёлая дисплазия и кишечная метаплазия эпителия желудка. Кишечная метаплазия бывает полная (тонкокишечная) и неполная (толстокишечная). Только для неполной, или толстокишечной метаплазии характерны признаки клеточной атипии, свойственные дисплазии.
Дисплазия,по рекомендациям Международных экспертов ВОЗ, приравнена к неоплазии, т.е. опухолевому процессу. В 2000 г. в Вене была принята согласованная Международная классификация эпителиальных неоплазий желудочно-кишечного тракта (табл. 13-1).
Таблица 13-1. Согласованная Международная классификация желудочно-кишечной эпителиальной неоплазии (2000 г.)
| Категория | Выраженность неоплазии |
| Категория 1 | Отсутствие неоплазии /дисплазии |
| Категория 2 | Неопределённая неоплазия /дисплазия |
| Категория 3 | Неинвазивная неоплазия низкой степени (низкая степень аденомы/ дисплазии) |
| Категория 4 | Неинвазивная неоплазия высокой степени |
| 4.1 4.2 4.3 | Аденома/ дисплазия высокой степени Неинвазивная карцинома (карцинома in situ) Подозрение на инвазивную карциному |
| Категория 5 | Инвазивная неоплазия |
| 5.1 5.2 | Интрамукозная карцинома Субмукозная или более глубокая карцинома |
В этой классификации дисплазия определена как неоплазия (неоплазма — клон клеток, отличающихся от других тканей автономным ростом и соматическими мутациями), т.е. опухоль. В пятую категории вошло такое состояние как интрамукозная карцинома, требующее срочного оперативного вмешательства. Мало того, даже неинвазивная неоплазия (категория 4) — показание к эндоскопической или хирургической резекции слизистой оболочки.
Морфогенез рака желудка подразумевает морфологию последовательных стадий или этапов развития рака от ранних предраковых поражений до распространённого рака, способного к генерализованному метастазированию. Проблема начала развития рака желудка, его канцерогенеза далека от решения. Предполагают генетическую связь между дисплазией эпителия, возникающей при всех вышеперечисленных предраковых состояниях желудка, и развитием рака. Доказательством служит общий источник развития и дисплазии, и рака желудка — область ямок и шеек желёз, где происходит естественная пролиферация и последующая дифференцировка эпителия.
Рак развивается из очагов дисплазии желудочного эпителия или эпителия метаплазированного, т.е. перестроенного по кишечному типу (толстокишечная метаплазия с клетками, секретирующими сульфомуцины). Тяжёлая дисплазия прогрессирует, возникает сначала неинвазивный рак (саrcinoma in situ), а затем инвазивный рак. Развитие инфильтрирующего рака начинается с пенетрации опухолевыми клетками базальной мембраны. Этот момент можно уловить, используя иммуногистохимические методы, в частности, антитела к ламинину и коллагену IV типа при микрокарциноме и внутрислизистом раке.
Гистогенез (канцерогенез) рака желудка.
● Рак желудка кишечного типа проходит следующие стадии развития: хронический атрофический гастрит — кишечная метаплазия — дисплазия — рак.
● Рак желудка диффузного типа не имеет такой последовательности развития, он обычно возникает на фоне неатрофического (поверхностного) гастрита.
Выделяют два пути канцерогенеза.
● Первый путь подразумевает первичное повреждение механизмов пролиферации и дифференцировки. Этот процесс относительно медленный, вялотекущий. Его начало — активный хронический гастрит, переходящий через кишечную метаплазию и дисплазию в рак кишечного типа.
● Второй путь связан с нарушениями экспрессииили мутацией генов, ответственных за синтез белков базальной мембраны, таких как ламинин, коллаген IV типа, интегринов, протеинов zonula adherens (кадхерин, катенин). Этот процесс быстро ведёт к формированию рака из недиспластичного шеечного эпителия. Инициирует оба пути канцерогенеза хеликобактерный активный гастрит, вовлекающий генеративную зону желудка.
Клинико - анатомическая классификация рака желудка учитывает параметры опухоли: локализацию в желудке, характер роста (экзофитный или эндофитный), макроскопическую форму, гистологический тип.
● По локализациивыделяют рак:
пилорического отдела;
малой кривизны с переходом на заднюю и переднюю стенки;
кардиального отдела;
большой кривизны;
дна желудка;
субтотальный, если опухоль занимает больше одного отдела желудка;
тотальный, если поражены все отделы желудка.
Опухоль может располагаться в любом отделе желудка, но самая частая локализация — пилорический отдел и малая кривизна (3/4 всех карцином желудка).
● Макроскопические формы рака желудка.Опухоли желудка растут либо в просвет желудка (экзофитно), либо в толщу стенки (эндофитно). Макроскопически их классифицируют с учётом преобладания того или иного характера роста.
◊ Преимущественно экзофитные опухоли: рак бляшковидный, полипозный, грибовидный, изъязвлённые раки (в том числе первично-язвенный, блюдцеобразный, язва-рак, т.е. рак, развившийся из язвы).
◊ Преимущественно эндофитные опухоли: диффузный рак, инфильтративно-язвенный рак.
◊ Смешанные экзо-эндофитные опухоли (переходные формы рака).
Ä Бляшковидный рак — редкая форма, представлена плоским, напоминающим бляшку образованием, слегка приподнятым над слизистой оболочкой желудка, обычно небольших размеров. Опухоль располагается в слизистой оболочке, последняя подвижна, на разрезе слои стенки желудка хорошо различимы. Обычно клинически ничем себя не проявляет, бывает случайной находкой при гастроскопическом исследовании.
Ä Полипозный рак имеет характерный вид полипа на тонкой ножке, растущего в просвет желудка, мягкого на ощупь, подвижного. Часто опухоль возникает при малигнизации аденоматозного полипа, реже из бляшковидного рака при преобладании экзофитного роста. Гистологически опухоль преимущественно имеет строение папиллярной аденокарциномы.
Ä Грибовидный рак растёт на широком основании и внешне напоминает цветную капусту. Опухоль чаще расположена на малой кривизне тела желудка и постоянно подвержена травмам, поэтому на её поверхности обычно наблюдают эрозии, кровоизлияния и очаги некроза, покрытые фибринозным налетом. Часто представляет собой стадию дальнейшего роста полипозного рака.
Ä Изъязвлённый рак — самая распространённая макроскопическая форма. Выделяют три разновидности различного генеза: первично-язвенный рак, блюдцеобразный рак и язва-рак.
Первично-язвенный рак с самого начала своего развития, т.е. со стадии плоской бляшки подвергается изъязвлению. При этом опухоль проходит три стадии развития: раковой эрозии, острой язвы, хронической раковой язвы. Симптомы первично-язвенного рака обычно характерны для ЯБ, выявляют его чаще на поздних стадиях. Эту форму рака практически невозможно отличить от хронической язвы желудка, подвергшейся малигнизации. Нередко имеет строение недифференцированного рака.
Блюдцеобразный рак — самая частая макроскопическая форма рака желудка. Опухоль имеет вид выбухающего в просвет желудка узла с валикообразно приподнятыми краями и западающим в центре дном. Обычно блюдцеобразный рак возникает в результате некроза и изъязвления грибовидного или полипозного рака.
Язва-рак — результат малигнизации хронической язвы. Опухоль располагается на малой кривизне (характерная локализация хронической язвы) и внешне также похожа на неё. Опухоль имеет вид плотной белесовато-серой ткани в одном из краёв язвенного дефекта. При далеко зашедшем процессе отличить язву-рак от блюдцеобразного рака невозможно.
Ä Диффузный рак —макроскопическая форма рака с выраженным эндофитным ростом. Опухоль представлена плотной белесовато-серой тканью, похожей на лён (отсюда старый термин — пластический линит). Опухоль прорастает стенку желудка. Последняя обычно утолщена до нескольких сантиметров, плотная, слои неразличимы; слизистая оболочка над опухолью резко сглажена, а просвет равномерно сужен. Желудок сморщен и уплотнён, напоминает по форме кобуру пистолета. По распространённости диффузный рак часто бывает субтотальным или тотальным, а микроскопически — недифференцированным со скиррозным типом роста, иногда слизистым раком.
Ä Инфильтративно-язвенный рак отличает выраженное прорастание стенки желудка опухолью и многочисленные эрозии или язвы на поверхности слизистой оболочки.
Ранний рак желудка — не временное понятие, это рак, располагающийся в слизистой оболочке желудка, реже в подслизистой основе, т.е. ранний рак — поверхностный рак. Обычно по размерам он невелик, иногда может достигать нескольких сантиметров, но не прорастает глубже подслизистого слоя. Выделение этой формы важно с клинической точки зрения, так как она имеет хороший прогноз. Пятилетняя выживаемость после операции составляет почти 100%, а метастазы обнаруживают не более чем у 5% больных. В классификации, предложенной японским эндоскопическим гастроэнтерологическим обществом, выделено три макроскопических типараннего рака желудка:
выступающий наружу, или полиповидный;
поверхностный (a — возвышающийся, b — плоский, c — вдавленный);
углублённый.
Гистологические типы рака желудка. Самая распространённая опухоль желудка — высоко-, умеренно и низкодифференцированная аденокарцинома. В зависимости от формы железистых структур аденокарцинома бывает папиллярная, тубулярная и муцинозная.
Кроме того, по гистологической классификации ВОЗ (2000 г.) выделяют следующие виды карциномы желудка:
перстневидноклеточная;
железисто-плоскоклеточная;
плоскоклеточная;
мелкоклеточная;
недифференцированная.
Существует ещё одна гистологическая классификация (по Лорен), согласно которой выделяют два варианта желудочной карциномы: кишечный и диффузный. Классификация терминологически несовершенна, т.к. первый тип рака выделен с учётом гистогенеза, второй — характера роста. Однако эта классификация получила широкое распространение на Западе.
● Кишечный тип рака, или интестинальный рак (термин обозначает, что микроскопически опухоль состоит из клеток эпителия кишечного типа). Как правило, это высокодифференцированная аденокарцинома. Диагностируют чаще в возрасте старше пятидесяти лет, у мужчин в два раза чаще, чем у женщин. Обычно имеет полипозную или грибовидную форму, развивается почти всегда на фоне хронического гастрита с кишечной метаплазией эпителия.
● Диффузный тип рака желудка — чаще недифференцированный перстневидноклеточный рак, реже низкодифференцированная аденокарцинома. Кишечная метаплазия вне опухоли крайне редка, в самой опухоли клетки, похожие на кишечный эпителий, также отсутствуют. Опухоль находят у лиц молодого возраста, одинаково часто у мужчин и женщин.
Метастазирование. Рак желудка даёт метастазы лимфогенным, гематогенным и имплантационным путями.
● Лимфогенные метастазы. Первые метастазы обычно возникают в регионарных узлах, расположенных на малой и большой кривизне желудка. В последующем возможны отдалённые лимфогенные метастазы в лимфатические узлы области ворот печени, парааортальные, паховые и др. (ортоградный путь). Рак желудка может давать метастазы в оба яичника (метастазы Крукенберга), параректальную клетчатку (метастазы Шницлера) и левый надключичный лимфатический узел (метастаз Вирхова). Это ретроградный путь.
● Гематогенные метастазы. Рак желудка чаще всего метастазирует в печень, реже в лёгкие, головной мозг, кости, почки, ещё реже — в надпочечники и поджелудочную железу.
● Имплантационные метастазы. Характерны метастазы в виде карциноматоза плевры, перикарда, диафрагмы, брюшины, сальника.
Осложнения при раке желудка могут возникнуть в связи с некрозом и воспалительными процессами в самой опухоли. Возможны перфорация стенки,кровотечение, перитуморозный гастрит, флегмона желудка.При прорастании опухолью головки поджелудочной железы, печёночно-дуоденальной связки развиваются желтуха, портальная гипертензия. Прорастание поперечно-ободочной кишки или корня брыжейки приводит к механической кишечной непроходимости. При локализации опухоли в пилорическом канале возможно развитие стеноза привратника. Осложнение карциноматоза плевры — геморрагический плевритилиэмпиема плевры. Наиболее часто при раке желудка возникают кахексия, обусловленная голоданием больных, выраженной интоксикацией, и железодефицитная анемия.
Среди неэпителиальных опухолей желудка наиболее интересна опухоль из группы злокачественных лимфом, называемая мальтомой.
Мальтома желудка
Мальтома— B-клеточная лимфома, происходящая из лимфоидной ткани, ассоциированной со слизистой оболочкой (mucosa associated lymphoid tissue — MALT). По сравнению с эпителиальными опухолями лимфомы в желудке редки и составляют 1–5% всех злокачественных новообразований желудка. Однако среди всех неходжкинских лимфом желудочно-кишечного тракта частота встречаемости лимфомы желудка — 40–60%.
Согласно последней пересмотренной Евро-Американской классификации лимфоидных опухолей (1994 г.), правильное название этой опухоли — экстранодальная B-клеточная лимфома краевой зоны низкой (или высокой) степени злокачественности. Гистологически опухоль состоит из разных типов клеток: малых лимфоцитов, клеток краевой зоны (центроцитоподобных), небольшой примеси крупных клеток и плазматических клеток опухолевой природы. Состав, плотность, глубина проникновения клеточного инфильтрата зависят от степени злокачественности мальтомы.
● При мальтоме низкой степени злокачественности обнаруживают диффузную инфильтрацию собственной пластинки слизистой оболочки желудка центроцитоподобными клетками или малыми лимфоцитами с примесью иммунобластов того же клона, плазматическими клетками, дифференцированными из опухолевых клеток, с наличием лимфоэпителиальных повреждений (проникновение лимфоцитов в желудочные железы и последующее их разрушение) и реактивных внутриопухолевых лимфоидных фолликулов. Инфильтрат разрушает железы, не затрагивая покровный эпителий, что способствует длительному скрытому течению заболевания.
● При мальтоме высокой степени злокачественности опухолевый инфильтрат очень плотный, выходит за мышечную пластинку слизистой оболочки, состоит из крупных бластов разной степени дифференцировки, среди них можно встретить клетки с расщеплёнными и перекрученными ядрами. Лимфоэпителиальных комплексов почти нет, т.к. большинство желёз разрушено. H. pylori обнаруживают реже, чем при мальтоме низкой степени дифференцировки.
Основной метод дифференциальной диагностики — морфологический, однако абсолютным критерием может быть только фенотипирование. Мальтомы высокой степени злокачественности экспрессируют р 53, иногда bcl -2, а в ядрах клеток опухоли с помощью молекулярных методов диагностики можно выявить хромосомную мутацию по типу транслокации.
Главная и уникальная особенность мальтомы желудка состоит в том, что она успешно регрессирует после эрадикации H. pylori. Основной механизм развития мальтомы желудка — аутоиммунный конфликт, запускаемый H. pylori.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 3556; Нарушение авторских прав?; Мы поможем в написании вашей работы!