
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Марганец
|
|
|
|
Хром
Примеры заданий части А
1. Среди металлов главной подгруппы II группы наиболее сильным восстановителем является
1) барий
2) кальций
3) стронций
4) магний
2. При сжигании магния на воздухе образуются
1) Mg(OH)2
2) MgO
3) Mg(NO3)2
4) Mg3N2
3. Алюминий будет выделять водород из реактива
1) HNO3 (разб.)
2) NaHSO4 (разб.)
3) H2SO4 (конц.)
4) NaOH (конц.)
4. Реакция замещения протекает в растворе между алюминием и
1) Na2SO4
2) BeSO4
3) NiSO4
4) MgSO4
5. Из раствора гидрокарбоната бария выпадает осадок при добавлении реактивов
1) ВаО
2) СO2
3) Ва(ОН)2
4) H2SO4
6. Калий можно получить электролизом на угольных электродах из
1) раствора КCl
2) раствора KNO3
3) расплава КCl
4) расплава смеси КCl и MgCl2
7–8. Если внести каплю раствора
7. поваренной соли
8. хлорида калия
в бесцветное пламя газовой горелки, оно станет
1) красным
2) желтым
3) зеленым
4) фиолетовым
9. Устранение временной жёсткости воды проводится по реакции
1) Са(НСO3)2 + Na3PO4 →…
2) Са(НСO3)2 + Са(ОН)2 →…
3) CaSO4 + Na2CO3 →…
4) СаCl2 + NaHCO3 →…
6. Переходные металлы 4‑го периода. Свойства, способы получения. Общие свойства металлов
Хром – элемент 4‑го периода и VIБ‑группы Периодической системы, порядковый номер 24. Электронная формула атома [18Ar]3d54s1, характерные степени окисления +VI, + III и 0.
Шкала степеней окисления хрома:
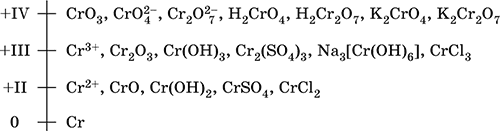
По электроотрицательности (1,56) хром занимает промежуточное положение между типичными металлами (Na, К, Са) и типичными неметаллами (F, О, N. CI, S). Соединения CrIII проявляют амфотерные свойства, металлические (основные) свойства преобладают у CrII, неметаллические (кислотные) – у CrVI; в соединениях хром чаще находится в составе катионов и реже – в составе анионов. Хром образует многочисленные соли и бинарные соединения.
В природе – девятнадцатый по химической распространенности элемент (десятый среди металлов), находится только в виде соединений (минералы, полиметаллические руды). Растворимые соли хрома ядовиты.
Хром Cr. Серый (с голубоватым оттенком) металл, очень твердый, ковкий (технический продукт – хрупкий). Блестящий, хотя покрыт очень тонкой оксидной пленкой, сохраняет блеск даже во влажном воздухе. Не реагирует с водой, щелочами и гидратом аммиака, пассивируется в концентрированной и разбавленной азотной кислоте и в «царской водке».
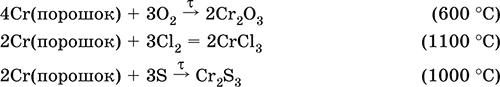
В ряду напряжений стоит левее водорода, из разбавленных кислот HCl и H2SO4 вытесняет водород:
Cr + 2H+ = Cr2+ + Н2↓
Далее катион Cr2+ можно перевести кислотами‑окислителями в катион Cr3+:

Хром реагирует в расплаве с сильными окислителями:
2Cr + КClO3 = Cr2O3 + КCl (500–700 °C)
2Cr + 3KNO3 = Cr2O3 + 3KNO2 (400–550 °C)
Получение хрома в промышленности – алюминотермия:
Cr2O3 + 2Al = 2Cr + Al2O3 (800 °C)
и электролиз раствора:
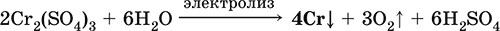
Промышленно важен сплав хрома с железом – феррохром (6O–85 % хрома), его производят восстановлением оксидов, например минерала хромит:
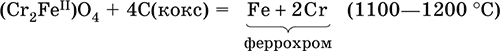
Применяется хром для создания защитных покрытий на других металлах (хромирование), как компонент механически прочных и коррозионно‑стойких сталей.
Гидроксид хрома (III) Cr(ОН)3. Амфотерный гидроксид. Серо‑зеленый, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrО(ОН). Не растворяется в воде. Из раствора осаждается в виде серо‑голубого и голубовато‑зеленого гидрата. Реагирует с кислотами и щелочами, не взаимодействует с гидратом аммиака. Применяется для синтеза соединений хрома (III).
Уравнения важнейших реакций:
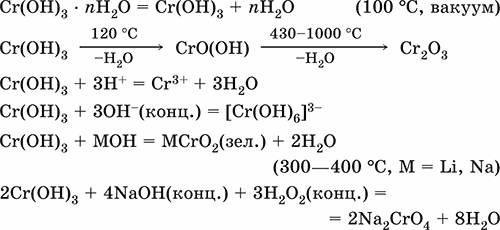
Получение: осаждение гидратом аммиака из растора солей хрома(III):
Cr3+ + 3(NH3 Н2O) = Cr(OH)3 ↓ + 3NH4+
Хромат калия К2CrO4. Оксосоль. Желтый, негигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде (желтая окраска раствора отвечает иону CrO42‑), незначительно гидролизуется по аниону. В кислотной среде переходит в К2Cr2O7. Окислитель (более слабый, чем К2Cr2O7). Вступает в реакции ионного обмена.
Качественная реакция на ион CrO42‑ – выпадение желтого осадка хромата бария, разлагающегося в сильнокислотной среде. Применяется как протрава при крашении тканей, дубитель кож, селективный окислитель, реактив в аналитической химии.
Уравнения важнейших реакций:
2К2CrO4 + H2SO4 (30 %) = К2Cr2O7 + K2SO4 + Н2O
2К2CrO4(т) + 16HCl (конц., гор.) = 2CrCl3 + ЗCl3↑ + 8H2O + 4КCl
2К2CrO4 + 2H2O + 3H2S = 2Cr(OH)3↓ + 3S↓ + 4KOH
2К2CrO4 + 8H2O + 3K2S = 2K3[Cr(OH)6] + 3S↓ + 4KOH
2К2CrO4 + 2AgNO3 = 2KNO3 + Ag2CrO4 (красн.)↓
Качественная реакция:
К2CrO4 + ВаCl2 = 2КCl + ВаCrO4↓
2BaCrO4(т) + 2HCl (разб.) = ВаCr2O7(р) + ВаCl2 + Н2O
Получение: спекание хромита с поташом на воздухе:
4(Cr2FeII)O4 + 8К2СO3 + 7O2 = 8К2CrO4 + 2Fe2O3 + 8СO2 (1000 °C)
Дихромат калия К2Cr2O7. Оксосоль. Техническое название хромпик. Оранжево‑красный, негигроскопичный. Плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (оранжевая окраска раствора отвечает иону Cr2O72‑). В щелочной среде образует К2CrO4. Типичный окислитель в растворе и при сплавлении. Вступает в реакции ионного обмена.
Качественные реакции – синее окрашивание эфирного раствора в присутствии Н2O2, синее окрашивание водного раствора при действии атомарного водорода.
Применяется как дубитель кож, протрава при крашении тканей, компонент пиротехнических составов, реагент в аналитической химии, ингибитор коррозии металлов, в смеси с H2SO4 (конц.) – для мытья химической посуды.
Уравнения важнейших реакций:

Марганец – элемент 4‑го периода и VIIB‑группы Периодической системы, порядковый номер 25. Электронная формула атома [18Ar]3d54s2; характерные степени окисления +VII, +VI, +IV, +II и 0.
Шкала степеней окисления марганца:
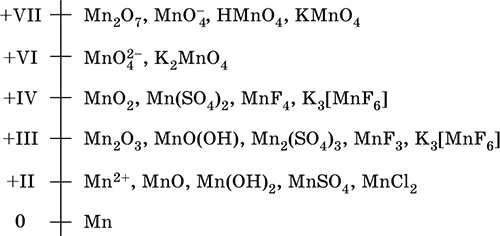
По электроотрицательности (1,60) марганец занимает промежуточное положение между типичными металлами (Na, К, Са, Mg) и неметаллами (F, О, N, Cl). Соединения MnII – оксид и гидроксид – проявляют основные свойства, соединения MnIII и MnIV – амфотерные свойства, для соединений MnVI и MnVII характерно почти полное преобладание кислотных свойств. Марганец образует многочисленные соли и бинарные соединения.
В природе – четырнадцатый по химической распространенности элемент (восьмой среди металлов; второй, после железа, тяжелый металл).
Марганец Mn. Серебристо‑белый (с серым оттенком) металл, более твердый и хрупкий по сравнению с железом. В виде мелкого порошка пирофорен. На воздухе покрывается оксидной пленкой. Пассивируется в воде, поглощает водород, но не реагирует с ним.
При нагревании сгорает в кислороде воздуха, реагирует с хлором и серой:
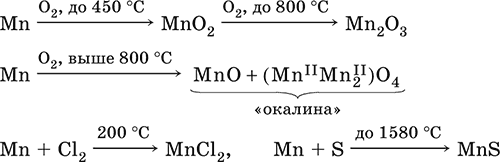
В ряду напряжений марганец стоит левее водорода, из разбавленных кислот HCl и H2SO4 вытесняет водород:
Mn (порошок) + 2H+ = Mn2+ + Н2↑
Взаимодействует с кислотами‑окислителями при нагревании, также образуя соли марганца (II):
Mn + 2H2SO4 (конц.) = MnSO4 + SO2↑ + 2Н2O
ЗMn + 8HNO3 (разб.) = 3Mn(NO3)2 + 2NO↑ + 4Н2O
Получение марганца в промышленности – восстановление пиролюзита MnO2 или гаусманита (MnIIMn2III)O4 коксом или алюминием:
MnO2 + С (кокс) = Mn + СO2 (600 °C)
3(MnIIMn2III)O4 + 8Al = 9 Mn + 4Al2O3 (700–900 °C)
Наиболее чистый марганец выделяют электролизом раствора из солей марганца(II), например:
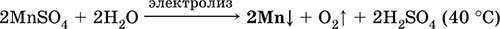
Промышленно важен сплав с железом – ферромарганец (> 70 % Mn), его получают восстановлением оксидных руд марганца и железа.
Применяется марганец для изготовления специальных и тугоплавких сплавов, зеркального чугуна и марганцевых твердых сталей, в качестве катализатора в органическом синтезе.
Оксид марганца (IV) MnO2. Черный, с коричневым оттенком, при нагревании разлагается. Из раствора осаждается в виде черного гидрата MnO2 nН2O. Не проявляет амфотерных свойств в силу малой реакционной способности по отношению к воде, разбавленным кислотам НCl и H2SO4, азотной кислоте и щелочам в растворе. Типичный окислитель в растворе и расплаве, менее характерны свойства восстановителя.
Применяется для промышленного производства марганца, как деполяризатор в «батарейках» (сухих гальванических элементах), компонент минеральных пигментов, осветлитель стекла.
Уравнения важнейших реакций:
4MnO2 = 2Mn2O3 + O2 (530–585 °C)
2MnO2 + 2H2SO4 (конц.) = MnSO4 + O2↑ + 2Н2O (кипячение)
MnO2 + 4HCl (конц.) = MnCl2 + Cl2↑ + 2H2O
MnO2 + H2SO4 (гор.) + KNO2 = MnSO4 + KNO3 + H2O
MnO2 + 2H2SO4 + 2FeSO4 = MnSO4 + Fe2(SO4)3 + 2H2O
MnO2 + 2KOH + KNO3 = K2MnO4 + KNO2 + H2O (350–450 °C)
3MnO2 + 3K2CO3 + KClO3 = 3K2MnO4 + KCl + 3CO2 (400 °C)
В природе самое распространенное соединение марганца – минерал пиролюзит.
Манганат калия К2MnO4. Оксосоль. Темно‑зеленый, плавится под избыточным давлением O2. В растворе устойчив только в сильнощелочной среде. Зеленая окраска раствора отвечает иону MnO42‑. Медленно разлагается при разбавлении раствора водой, быстро – при подкислении. Проявляет окислительно‑восстановительные свойства.
Качественная реакция – появление фиолетовой окраски при подкислении раствора. Промежуточный продукт при синтезе КMnO4.
Уравнения важнейших реакций:
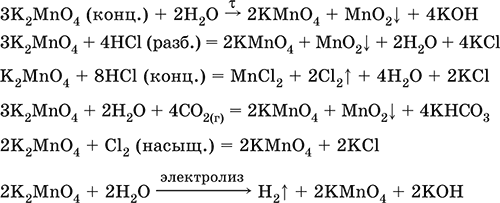
Получение: сплавление MnO2 с сильными окислителями (KNO3, КСlO3).
Пермапгапат калия КMnO4. Оксосоль. Красно‑фиолетовый (почти черный). При нагревании разлагается без плавления. Умеренно растворим в воде (интенсивно‑фиолетовая окраска раствора отвечает иону MnO4‑), гидролиза нет. Медленно разлагается в воде, серной кислоте, щелочах. Сильный окислитель в растворе и при сплавлении; в сильнокислотной среде восстанавливается до MnII, в нейтральной среде – до MnIV, в сильнощелочной среде – до MnVI.
Качественная реакция на ион MnO4‑ – исчезновение фиолетовой окраски раствора при восстановлении в кислотной среде.
Применяется как окислитель углеводородов до карбоновых кислот, реактив в фотографии, антисептик в медицине, средство для очистки газов и отбеливания тканей, твердый источник кислорода. Распространенный окислитель в лабораторной практике.
Уравнения важнейших реакций:
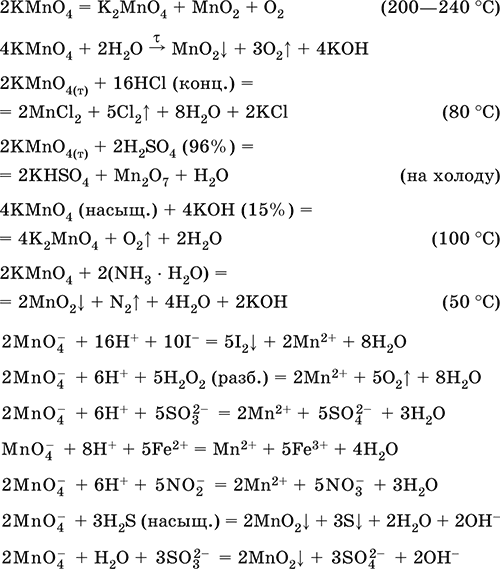
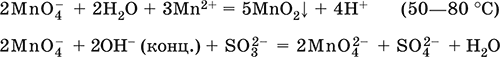
Получение – электролиз раствора K2MnO4 (см.).
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!