
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диоксид серы. Сульфиты
|
|
|
|
Диоксид серы SO2. Кислотный оксид. Бесцветный газ с резким запахом. Молекула имеет строение незавершенного треугольника [: S(O)2] (sр2‑гибридизация), содержит σ,π‑связи S=O. Легко сжижается, термически устойчивый. Хорошо растворим в воде (~40 л/1 л Н2O при 20 °C). Образует полигидрат, обладающий свойствами слабой кислоты, продукты диссоциации – ионы HSO3‑ и SO32‑. Ион HSO3‑ имеет две таутомерные формы – симметричную (некислотную) со строением тетраэдра [S(H)(O)3] (sр3‑гибридизация), которая преобладает в смеси, и несимметричную (кислотную) со строением незавершенного тетраэдра [: S(O)2(OH)] (sр3‑гибридизация). Ион SO32‑ также тетраэдрический [: S(O)3].
Реагирует со щелочами, гидратом аммиака. Типичный восстановитель, слабый окислитель.
Качественная реакция – обесцвечивание желто‑коричневой «йодной воды». Промежуточный продукт в производстве сульфитов и серной кислоты.
Применяется для отбеливания шерсти, шелка и соломы, консервирования и хранения фруктов, как дезинфицирующее средство, антиоксидант, хладагент. Ядовит.
Соединение состава H2SO3 (сернистая кислота) не известно (не существует).
Уравнения важнейших реакций:
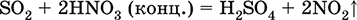
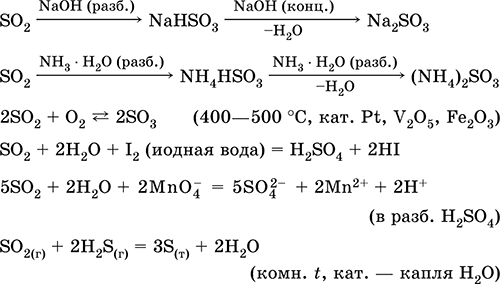
Растворение в воде и кислотные свойства:
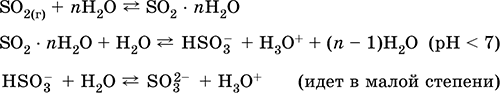
Получение: в промышленности – сжигание серы в воздухе, обогащенном кислородом, и, в меньшей степени, обжиг сульфидных руд (SO2 – попутный газ при обжиге пирита):
S + O2 = SO2 (280–360 °C)
4FeS2 + 11O2 = 2Fe2O3 + 8 SO2 (800 °C, обжиг)
в лаборатории – вытеснение серной кислотой из сульфитов:
BaSO3(т) + H2SO4 (конц.) = BaSO4↓ + SO2↑ + Н2O
Сульфит натрия Na2SO3. Оксосоль. Белый. При нагревании на воздухе разлагается без плавления, плавится под избыточным давлением аргона. Во влажном состоянии и в растворе чувствителен к кислороду воздуха. Хорошо растворим в воде, гидролизуется по аниону. Разлагается кислотами. Типичный восстановитель.
Качественная реакция на ион SO32‑ – образование белого осадка сульфита бария, который переводится в раствор сильными кислотами (НCl, HNO3).
Применяется как реактив в аналитической химии, компонент фотографических растворов, нейтрализатор хлора при отбеливании тканей.
Уравнения важнейших реакций:

Получение:
Na2CO3 (конц.) + SO2 = Na2SO3 + CO2↑
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 498; Нарушение авторских прав?; Мы поможем в написании вашей работы!