
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Принципы расчета химической эксергии
|
|
|
|
Система обладает эксергией, если она находится в неравновесном состоянии по отношению к окружающей среде. В зависимости от параметров, по которым существует неравновесность (температура, давление, химические потенциалы) можно выделить различные составляющие эксергии. Обычно выделяют термомеханическую и химическую эксергии системы. Первая обуславливается различием температуры и давления в системе и окружающей среде, а вторая различием химического состава и химических потенциалов в системе и окружающей среде. Расчет термомеханической составляющей может быть проведен строго исходя из законов термодинамики (вывод расчетных уравнений приведен в разделе 4) в то время как расчет химической составляющей затруднен по причине неравновесности самой окружающей среды, непостоянства ее химического состава и параметров Т, р. Поэтому при расчете химической эксергии необходимо использовать понятие об условных моделях окружающей среды (модель ОС) и реакции девальвации.
Расчет химической эксергии производится по реакции девальвации, которая является процессом обесценивания вещества до веществ отсчета окружающей среды. Впервые предложенный Шаргутом [3], метод реакции девальвации является основным способом расчета химической эксергии. Для проведения реакции девальвации обычно необходимо привлечение веществ отсчета из ОС (например, кислорода для сжигания). Затрачиваемая работа на их извлечение и приведение к концентрациям, необходимым по уравнению реакции девальвации, является концентрационной эксергией дополнительных веществ отсчета. Под общей концентрационной или просто концентрационной эксергией понимают сумму концентрационных эксергий всех веществ отсчета. Процесс девальвации вещества можно изобразить с помощью схемы девальвации. На рис. 5.1 приведена обобщенная схема девальвации произвольного вещества по Шаргуту [3]. В первом процессе температура и давление Т, Р вещества становятся равными Т0, Р0. Изменение эксергии в этом случае равно термомеханической эксергии вещества. Второй процесс соответствует реакции девальвации, в которой кроме вещества участвуют дополнительные вещества отсчета. Работа по их извлечению из ОС определяется в третьем процессе. В четвертом процессе полученные результирующие вещества отсчета разбавляются до их концентрации в окружающей среде. Например, углеводороды состава CxHy девальвируются до СО2 и Н2О, которые являются результирующими веществами отсчета. Необходимый для реакции сгорания кислород О2 извлекают в нужном количестве из ОС затрачивая работу. Уравнение девальвации для углеводорода CxHy имеет вид:
CxHy + (x+y)O2 ® x CO2 +y/2 H2O

Рис. 5.1: Обобщенная схема девальвации по Шаргуту.
Т,р - температура и давление вещества, Т0, Р0 - температура и давление ОС.
Эксергия соединения А с реакцией девальвации
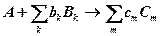
где Вк - дополнительные вещества отсчета,
Сm - результирующие вещества отсчета,
bk,cm - соответствующие стехиометрические коэффициенты, будет равна
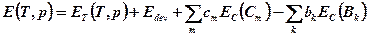
где 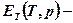 термомеханическая эксергия,
термомеханическая эксергия,
 - эксергия химической девальвации
- эксергия химической девальвации
 - концентрационная эксергия веществ отсчета.
- концентрационная эксергия веществ отсчета.
Шаргут предложил использовать в качестве ОС идеализированную модель окружающей среды, которая строится на следующих принципах:
1. Для каждого элемента из всех его соединений в природе выбирается
одно наиболее распространенное вещество отсчета, содержащее
этот элемент. Вещество отсчета должно быть наиболее
девальвированным, то есть обладать наименьшим значением
эксергии.
2. Совокупность всех веществ отсчета является условной окружающей
средой с определенным химическим составом.
3. Параметрами модели ОС являются температура Т0, давление р0 и
химический состав. Температура, давление и концентрации
веществ отсчета принимаются равными их средним значениям в
природной ОС.
4. Принятые таким образом параметры окружающей среды являются
условным нулевым уровнем отсчета для эксергии, а эксергия ОС
принимается равной нулю.
С усложнением модели ОС путем введения в нее гидросферы, написание реакций девальвации и расчеты по ней стали затруднительны. Поэтому используется также понятие стандартной эксергии простых веществ. Произведя расчет химических эксергий простых веществ в рамках выбранной модели ОС, присваиваются эти значения простым веществам как новый уровень отсчета. Тем самым изменяют принятое в химической термодинамике стандартное состояние. Энергия Гиббса в такой системе отсчета становится равной эксергии вещества. Формально, расчет ведут по формуле:



где 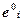 - стандартные значения эксергий простых веществ;
- стандартные значения эксергий простых веществ;
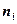 - число молекул (атомов) простых веществ в молекуле вещества.
- число молекул (атомов) простых веществ в молекуле вещества.
Такой подход к расчету эксергии упрощает процедуру расчета, так как значения стандартных эксергий простых веществ легко табулировать.
Схема девальвации веществ состава СaHbOcNdSe.
Обобщенное уравнение девальвации веществ состава СаНbOcNdSe имеет вид:

Схема девальвации представлена на рисунке 5.3, а расчетные соотношения для соответствующих процессов приведены ниже.
1. Расчет термической эксергии вещества
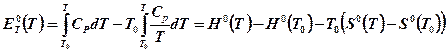 (5-1)
(5-1)
где Т0 = 298,15 К, Ср - теплоемкость СaHbOcNdSe.
2. Расчет эксергии девальвации.
 (5 -2)
(5 -2)
1. Расчет концентрационной эксергии дополнительных веществ отсчета
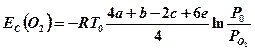 (5 -3)
(5 -3)
2. Расчет концентрационной эксергии результирующих веществ отсчета
 (5-4)
(5-4)

Рис.5.3. Схема девальвации веществ состава СаНbOcNdSe
Так как величины  ,
, 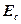 относятся к давлению
относятся к давлению 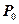 , то суммарное выражение эксергии вещества СаНbOcNdSe
, то суммарное выражение эксергии вещества СаНbOcNdSe
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 2198; Нарушение авторских прав?; Мы поможем в написании вашей работы!