
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота № 20 Кількісне визначення вмісту білків за нінгідриновим методом
|
|
|
|
Розділ 4. Використання фізико-хімічних методів в аналізі біооб’єктів
Контрольні питання.
Результати изначення заліза(III) сульфосаліцнловою кислотою
| № | Стандартний р-н Fe3+, мг | Вміст заліза, мг | ΔА | ΔА, контрольний р-н | m Fe3+, мг |
| 2,5 | 0,25 | А1/А3= | |||
| 5,0 | 0,5 | А2/А3= | |||
| 7,5 | 0,75 | А3/А3= | Ах/А3= | ||
| 10,0 | 1,0 | А4/А3= | |||
| 12,5 | 1,25 | А5/А3= | |||
| 15,0 | 1,5 | А6/А3= |
1. Опишіть оптимальні умови фотометричного визначення заліза у вигляді роданідного та сульфосаліцилового комплексу.
2. Яким чином підібрати світлофільтр для фотометричного визначення?
3. Які фактори впливають на величину молярного коефіцієнта поглинання?
4. Чому молярний коефіцієнт поглинання є найбільш об’єктивною характеристикою чутливості фотометричного методу?
Необхідні прилади і реактиви:
1.Фотоколориметр і кювети;
2.Мірні колби місткістю 25мл - 2 шт.;
3.Стандартний розчин гліцину, що містить 50мг гліцину у 1 мл;
4. 0,1% р-н нінгідрину в 95% ацетоні.
Принцип методу. В результаті взаємодії α-амінокислот з нінгідрином (трикетогідрінденом) утворюється забарвлена комплексна сполука. При нагріванні до 70○С α-амінокислоти окислюються нінгідрином та вступають в реакції окисного дезамінування з утворенням аміаку, диоксиду вуглецю та альдегіду, а нінгідрин відновлюється.
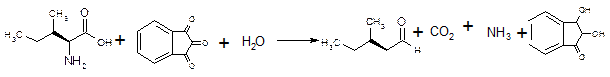 Відновлений нінгідрин, конденсується з аміаком та окисненим нінгідрином, утворюючи єнольну сполуку, що має синьо-фіолетове забарвлення.
Відновлений нінгідрин, конденсується з аміаком та окисненим нінгідрином, утворюючи єнольну сполуку, що має синьо-фіолетове забарвлення.

В присутності органічних розчинників (ацетон, етиловий спирт) можливе протікання побічного процесу з утворенням сполуки, що має в своєму складі радикал амінокислоти, і забарвлена вона у червоний, жовтий, голубий колір. Гліцин з нінгідрином має синьо-фіолетове забарвлення.

Хід роботи. В одну колбу на 25 мл вносять 20 розчину гліцину з концентрацією 50 мг/мл, доводять до мітки дистильованою водою, отримують стандартний розчин порівняння. В другу колбу вносять досліджуваний розчин з невідомим вмістом гліцину. В обидві колби додають по 10-15 крапель розчину нінгідрину, перемішують, нагрівають на протязі 5 хвилин при 700С, охолоджують доводять до риски дистильованою водою і через 30 хв спостерігають екстинкцію за допомогою фотоколориметру у кюветі з товщиною 10 мм при червоному світлофільтрі (750 нм). Як розчин порівняння використовують дистильовану воду. Потім проводять визначення оптичної густини в задачі. Знаходять невідому концентрацію гліцину в задачі за формулою:
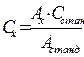
|
|
|
|
|
Дата добавления: 2015-06-28; Просмотров: 515; Нарушение авторских прав?; Мы поможем в написании вашей работы!