
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчеты для приготовления растворов
|
|
|
|
Пример. Приготовить р-р с массовой долей кислоты W = 0,09 из ледяной уксусной кислоты. Ледяной называют безводную кислоту т.к. она замерзает в льдоподобную массу при +17°С. Если в задании не указан объем, его выбирают условно. Пусть надо приготовить V (р-ра ук.к-ты) = 100мл. Справочные данные: ρ(лед. к-ты) = 1,050г/мл; W (укс.к-ты разб.) = 0,09; ρ (р-раСН3СООН) = 1,011 г/мл.
1. Масса раствора разбавленной кислоты: m(р-ра) = V × ρ(р-ра) = 100 × 1,011 = 101,1(г).2. Масса растворенного вещества в разбавленном растворе:m(р.в.) = m(р.в.) × ρ(р-ра) × W(р.в.) = 101,1 × 0,09 ≈9,1 (г)
m(р.в. в разбавленном растворе) = m(ледяной СН3СООН) = 9,1(г)3. Объем ледяной уксусной кислоты:V (лед. ук. к-ты) = 9,1/1,05 ≈ 8,7 (мл)4. Масса воды: m (воды)=101,1 – 9,1 = 92(г)Ответ: к 8,7л «ледяной» уксусной кислоты следует добавить 92 мл воды. Практически: 8,7 мл «ледяной» уксусной кислоты развести водой до объема 100 мл в мерной колбе.Иногда, если данные даны в массовых долях или процентном содержании, удобно использовать «правило креста». Слева записывают содержание растворенного вещ-ва в % (или в массовой доле). В середине – процентное содержание (массовую долю) растворенного вещ-ва в растворе, который следует приготовить. Справа записывают разность между большим и меньшим значением по диагонали (кресту). Полученные при вычитании данные означают массовые соотношения исходных растворов. Если участвует вода, то содержание растворенного вещ-ва в ней принимают за 0. Если участвует кристаллогидрат, то за содержание вещества в нем принимают процентное содержание безводной соли в кристаллогидрате.
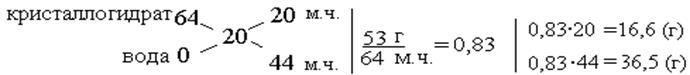
Следующая после «креста» запись означает определение массы, приходящейся на одну массовую часть, и далее масса, приходящаяся на 20 массовых частей и на 44 массовые части. Итак, для приготовления раствора следует взять 16,6 г кристаллогидрата и 36,5 г воды.
79.. Газы в процессе работ получают, собирают, хранят, сжимают, от них освобождают сосуды, создают вакуум, очищают от примесей, проводят операции в их атмосфере.Приборы для получения газов: 1) приборы для взаимодействия твердых веществ с жидкостью, подводимой к вещ-ву снизу, 2) приборы капельного действия, 3) приборы для взаимодействия жидкости с жидкостью, 4) приборы, в которых газ образ. при термич. разложении твердого вещ-ва.Распространенным прибором первой группы является аппарат Киппа. В колбу-реактор, вынув верхнюю воронку, или через тубус реактора загружают кусочки твердого реагента (цинка, мрамора). В верхнюю воронку аппарата через установленную хим. воронку заливают жидкий реагент при открытом кране верхнего тубуса. Оптимально, чтобы жидкость покрыла твердое вещество на 1–1,5 см. Верхняя воронка должна быть хорошо пришлифована к реактору. Кран верхнего тубуса закрывают. В результате под действием образующ. газа жидкость уходит из реактора в нижний полушар, а оттуда в верхнюю воронку.Если этот процесс происходит быстро - прибор герметичен. «Слабым звеном» прибора может быть пробка нижнего тубуса, через которую при демонтаже прибора выливают жидкость. Чтобы предотвратить выход газа через верхнюю воронку, ее закрывают предохранительной склянкой. Аппарат стоит в широком кристаллизаторе на случай протекания жидкости.Образующийся газ выпускают из колбы 5-10 минут для полного удаления воздуха из реактора.
Порядок демонтажа аппарата. Аппарат приподнимают и ставят на край широкого кристаллизатора. Наклонив в сторону от слива жидкости, расшатывающим движением открывают пробку нижнего тубуса и сливают жидкость. Из кристаллизатора жидкий реактив сливают в фарфоровую кружку, а оттуда в сосуд для хранения. Заливают в аппарат воду и покачивающим движением промывают твердый реагент. Обмывают внешнюю сторону аппарата. Слив воду, через нижний тубус, высыпают остатки тв. вещ-ва из верхнего тубуса. В ап-те Киппа получают водород, углекислый газ, сероводород, хлор, кислород, оксид азота (II), ацетилен.Сущ. простые аналоги - аппарат Кирюшкина, состоящий из пробирки, воронки, куда уходит жидкость при перекрывании зажимом хода газа. Кусочки твердого реагента закладываются на перегородку. Приборы капельного действия имеют капилляр, по которому жидкость поступает каплями в реакционный сосуд к твердому реагенту. Прибор может быть снабжен краном, через который прореагировавшая жидкость уходит, жидкий реагент не смешивается с продуктом реакции.Стандартный прибор для получения газа методом «твердое вещество-жидкость» и «жидкость – жидкость» в лаборатории состоит из колбы Вюрца, в которую закрепляется капельная (или делительная) воронка с краном. Для подогрева используются колбонагреватели или бани. Приборы для получения газов методом термического разложения вещества состоят из реактора, в качестве которого могут быть использованы реторта, круглодонная колба из термостойкого стекла, длинные пробирки, лодочки.При получении газа реактор связывают с системой предохранительных и поглотительных склянок и с сосудами для хранения или дальнейшего использования. Для предотвращ. растрескивания сосуда прим. кварцевое стекло или нагревают горло сосуда. Методы собирания газа. При собирании газа методом вытеснения воздуха пробирку-приемник держат вверх дном - газ легче воздуха и вниз дном - газ тяжелее воздуха. Чтобы определить наполнился ли сосуд газом, следует поднести бумажку с индикатором, лучинку и пр., в зависимости от хим. свойств газа. Собирание методом вытеснения воды. В сосуд набирают воды и опрокидывают его, закрыв отверстие пальцем или пробкой, в кристаллизатор с водой, под водой снимают пробку и подводят в отверстие газоотводную трубку с газом. Газ вытесняет воду и собирается в сосуде-приемнике. Если пузырьки газа появились вокруг заполняемого сосуда – значит, он полностью заполнен.
Очистка и осушка газов. Выбор способа очистки газов зависит от природы газов и его примесей. Для сушки газов применяют конц. серную кислоту, хлорид кальция, гидроксид натрия, натронную известь, оксид фосфора (V), силикагель. Сущность - газ пропускают через слой жидкости или твердого осушителя. При этом газ должен свободно без препятствия проходить через осушители. Скорость подачи газа определяется экспериментально. Мокрая очистка газов осущ. с помощью жидких реагентов. В качестве посуды используют промывные склянки Тищенко, Дрекселя где контакт газа с жидкостью короткий. Промывная жидкость наливается таким образом, чтобы газоотводная трубка была опущена на 1-2 см в жидкость, для уменьшения сопротивления потоку газа. В качестве жидкого осушителя применяется конц. серная кислота для газов, к-рые с ней не реагируют. Для сухой очистки газов прим. тверд. поглотители и сосуды разнообразной конструкции: пробирки или U-образные сосуды, склянки Тищенко и др. Их наполняют кристаллическими поглотителями. Сухую очистку применяют для: азота, кислорода, водорода, очищают их от воды, сероводорода, хлористого водорода и других примесей кислотного характера. Хранение газов. Небольшие объемы газы хранят в колбе, газовой пипетке. Газы объемом от 1 до 5 л хранят в аспираторах и газометрах. Большие количества хранят в газгольдерах или в баллонах. Принцип действия всех газометров – газ вытесняется из нижней склянки, в которой он хранится, жидкостью из воронки или верхней склянки.Газометр состоит из сосуда, в котором газ хранится и верхней воронки с краном. Сосуд, в котором хранится газ, имеет два тубуса, верхний с краном, нижний с краном или пробкой. Газометр заполняется водой. Проверяют герметичность при закрытых кранах без пробки из нижнего тубуса. Если жидкость не выливается, прибор герметичен. В газометре можно хранить газы, не образ. с воздухом взрывоопасных смесей и не реагир. с водой. Заправка газометра: подводят газоотводную трубку от реактора в нижний тубус. При наполнении сосуда газом, пробку закрывают. Для использ. газа, открывают кран верхнего сосуда, вытекающая из верхней воронки вода вытесняет газ в незакрытый кран. Работа в атмосфере газов. Для восстановления металлов из их оксидов применяется H2, котор. пропускается через систему очистки, направляется в трубку с веществом в лодочке. Трубка закрепляется в трубчатой печи. Подача газа регулир. по скорости пузырьков в системе очистки.Работа в атмосфере углекислого газа необходима для вещ-в, которые могут реагировать с кислородом воздуха. Для упаривания в атмосфере CO2, его пропускают через р-р упаривающейся жидкости при нагревании на плитке. Газ пропускается способом барботирования. В этом случае газ играет роль инертного газа, он также уносит пары воды. Сушка в атмосфере углекислого газа. Для предотвращения окисления во время сушки некоторых веществ над ним пропускают углекислый газ. Для этого стеклянную трубку с веществом на фильтре закрепляют над плиткой в наклонном положении, чтобы стекали капли воды. Следует добиться, чтобы вода полностью испарилась со стекла, так как при изымании вещества из трубки, имеется возможность его увлажнения.
Получение газов. Получение водорода. Водород получают в лаборатории взаимодействием металлов с кислотами. Используют гранулированный цинк и 20 –30%-й р-р серной кислоты.Высокой степени чистоты получается водород при действии щелочи (10-15%-й раствор) на алюминий (проволока, фольга). Реакцию удобнее проводить в колбе Вюрца, приливая из капельной воронки воду.Для большого количества применяют метод электролиза воды – Получение кислорода. В лаб. кислород получ. в небольших кол-вах при разложении кристаллич. перманганата калия. В больших кол-вах получают в колбе Вюрца с кусочками диоксида марганца, приливая в нее из делительной воронки конц. р-р пероксида водорода. Кислород можно получ. электролизом воды. Получение углекислого газа. Углекислый газ получают в приборе для капельного метода и в аппарате Киппа. В качестве твердого реагента беруткусочкимрамора.К нему через верхний шар наливают разбавленную (1:1) НСl Получение хлора. Газ ядовитый, тяга!Заранее готовятся нейтрализ. р-ры – сульфита калия, щелочи или соды. Хлор получают в колбе для капельного метода. В колбу Вюрца помещают кристаллический перманганат калия, увлажняют его водой, приливают по каплям конц. HCl. Перманганат калия явл. сильным окислителем, реакция идет бурно; Реакцию проводят на холоде, при нагревании содержание примесей увелич. Установка для очистки состоит из промывалок с водой и конц. серной кислоты, предохранительной склянки. Получение хлористого водорода. Газ ядовитый, тяга! Реагенты – кристаллический хлорид натрия и конц. серная кислота. Прибор – для капельного метода получения газов. Для очистки газ пропускают через колонку с битым стеклом, смоченным конц. серной кислотой для улавливания брызг ее из исходного реагента. Получение сернистого газа. Газ ядовитый, тяга! Реагенты – кристаллический сульфит натрия и конц. серная кислота. Прибор – для капельного способа получения газов. Нейтрализующее вещество – раствор щелочи. Освобождение сосудов от газов. Чтобы освободить сосуд от газов следует наполнить его водой доверху под тягой, при этом газ вытесняется водой в атмосферу вытяжного шкафа. Если газ растворяется в воде, то часть его вытесняется, а часть растворяется в воде, после этого следует жидкость нейтрализовать. Можно заполнять сосуд с газом соответствующей нейтрализующей жидкостью.Отсюда важный принцип безопасности: сосуды после пребывания в них летучих кислот (соляной, азотной и др.) следует ополаскивать под тягой, наполнив их водой или нейтрализующей жидкостью доверху.
77. Лабораторные операции. Для нагревания используют чаще всего электроплитки с закрытым нагревательным элементом. Плитки с открытой спиралью применяют, когда нет опасности попадания на спираль нагреваемого вещ-ва. На электроплитке можно нагревать тонкостенную посуду (термич. стойкую). Для упаривания, когда требуется меньшая t, исп. асбестовые сеточки. Нагревание проводят на водяных банях когда необх. вести длительное нагревание при t, не превыш. 100°С, в качестве бани можно исп. термически стойкие стаканы, жестяные упаковки из-под консервированных продуктов. Для достижения более высокой t нагревание ведется на песочной бане. Для получения t 600-1000°С – муфельная печь. Часто для нагревания исп. спиртовки. Исп. в спиртовках этиловый спирт. Уровень спирта не менее 2/3 высоты резервуара, при меньшей высоте - образование взрывоопасной газовоздушной смеси. Порядок зажигания спиртовки: снять колпачок, поправить фитиль просушить руки, зажечь спичку и поднести к фитилю.На открытом пламени можно нагревать реактивы в пробирках и круглодонных колбах, нельзя нагревать выпарительные чашки, толстостенную посуду из-за неравномерного нагревания. Пробирку следует сначала прогреть по всей длине, а потом нагревать реактив; недопустимо нагревать пробирку выше жидкости.
Колбу и пробирку можно высушить, держа их высоко над пламенем вверх дном, а лучше над электрической плиткой, всё время поворачивая сосуд и вдувая в него воздух с помощью груши. Прокаливание. Прим-ют для обезвоживания или разложения тв. вещ-ва. Вещ-во помещают в фарфоровый тигель, который ставят в фарфоровый треугольник, положенный на кольцо штатива. Тигель нагревают небольшим пламенем горелки, пламя постепенно увеличивают. После прокаливания тигель охлаждают на треугольнике или, несколько остывший, переносят в эксикатор с пом. пинцета. Если прокаливание проводят с целью разложения тв. вещ-ва и получения газообразного продукта, то прокаливаемое вещ-во помещ. в пробирку, снабженную газоотводной трубкой. Конец тр. Опускаю в приемник для газа. Охлаждение. Охлаждение можно вести холодной водой или в банях: водяных, ледовых солевых Рабочий раствор следует время от времени помешивать для равномерного охлаждения. Охлаждение не должно быть резким – выпадение загрязн. осадков в процессе выделения вещ из р-ра. Холодильники – приборы для охлаждения и конденсации паров, обр. при нагревании различных вещ-в. Применяют при перегонке, экстракции и др. процессах. Поступающие в холодильник пары, соприкасаясь с холодной поверхностью, охлаждаются и конденсируются. Если охлаждаемые пары поступают в холодильник сверху, а конденсат стекает в другой сосуд (приемник), то холодильник нисходящий. Если пары поступают снизу, а конденсат стекает в ту же колбу, где происходит кипение, холодильник обратный. По строению трубки холодильники бывают: шариковые; прямотрубочные (Либиха); холодильники со змеевиковым охлаждением. При выборе холодильника учитывают его производительность — кол-во паров, которое в нем будет конденсироваться в единицу времени. Производительность холодильника тем выше, чем больше поверхность теплообмена и время контакта паров с холодной поверхностью. Наименьшей производительностью при равных размерах обладают холодильники Либиха. Они используются в основном при конденсации паров высококипящих жидкостей при небольших расходах. Эффективны холодильники со змеевиковым охлаждением: скорость движения паров в них очень мала, а поверхность охлаждения значительна. Сушка твердых веществ. Осадки, снятые с фильтра, содержат некоторое кол-во растворителя. Удалить можно сушкой.В процессе сушки вещ-ва не должны разлагаться или претерпевать какие-либо другие хим. превращения. Сушка твердых веществ проводиться на воздухе при комнатной t и при нагревании в сушильном шкафу. При комнатной t твердые вещ-ва сушат на фарфоровых и глиняных тарелках или на фильтр. бумаге. В сушильном шкафу сушка твердых веществ производится на часовых стеклах, фарфоровых противнях, в фарфоровых чашках или бюксах. При этом t в сушильном шкафу должна быть значительно ниже t плавления вещ-ва. Запрещается сушить в сушильном шкафу на бумаге. Многие органич. соединения при высокой t разлагаются и подвергаются окислению. Такие соединения сушат при разрежении в лаб. вакуум-сушильных шкафах. Для сушки широко используются инфракрасные лампы.Сушку можно проводить в присутствии вещ-в, поглощ. пары удаляемого растворителя. Для этой цели широко применяются эксикаторы и, в частности, вакуум-эксикаторы. Для связывания паров воды или спирта применяют едкий натр, хлористый кальций, фосфорный ангидрид, серную кислоту. Перед тем как начать откачивать воздух из эксикатора, его необходимо обернуть полотенцем или закрыть матерчатым колпаком, чтобы в случае разрыва эксикатора избежать неприятных последствий. Газоотводную трубку присоед. с помощью резинового вакуум-шланга к вакуумной линии и осторожно открывают кран. Через время кран закрывают и разъединяют газоотводную трубку с вакуумной линией.
Для сушки в вакууме при повышенной температуре весьма пригодна «пистолетная» сушилка. В колбу налив. жидкость, ее парами обогревают корпус сушилки, в которую помещают лодочку с осушаемым вещ-ом. В колбе находится осушающее вещество (адсорбент). Сушка в атмосфере углекислого газа. Для предотвращения окисления во время сушки некоторых веществ над ним пропускают углекислый газ. Для этого стеклянную трубку с веществом на фильтре закрепляют над плиткой в наклонном положении, чтобы стекали капли воды. Сушка жидкостей. Присутствие воды при нагревании может привести к разложению перегоняемых вещ-в. Наличие воды в р-ре при перегонке ведет к появлению новых фракций, что связано с потерей основного вещ-ва. Широко распространены методы сушки жидкостей при помощи осушающих веществ, которые связывают воду. Основное требование к осушающим вещ-вам - не должны взаимодействовать ни с растворителем, ни с растворенными в нем веществами. Исп. Силикагели, H2SO4, цеолиты. Сушка газов. Прим. конц. серную кислоту, хлорид кальция, гидроксид натрия, натронную известь, оксид фосфора (V), силикагель. Сущность технической стороны сушки газа в том, что газ пропускают через слой жидкости или твердого осушителя. При этом газ должен свободно без препятствия проходить через осушители. Скорость подачи газа определяется экспериментально и визуально определяется по скорости пузырьков в поглотительных склянках.
|
|
|
|
|
Дата добавления: 2015-06-28; Просмотров: 505; Нарушение авторских прав?; Мы поможем в написании вашей работы!