
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водород имеет один неспаренный электрон на s- орбитали
|
|
|
|
Селен имеет два неспаренных электронов на p- орбитали
ЗАДАЧА 4. Вычислите величины ∆H0298, ∆S0298 и ∆G0298 для данной реакции (необходимые для расчетов данные см. в Приложении). Объясните знак изменения энтальпии и энтропии. Возможна ли данная реакция при стандартных условиях?
4H2(г) + 2NO2(г) ↔ 4H2O(г) + N2(г)
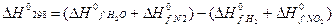
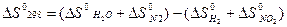
∆G0298 = ∆H0298 – T * ∆S0298
∆H0298= (4*(-241,81) + 0) – (4*0+2*34,19)=-1035,62 кДж/моль
∆S0298= (4*188,72+191,5)-(4*130,52+2*240,06) =-55,82 Дж/моль*K=-0,05582 кДж/моль*K
∆G0298 =-1035,62 кДж/моль– 298K*(-0,05582 кДж/моль*K) =-1018,9 кДж/моль
1)Мы получили, что ∆H0298 <0, значит реакция протекает с выделением тепла
2) ∆S0298<0 свидетельствует о возрастании упорядоченности системы в ходе реакции.
3) ∆G0 298 <0, значит данная химическая реакция принципиально осуществима при стандартных условиях,самопроизвольна.
ЗАДАЧА 5. Для той же pеакции: 4H2(г) + 2NO2(г) ↔ 4H2O(г) + N2(г) 1) составьте кинетическое уpавнение; 2) составьте выpажение для константы pавновесия; 3) вычислите, во сколько pаз изменится скоpость pеакции пpи заданных изменениях: а) темпеpатуpы, б) общего давления (пpи изменении объема системы) и в) концентpаций pеагентов; 4) укажите, как необходимо изменить внешние паpаметpы (темпеpатуpу, общее давление, концентpации pеагентов), чтобы сместить pавновесие впpаво. Все необходимые для pешения данные пpиведены в таблице (темпеpатуpный коэффициент – γ; в тpех последних столбцах указано, во сколько раз увеличили концентрацию первого реагирующего вещества, второго реагирующего вещества и общее давление в системе).
| Поpядок по 1-му pеагенту | Поpядок по 2-му pеагенту | γ | T 1, K | T 2, K | 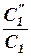
| 
| 
|
| 3,2 |
1)Кинетическое уравнение

2) Константа равновесия
Кр= 
3) а) 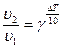 ,
, 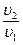 =
= 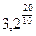 , значит
, значит 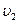 =10,24
=10,24 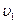 значит скорость реакции увеличится в 10,24 раза
значит скорость реакции увеличится в 10,24 раза
б) При повышении давления в 2 раза (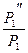 ) скорость реакции возрастет в 22= 4раза.
) скорость реакции возрастет в 22= 4раза.
в) При повышении концентрации первого реагента в 2 раза (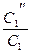 ) скорость реакции возрастет в 2 раза.
) скорость реакции возрастет в 2 раза.
При повышении концентрации второго реагента в 2 раза ( ) скорость реакции возрастет в 4 раза.
) скорость реакции возрастет в 4 раза.
для смещения равновесия слева направо в рассматриваемой в задаче системе обратимых химических реакций, в которой прямая реакция происходит с выделением тепла (DH < 0) и уменьшением количеств газообразных веществ (из 6 моль газов (4H2 и 2NO2) в результате реакции образуется 5 моль газообразных продуктов(4H2O и N2)), НЕОБХОДИМО:
n - температуру понизить
n - давление понизить
n - концентрацию исходных веществ 4H2 и 2NO2 повысить
n - концентрацию продуктов прямой реакции 4H2O и N2 понизить
ЗАДАЧА 6. Пpоизведите необходимые вычисления и найдите недостающие величины, обозначенные знаком "?" в стpоке таблицы (все pаствоpы – водные).
| Растворенное вещество | Масса растворенного вещества, г | Масса растворителя, г | Объем раствора, мл | Плотность раствора, г/см3 | Массовая доля, % | Мольная доля, % | Молярная концентрация, моль/л |
| NaOH | 38,75 | 38,75 | 50,6 | 1,53 | 49,5 | 19,2 |
1) ω(массовая доля)=(m(раств.вещ-ва)/m(рас-ра))*100%
m(рас-ра)=m(в-ва)+m(рас-ля)
пусть m(вещ-ва)=x, тогда ω =(x/(x+m(рас-ля)))*100%
0,5=x/(x+38,75)
=>x=38,75, значит m(в-ва)=38,75 г, m(рас-ра)=38,75 г+38,75 г=77,5 г
2) V(р-ра)=m(рас-ра)/ ρ (рас-ра)
V(рас-ра)=77,5г/1,53г/см3=50,6 см3 1 см3=1мл
3) x  =n(вещ-ва)/n(рас-ра)*100%
=n(вещ-ва)/n(рас-ра)*100%
n(вещ-ва)=m(вещ-ва)/M(NaOH) n(рас-ра)=m(рас-ра)/M(NaoH)
n(вещ-ва)=38,75 г:40 г/моль=0,96 моль n(рас-ра)=77,5 г:40 г/моль =1,94 моль
x  =0,96 моль/1,94 моль*100%=49,5%
=0,96 моль/1,94 моль*100%=49,5%
4) С 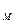 =n(вещ-ва)/V(рас-ра)
=n(вещ-ва)/V(рас-ра)
С 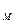 =0,96 моль/0,05 л = 19,2 моль/л
=0,96 моль/0,05 л = 19,2 моль/л
ПРИЛОЖЕНИЯ
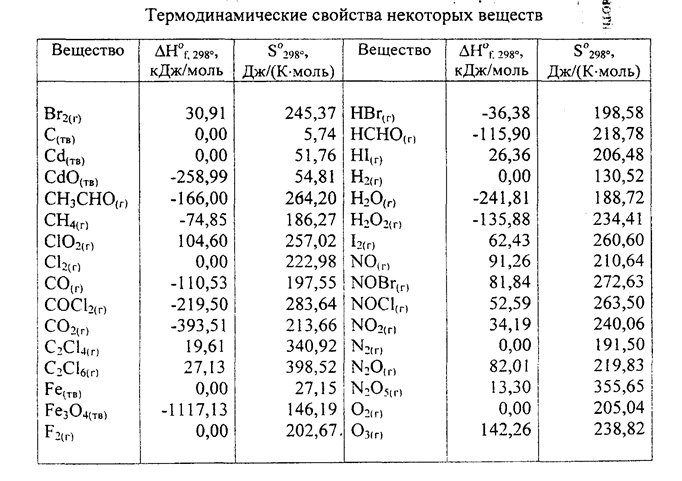
|
|
|
|
|
Дата добавления: 2015-06-29; Просмотров: 1092; Нарушение авторских прав?; Мы поможем в написании вашей работы!