
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительно-восстановительных реакций. Реакции окисления-восстановления могут протекать в различных средах: в кислой (избыток Н+ - ионов )
|
|
|
|
Влияние среды на протекание
Реакции окисления-восстановления могут протекать в различных средах: в кислой (избыток Н+ - ионов), нейтральной (Н2О) и щелочной (избыток гидроксид – ионов ОН-). В зависимости от среды может измениться характер протекания реакции между одними и теми же веществами. Среда влияет на изменение степеней окисления атомов. Рассмотрим взаимодействие перманганата калия с сульфитом калия в зависимости от pH среды.
Реакции в кислой среде
5K2S+4O3 + 2KMn+7O4 + 3H2SO4 = 6K2S+6O4 + 2Mn+2SO4 + 3H2O
электронный баланс
| Mn7+ + 5ē = Mn2+ | |
| S4+ – 2ē = S+6 |
метод полуреакций
| MnO4- + 8H+ + 5ē = Mn2+ + 4H2O | |
| SO32- + H2O – 2ē = SO42- + 2H+ |
–––––––––––––––––––––––––––––––––––––––––––––––––––
2MnO4- + 16H+ + 5SO32- + 5H2O = 2Mn2+ + 8H2O + 5SO42- + 10H+
или 2MnO4- + 6H+ + 5SO32- = 2Mn2+ + 3H2O + 5SO42-
Фиолетовый раствор KMnO4 обесцвечивается при добавлении раствора K2SO3.
Реакции в нейтральной среде
3K2S+4O3 + 2KMn+7O4 + H2O = 3K2S+6O4 +2Mn+4O2¯ + 2KOH
электронный баланс
| S4+ – 2ē = S6+ | |
| Mn7+ + 3ē = Mn4+ |
метод полуреакций
| MnO41- + 2H2O + 3ē = MnO2 + 4OH- | |
| SO32- + 2OH- - 2ē = SO42- + H2O |
–––––––––––––––––––––––––––––––––––––––––––––––––––
2MnO4- + 4H2O + 3SO32- + 6OH- = 2MnO2 + 8OH- + 3SO42- + 3H2O
или 2MnO4- + H2O + 3SO32- = 2MnO2 + 2OH- + 3SO42-
Фиолетовый раствор KMnO4 после окончания реакции обесцвечивается и наблюдается выпадение бурого осадка.
Реакции в щелочной среде
K2S+4O3 + 2KMn+7O4 + 2KOH = K2S+6O4 +2K2Mn+6O4 + H2O
электронный баланс
| S4+ – 2ē = S6+ | |
| Mn7+ + 1ē = Mn6+ |
метод полуреакций
| SO32- + 2OH- - 2ē = SO42- + H2O | |
| MnO41- + ē = MnO42- |
–––––––––––––––––––––––––––––––––––––
SO32- + 2OH- + 2MnO4- = SO42- + H2O + 2MnO42-
Фиолетовый раствор KMnO4 превращается в зеленоватый раствор K2MnO4.
Схематически эти изменения можно представить
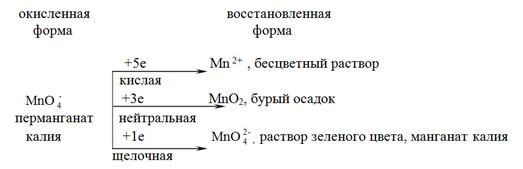
Перманганат калия называют минеральным «хамелеоном».
Реакции с дихроматом калия в качестве окислителя. Хром в своих соединениях имеет наиболее характерные степени окисления +6 и +3. В первом случае соединения хрома проявляют свойства окислителей, во втором восстановителей. В кислой среде ионы 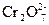 – сильные окислители, они восстанавливаются до соединений Cr3+. В щелочной среде ионы [Cr(OH)6]3- окисляются до ионов
– сильные окислители, они восстанавливаются до соединений Cr3+. В щелочной среде ионы [Cr(OH)6]3- окисляются до ионов 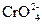 . Наблюдается изменение окраски реакционной массы с желто-оранжевого цвета до зеленого или фиолетового. Схематически эти изменения можно представить
. Наблюдается изменение окраски реакционной массы с желто-оранжевого цвета до зеленого или фиолетового. Схематически эти изменения можно представить
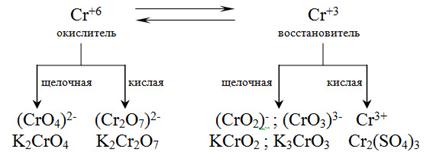
В зависимости от реакции среды имеют место переходы
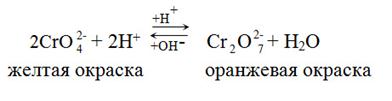
Реакции в кислой среде.
K2Cr2+6O7 + 3H2S-2 + 4H2SO4 = K2SO4 + Cr2+3(SO4)3 + 3S0 + 7H2O
электронный баланс
| 2Cr6+ + 6ē = 2Cr3+ | |
| S2- - 2ē = S0 |
метод полуреакций
| Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O | |
| H2S0 - 2ē = S0 + 2H+ |
––––––––––––––––––––––––––––––––––
Cr2O72- + 8H+ + 3H2S = 2Cr3+ + 7H2O + 3S0
K2Cr2+6O7 + 6Fe+2SO4 + 7H2SO4 = 3Fe2+3(SO4)3 + K2SO4 + Cr2+3(SO4)3 + 7H2O
электронный баланс
| 2Cr6+ + 6ē = 2Cr3+ | |
| Fe2+ – ē = Fe3+ |
метод полуреакций
| Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O | |
| Fe2+ - ē = Fe3+ |
–––––––––––––––––––––––––––––––––––––
6Fe2+ + Cr2O72- + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
K2Cr2+6O7 + 14HCl- = 3Cl20 + 2KCl + 2Cr+3Cl3 + 7H2O
электронный баланс
| 2Cr6+ + 6ē = 2Cr3+ | |
| 2Cl- – 2ē = Cl20 |
метод полуреакций
| Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O | |
| 2Cl1- - 2ē = Cl20 |
–––––––––––––––––––––––––––––––––––
Cr2O72- + 6Cl- + 14H+ = 2Cr3+ + 3Cl20 + 7H2O
Реакции в щелочной среде. Для создания щелочной среды применяют растворы гидроксида калия или натрия. В результате реакции, вновь образующиеся анионы кислотных остатков взаимодействуют с металлом среды и образуют соли.
+3 0 +6 -1
NaCrO2 + Cℓ2 + NaOH = Na2CrO4 + NaCℓ + H2O
восстановитель окислитель среда
метод полуреакций
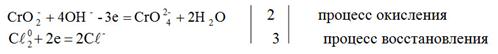
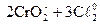 + 8OH– =
+ 8OH– = 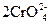 + 4H2O + 6Cℓ-
+ 4H2O + 6Cℓ-
или
2NaCrO2 + 3Cℓ2 + 8NaOH = 2Na2CrO4 + 6NaCℓ + 4H2O.
Реакции в нейтральной среде.
Fe+2(OH)2 + O20 + H2O = Fe+3(OH)3
восстановитель окислитель среда
электронный баланс

4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 1622; Нарушение авторских прав?; Мы поможем в написании вашей работы!