
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рост пленок. Эпитаксия
|
|
|
|
Лекция №8
Поскольку реальная толщина пленок во многих случаях больше, чем высота купола критических и сверхкритических зародышей то необходимо рассматривать не только образование, но и развитие (рост) пленки после того, как она стала сплошной, т. е. после исчезновения островковой структуры. При этом следует определить: 1) степень влияния механизма образования зародышей на дальнейшую структуру пленки, а также на возникновение границ зерен, дефектов структуры: упаковки, двойниковых структур, вакансий, дислокаций и др.; 2) зависимость изменения или повторения образовавшейся структуры от механизма роста пленок и различных параметров состояния; 3) способы влияния на изменение структуры пленки с целью улучшения ее электрофизических свойств.
Эпитаксией называется направленные рост одного кристаллического вещества на поверхности другого кристалла в случае, если формирующийся слой является в кристаллографическом отношении естественным продолжением кристаллической решетки подложки и включает в себя все ее несовершенства.
Эпитаксиальная пленка когерентна со структурой пластины, т. с. повторяет эту структуру. Такая пленка может «наследовать» или «залечивать» дефекты пластины в зависимости от условий осаждения и ее обработки.
В зависимости от главного признака, положенного в основу процесса, различают гомо-, гетеро-, и хемоэпитаксии.
Гомоэпитаксия (автоэпитаксия) – процесс ориентированного наращивания вещества на собственной подложке. В этом случае физическая граница между подложкой и эпитаксиальным слоем отсутствует, отличие лишь в содержании и типе примесных атомов.
Гетероэпитаксия – процесс ориентированного наращивания вещества, отличающегося по составу от вещества подложки. В данном процессе имеет место кристалло-химическое взаимодействие срастающихся фазс образованием переходного эпитаксиального слоя.
При увеличении числа слоев гетероэпитаксия сменяется гомоэпитаксией.
Хемоэпитаксия - процесс ориентированного наращивания вещества, в результате которого образование новой фазы происходит при химическом взаимодействии вещества подложки с веществом,поступающим из внешней среды. При этом формирующийся хемоэпитаксиальный слой отличается по составу как от вещества подложки так и от вещества поступающего на ее поверхность.
Переходный эпитаксиальный слой (ПС) – промежуточная область между двумя срастающимися фазами, структура и состав которой определяются характером физико-химического взаимодействия этих фаз.
Как уже было сказано после того как получен первый сплошной слон пленки, следующий слой формируется независимо от структуры пластины. Рост отдельного агрегата на атомарном уровне может быть как эпитаксиальным, так и неэпитаксиальным. Для анализа механизма роста пленки необходимо воспользоваться моделью образования куполообразного зародыша, описанной ранее.
Согласно уравнению (213) свободная энергия образования критического зародыша
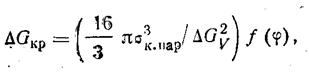
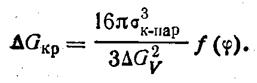 (223)
(223)
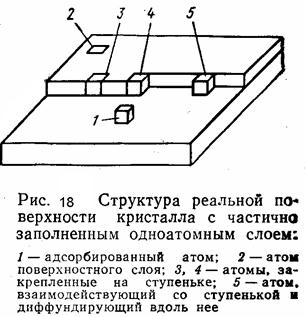
При осаждении пленки на предыдущий слой того же материала можно принять φ = 0. Тогда f (φ) =0 и ∆GKp = 0. Следовательно, энергетический барьер отсутствует. Поэтому конденсирующиеся атомы на поверхности пленки непосредственно встраиваются в структуру растущего слоя. В этом случае классическая модель образования зародышей макроскопических размеров не применима к образованию микроскопических (например, двухатомных или трехатомных) агрегатов. После возникновения на пластине сплошной пленки ее рост следует рассматривать с позиций роста кристаллов. Поверхность кристалла никогда не бывает идеально гладкой. На ней всегда имеются различные выступы, ямки, островки и другие неоднородности структуры (рис. 18 ). Механизм роста пленки включает в себя адсорбцию атомов из паровой фазы (преимущественно на гранях кристалла), поверхностную диффузию к ступеньке, взаимодействие со ступенькой, диффузию вдоль ступеньки и достраивание ступеньки. В зависимости от того, какое положение занимает адсорбированный атом на поверхности кристалла, число атомов, окружающих его, различно. Поэтому различна и энергия связи его с поверхностью кристалла, а следовательно, и энергия активации поверхностной диффузии.
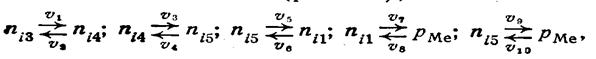 Условия равновесия, которые существуют между различными положениями атомов (рис. 18 ), таковы:
Условия равновесия, которые существуют между различными положениями атомов (рис. 18 ), таковы:
(224)
где пi1, ni2, ni3, ni 4 равновесные концентрации атомов соответствующего типа; pMe — давление пара осаждаемого компонента; υ1, υ2,… υ10 — скорости движения атомов.
Скорости v5—v10, влияющие на рост пленки, можно найти следующим образом:
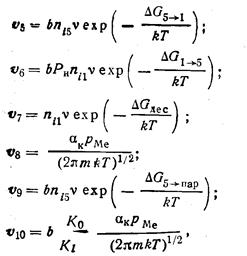
(225)
где b — длина ступеньки на единицу площади; v ≈10 13c-1 — частота колебаний атомов, находящихся на поверхности пленки; ∆G1→5— свободные энергии диффузии атомов при переходе из положения 1 в положение 5 и обратно; Рн — вероятность данного направления движения атомов при их миграции по поверхности пленки (для плотно упакованных кристаллов Pн=1/6); К0, Kl — число позиций атомов на единичной поверхности и длине ступеньки.
Таким образом, анализ роста пленки сводится к выявлению преобладающей стадии роста в тех или иных задаваемых условиях. Для случая, когда преобладает скорость поверхностной диффузии u 6, а скоростью диффузии вдоль ступеньки u4 можно пренебречь, уравнение диффузии для адсорбированных атомов примет вид
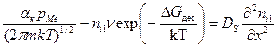 (226)
(226)
где Ds — коэффициент поверхностной диффузии; х — координата движения частицы.
Выражение (226) является кинетическим уравнением роста пленок.
Анализ роста монокристаллических (эпитаксиальных) пленок позволяет выявить кроме первичных дефектов структуры, вызванных условиями зарождения, и вторичные Дефекты, появляющиеся в процессе роста,— дислокационные петли, дефекты упаковки и точечные дефекты. Часто встречающимися дефектами в пленках являются дислокации. Концентрация дефектов условно характеризуется плотностью дислокаций, измеряемой их числом на 1 см2. Эта величина в эпитаксиальных пленках металлов достигает нередко значений 1010—1011 см2. В полупроводниковых эпитаксиальных пленках, используемых в производстве ИМС, плотность дислокаций составляет 10—104 см-2.
Причины появления дислокаций различны. Пленки формируютсяв процессе осаждения. Ранее осажденные слои могут покрываться последующими до того, как будет достигнуто термическое равновесие с предыдущим слоем. При этом в слой может попадать, большое число вакансий. Процесс усугубляется, если температура пластин низкая. В этом случае тепловой энергии (конденсации) может не хватить для того, чтобы обеспечить миграцию атомов по поверхности. Поэтому атомы будут оставаться в тех местах, куда они попали при соударении с поверхностью. Поскольку их распределение носит случайный характер, они будут вносить разупорядоченность в структуру осаждаемой пленки. Степень разупорядоченности зависит от наличия примесей в пленке и на ее поверхности, а также от неоднородных поверхностных свойств предыдущего слоя, низкой температуры конденсации и т. п.
Рассмотрим отношение скорости образования зародышей v3l некоторой эпитаксиальной (благоприятной) ориентации, характеризующейся контактным углом φi, к скорости образования зародышей неэпитаксиальной (неблагоприятной) ориентации, характеризующейся углом φ2 :
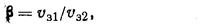 |
 (227)
(227)
где β — коэффициент благоприятной ориентации.
Существует множество неблагоприятных ориентаций, поэтому условие эпитаксиального образования зародышей выражается как
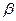 >>1 (228)
>>1 (228)
Скорость роста пленки определяется произведением числа единичных адсорбированных атомов n адс2πrкр a sinφ, примыкающих к зародышу, на частосту диффузионного перескока 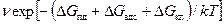 :
:
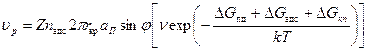 (229)
(229)
где ап — расстояние между позициями зародышей на пластине.
Для заданных технологических условий уравнение скорости осаждения имеет вид
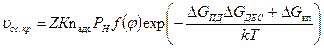 , (230)
, (230)
где vос-кр — скорость осаждения при критических параметрах.
Свободные энергии десорбции, поверхностной диффузии и конденсации не зависят от углаφ: они одинаковы для зародышей любого типа, Поэтому
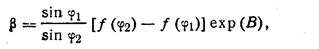 (231)
(231)
где 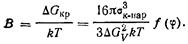
Для эпитаксиальной ориентации σк-пл меньше, чем для неэпитаксиальной, следовательно, 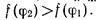
Рассмотрим зависимость коэффициента р от температуры пластины Т. С ростом температуры ∆GV уменьшается быстрее, чем увеличивается Т и значение В растет. Соответственно возрастает и β, что благоприятствует эпитаксии. Кроме того, поверхностная диффузия, увеличивающаяся с ростом температуры, способствует переходу атомов в состояния с меньшей свободной энергией. Эпитаксиальному росту пленки соответствует минимум свободной энергии.
Зависимость β от ∆GV можно получить, продифференцировав (231):
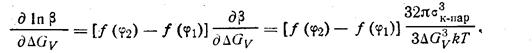 (232)
(232)
По мере увеличения ∆GV значение р уменьшается тем быстрее, чем меньше Т.
Температурная зависимость β=f(T), полученная при рассмотрении модели куполообразного зародыша, в общем виде справедлива для любой другой модели осаждения эпитаксиальных. слоев из пара. Только при химическом осаждении из парогазовой смеси, могут наблюдаться другие закономерности.
Химический рост эпитаксиальных пленок
В предыдущих параграфах были рассмотрены процессы образования и роста пленок при испарении и конденсации согласно термодинамической теории Гиббса — Фольмера, справедливой для степени перенасыщения, не превышающей 108. При испарении тугоплавких металлов (W, Mo, Re, V) степень перенасыщения достигает значений 1030—1040; размеры критических зародышей, рассчитанные по уравнению (200), соответствуют размерам одного атома и меньше, что противоречит физическому смыслу. Аналогичная ситуация возникает и при осаждении слоев химическими способами из газовой фазы, где степень перенасыщения составляет 1020—1040. В этом случае единственно приемлемой теорией для анализа роста пленок является кинетическая теория Френкеля — Родина.
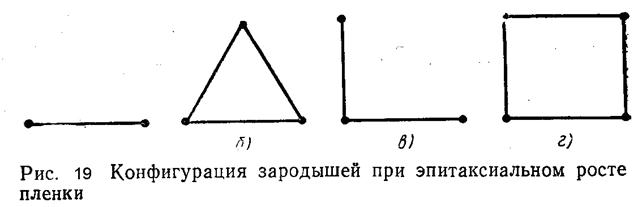
Пока не существует достаточно разработанной теории образования и роста эпитаксиальных слоев. Излагаемая теория Френкеля — Родина устанавливает лишь ряд важных закономерностей, часто подтверждаемых экспериментально.
В 1924 г. Я. И. Френкелем было введено понятие двумерного пара (газа). В соответствии с этим понятием атомы, попавшие на поверхность твердого тела из объема паровой или газовой фазы, адсорбируются этой поверхностью иудерживаются на ней в течение времени:
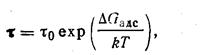 (233)
(233)
где τо =10-13 с — время, соответствующее дебаевской частоте; ∆Gадс — свободная энергия адсорбции атома; Т — температура поверхности.
Частицы двумерного пара, мигрируя по поверхности, сталкиваются друг с другом, образуя агрегаты издвух, трех и т. д. атомов. Простейшим агрегатом является двойник (i = 2), показанный нарис. 19, а, с энергией межатомной связи Еп и энергией связи с поверхностью 2 E 12. Поскольку двухатомные агрегаты вдвое сильнеесвязаны с поверхностью, чем одиночные атомы, они и менее подвижны. Для испарения двойника нужна энергия 2E12, а одного атома Е12. При осаждении металлов и полупроводников на диэлектрические пластины Е11>Е12 процесс испарения двойника менее вероятен, чем одного атома, что соответствует образованию зародыша конденсированной фазы. При увеличении агрегата (i = 3, 4,… п) вероятность образования зародышей увеличивается.
При очень большом перенасыщении газовой фазы критический зародыш может состоять из одного атома. Поэтому, когда возникает агрегат из двух атомов, более вероятно, что он будет расти, а не распадаться. Снижение перенасыщения приводит к тому, что вероятность присоединения к одному атому другого становится равна вероятности распада агрегата. В таком случае стабильными станут конфигурации с двумя связями на атом. При дальнейшем снижении перенасыщения стабильными становятся агрегаты из трех, четырех и т. д. атомов (рис. 19, а—г). Стабильными образованиями являются треугольник и квадрат. В первом случае зародыш имеет ориентацию < 111 >, во втором — < 100>. Таким образом, степень перенасыщения должна сказываться на ориентации стабильных зародышей.
Зависимость скорости vk образования зародышей (конденсации) из потока J частиц, попадающих на пластину, от температуры пластины T может быть описана следующими уравнениями:
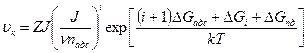 (234)
(234)
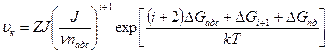 (235)
(235)
где nадс — число единичных адсорбированных атомов; v — частота колебания адсорбированного атома; ∆Gi ∆Gi+1 — свободные энергии образования зародыша в результате межатомного взаимодействия (аналог ДСКЛ1 при эпитаксии).
Поскольку i невелико, можно методом проб и ошибок установить, какое значение i (1, 2, 3,...) отвечает экспериментальным данным.
На рис. 20 приведена логарифмическая зависимость скорости конденсации зародышей от обратной температуры конденсации. При некоторой температуре критический зародыш может состоять из одного атома, следовательно, преобладающей ориентации не будет. При температуре T2-3 должен наблюдаться ориентированный рост пленки.
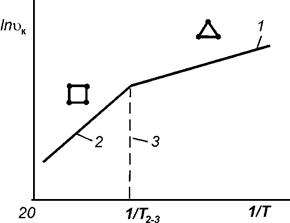 Рис.20 Логарифмическая зависимость скорости конденсации зародышей от обратной температуры конденсации:
Рис.20 Логарифмическая зависимость скорости конденсации зародышей от обратной температуры конденсации:
1-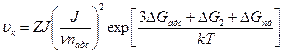 ;
;
2-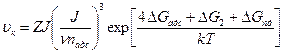
3-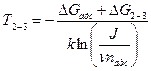
Температуру T2-3 перехода от одной ориентации к другой при осаждении эпитаксиального слоя можно определить, приравняв выражения (234) и (235):
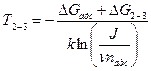 (236)
(236)
где ∆G2-3 — свободная энергия перехода от одной ориентации кдругой.
Это уравнение связывает температуру изменения ориентации от < 111 > к < 100> со скоростью конденсации vK≈J.
Таким образом, между обратной температурой эпитаксиального роста пленки и скоростью конденсации должна существовать линейная зависимость. Экспериментальные данные согласуются с этим теоретическим выводом.
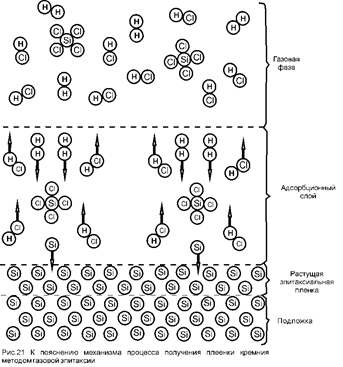
Рассмотрим эпитаксиальный рост кремниевых пленок из газовой фазы согласно теории Френкеля — Родина для реакции SiCl4 + 2H2→Si+4HCl. Реакция протекает на поверхности. В результате образуется адсорбирующийся поток атомов свободного кремния и легколетучий компонент HCl, удаляемый вакуумной системой. Атомы Si врастают в пластину, формируя эпитаксиальный слой. Образование зародышей из газовой фазы с помощью химической реакции (химическое осаждение) отличается от их образования при конденсации в вакууме тем, что появляются дополнительные влияющие факторы. К ним относятся наличие адсорбированного слоя более сложного состава, чем при конденсации в вакууме, возможность более плавного регулирования степени перенасыщения путем изменения термодинамических и кинетических параметров химической реакции. Например, при осаждении эпитаксиальных пленок кремния по схеме (рис.21) SiCl4 + 2H2→Si+4HCl, можно в широких пределах менять степень перенасыщения, регулируя режимы реакций осаждения и травления таким образом, чтобы общая скорость потока частиц на пластину отвечала оптимальным условиям образования и роста эпитаксиальных слоев. Таких условий при осаждении вакуумным испарением практически достигнуть трудно, так как для этого температуру пластины нужно поддерживать на 200—300°С ниже температуры испарения, что технически трудно осуществить для многих веществ.
Для химического осаждения плотность критических зародышей, состоящих из i атомов,
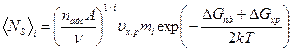 (237)
(237)
где υx.p — скорость роста пленки при химической реакции; mi — порядок реакции; ∆Gxp— свободная энергия активации химической реакции.
Это уравнение позволяет по известной связи между величинами Ns, υx.p и тi при данной температуре Т рассчитать размеры критического зародыша при химическом росте пленки.
Процессы образования эпитаксиальных слоев во многом определяют характер их роста и, следовательно, степень кристаллического совершенства полученной структуры. При значительной ра-зориентации отдельных зародышей слой будет иметь большое число дефектов и может стать неприемлемым для изготовления ИМС
Наибольшее распространение в промышленной практике получили процессы эпитаксии полупроводников из газовой фазы с помощью химических реакций.
Развитие методов эпитаксии, особенно гетероэпитаксии (выращивания пленки одного материала на подложке другого), позволяет получать приборы с такими высокими электрическими характеристиками, которые трудно реализовать другими технологическими методами.
Методы получения эпитаксиальных структур:
1 –молекулярно-лучевая эпитаксия заключается в прямом переносе вещества источника к нагретой монокристаллической подложке без промежуточных реакций. Процесс происходит в сверхвысоком вакууме при давлении 1,33 •10-8Па в режиме молекулярных потоков. Достоинства: высокая точность управления уровнем легирования; широкий выбор легирующих элементов как р-типа так и n-типа; совершенная структура и однородная толщина эпитаксиальных слоев; возможность проводить селективную эпитаксию; низкие температуры процесса; возможность получения сверхтонких пленок (0,5-50 нм); сверхвсокий вакуум и сверхчистота подложек следовательно улучшенные показатели изготавливаемых структур. В состав однокамерной установки МЛЭ входят: вакуумная рабочая камера с средствами получения сверхвысокого вакуума; система формирования молекулярных пучков; система анализа элементного состава и структуры поверхности подложки, а также выращенной эпитаксиальной пленки; ионнная пушка для очистки подложек.
2- газофазовая эпитаксия заключается в организации химических реакций на поверхности подложки или в непосредственной близости от нее при которых образуетсяэпитаксиальный слой. Активация химических реакций может осуществляться тепловым, высокочастотным полями, световым, электронным и рентгеновским излучением. При данной химреакции могут использоваться один или несколько газов-реагентов, ведущих к выделению твердой фазы, но подложка не вступает в химическое взаимодействие при температурах реакции.
3- жидкофазгная эпитаксия осуществляется из растворов расплавов полупроводников в легкоплавком металле растворителе. Раствор-расплав представляет собой разбавленный раствор кристаллизуемого вещества в легкоплавком металле-растворителе.
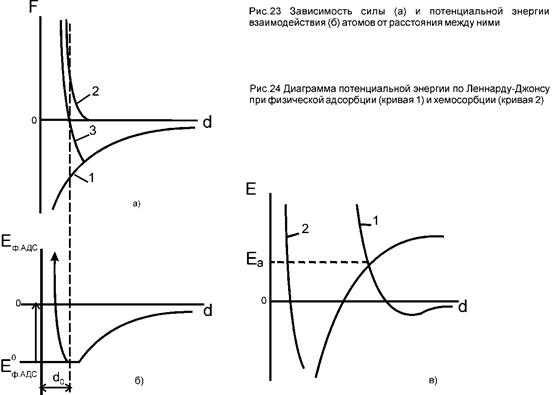
Продифференцировав значение Eф.адcпо d [уравнение (224)] и приравнивая производную нулю, получим выражение для равновесного расстояния da и соответствующей ему энергии взаимодействия Eф.адcОбычно d0 = 50-100 нм (5-10 А), значения Eф.адc в 10— 100 раз меньше энергий диссоциации молекул, но близки к теплоте испарения.
Энергетическое состояние адсорбируемых частиц удобно рассмотреть с помощью диаграммы потенциальной энергии адсорбируемого атома (рис. 24). По мере приближения частиц к поверхности подложки (d→0) они могут адсорбироваться в соответствии с кривой. Если частицы в активированном состоянии имеют некоторое химическое сродство к поверхности, то они хемосорбируются после приобретения ими энергии активации Еa (переход с кривой 1 на кривую 2). Следовательно, механизм адсорбции может соответствовать не только кривой 1, но и кривой 2. При этом сначала осуществляется физическая адсорбция, затем — химическая активация молекулы и хемосорбция.
При хемосорбции происходит перекрытие электронных оболочек адсорбата иадсорбента. Адсорбционные силы в этом случае связаныс передачей электронов от адсорбированных частиц к поверхности и наоборот. В результате на поверхности образуется слой ионов, который индуцирует противоположно заряженный слои на поверхности адсорбента, что обусловливает появление кроме гетерополярных и других сил притяжения.
Энергия взаимодействия адсорбированных поляризованных частиц с поверхностью
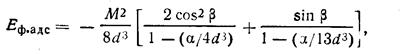 (257)
(257)
где β — угол, образуемый диполем с поверхностью перпендикулярен поверхности, то β = 0).
Уравнение (257) удовлетворительно согласуется с экспериментом.
В зависимости от сил взаимодействия частиц с поверхностью они могут быть локализованными или нелокализованными. Во втором случае частицы свободно диффундируют по поверхности адсорбента, преодолевая потенциальные барьеры (свободную энергию поверхностной диффузии ∆Gп.д.)
Если адсорбированным частицам, находящимся в локализованном состоянии, сообщить дополнительную энергию, то они перейдут в нелокализованное состояние. Поэтому способность адсорбированных частиц диффундировать по поверхности увеличивается с повышением ее температуры.
При соударении частиц с поверхностью твердого тела могут протекать следующие процессы (рис. 25):
1) упругое рассеяние частиц (стадия 1);
2) передача части кинетической энергии твердому телу (стадия 2);
3) захват частиц твердым телом в состоянии А (стадия 3);
4) переход частиц на нижний уровень, потенциальной ямы (стадии 4,5);
5) переход частиц из одного состояния в другое в результате приобретения энергии активации ЕаА-В (стадия 6);
6) переход частиц из одного состояния в другое без дополнительной энергии ЕаА~Б (стадия 7);
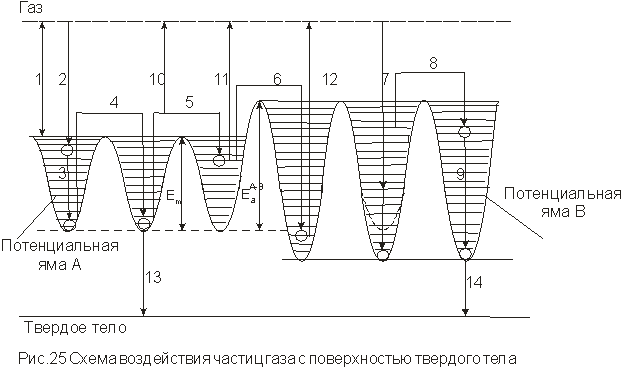
7) фиксация частиц на определенном центре адсорбции (стадия 8) с последующим переходом на дно потенциальной ямы. (стадия 9);
8) десорбция частиц в процессе диффузии (стадия 10) и из состояний А и В (стадии 11 и 12);
.9) образование слоя трехмерного соединения с адсорбентом (стадии 13 и 14).
На перечисленные процессы могут влиять взаимодействия адсорбированных частиц, которые теоретически считались независимыми друг от друга.
При хемосорбции важно определить вероятность удержания поверхностью ударившейся о нее частицы в течение времени, достаточного для протекания дальнейших поверхностных процессов. Однако эту вероятность вычислить трудно.
Описанные модели основаны на методах классической механики. Они выбраны в-виду простоты используемых понятий.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 5803; Нарушение авторских прав?; Мы поможем в написании вашей работы!