
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Процесс управления рисками
|
|
|
|
Чтобы рассмотреть последовательность проведения анализа рисков, можно руководствоваться схемой управления рисками качества, приведенной в документе ICH Q9.
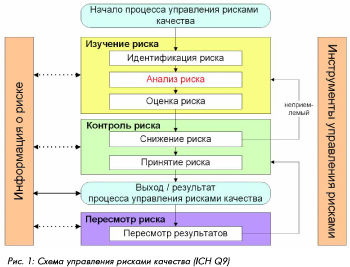
В соответствии с этой схемой процесс управления рисками может быть представлен следующим образом:
1. Изучение возможных отклонений / ошибок (потенциальных рисков) для отдельных компонентов и систем в целом (технологический процесс, оборудование, инженерные системы обеспечения, помещения и т.д.)
2. Анализ и оценка критичности отклонений в отношении качества
3. Определение мер по предотвращению или снижению риска
4. Использование результатов и документирование
5. Информирование о рисках и пересмотр рисков
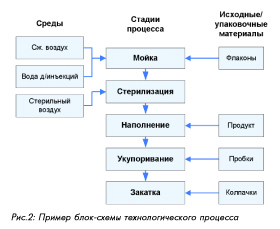
Изучение возможных рисков для отдельных компонентов и системы относится к стадии идентификации риска. Для процесса должно быть составлено описание по стадиям и операциям или приведена блок-схема с указанием стадий и критических факторов (см. пример на рис. 2); для оборудования или систем должно быть приведено описание с перечислением компонентов (и/или приложены необходимы схемы).
Для четкой идентификации рисков в процессе их изучения могут помочь три фундаментальных вопроса:
1. Что может пойти неправильно?
2. Какова вероятность, что это пойдет неправильно?
3. Каковы могут быть последствия (тяжесть)?
Как правило, идентификация рисков в процессе производства лекарственных средств должна охватывать следующие аспекты:
· Состояние помещений и гигиена
· Потоки персонала и материалов
· Окружающие условия
· Спецификации на критические материалы
· Технические аспекты функционирования оборудования
· Поведение продукта (физические свойства, контакт с окружающей средой и оборудованием и др.)
На этой стадии изучения рисков должна использоваться вся имеющаяся информация (документация по процессам, оборудованию, продуктам, проектная документация, эмпирические сведения и опыт на основе аналогичных объектов). В данном случае очень важна достоверность и обширность изучения исходных данных, поэтому наиболее надежные результаты могут быть получены предпочтительно за счет привлечения опытных специалистов из соответствующих областей. В сложных случаях полезно использовать метод экспертной оценки, при этом также важна квалификация и опыт привлекаемых экспертов.
Анализ и оценка критичности рисков, как правило, включает определение величины риска на основании анализа вероятности и тяжести вреда для качества. При этом для GMP -рисков (качественная оценка) достаточно анализа того, существует ли угроза нарушения требований GMP; в любом случае должно прослеживаться влияние на качество продукта.
При необходимости количественной оценки должны использоваться методы и подходы, учитывающие величину вероятности, тяжести и (дополнительно) возможности обнаружения вреда или ущерба.
Для качества и надежности результата важна достоверность данных, поэтому большое значение здесь также приобретает опыт экспертов в данной области. В сложных случаях можно использовать метод экспертной оценки. Поскольку анализ и оценка рисков предполагает возможность или необходимость проверки, то в документации на данной стадии полезно приводить пояснение или обоснование оценки критичности риска, чтобы не возникало разногласий или непонимания при коммуникации и проведении проверок и инспекций.
Для многих задач применения анализ и оценка рисков является окончательной стадией, дающей требуемый результат. Примерами таких задач являются, например, планирование валидации, выбор оборудования и систем, оценка поставщиков и др.
Определение мер по предотвращению или снижению риска относится к стадии контроля рисков. Контроль подразумевает 1) измерение уровня параметра, характеризующего риск (опасного фактора), и 2) управление риском, т.е. принятие меро по его снижению или предотвращению. Поэтому для идентификации и измерения опасного фактора должны быть указаны возможные контрольные признаки, позволяющие качественно или количественно протестировать этот фактор. Для этих контрольных признаков должны быть определены критерии приемлемости, в пределах которых риск считается допустимым.
Методы контроля, предусмотренные для данного риска на данной стадии, рассматриваются как предупреждающие действия в отношении риска, поэтому они также указываются как часть стадии контроля рисков. Все же по характеру действия их можно определить как пассивные методы контроля рисков.
Напротив, меры по снижению или избежанию риска, если он выходит за допустимые пределы, являются активными методами контроля рисков. При разработке этих мер необходимо придерживаться следующих принципов:
· Усилия и ресурсы, требуемые для устранения или снижения риска, должны быть соразмерны значительности риска (вероятности и тяжести ущерба). Как раз в этом проявляется отличие подхода, основанного на изучении рисков, от простого следования и выполнения всех предупредительных мер. Следует учитывать, что такой параметр, как например, тяжесть ущерба вследствие отклонения от качества, может значительно различаться для разных компаний-производителей. Соответственно будет различаться и уровень запланированных предупредительных мер, которые могут варьировать, например, от разработки или изменения процедур до закупки оборудования или изменения его конструкции.
· Снижение риска может включать в себя действия по снижению тяжести и вероятности вреда, а также способствующие обнаружению рисков.
· Если снижение риска до приемлемого уровня невозможно, то необходимо изменить процесс или предусмотреть страхование риска (если это допустимо). При этом страхование рисков может выражаться как в дублировании операций и оборудования, так и в создании резерва ресурсов (например, в крайнем случае - финансовых средств для урегулирования возможных судебных исков в отношении некачественного продукта).
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 466; Нарушение авторских прав?; Мы поможем в написании вашей работы!