
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 1. 8
|
|
|
|
Внутренняя энергия идеального газа. В общем случае, рассматривая произвольную термодинамическую систему, выражение для ее полной энергии можно представить в виде
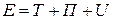 ,
,
где 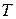 - кинетическая энергия системы как целого или ее макроскопических частей,
- кинетическая энергия системы как целого или ее макроскопических частей, 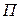 - потенциальная энергия системы во внешнем силовом поле (гравитационном или электромагнитном),
- потенциальная энергия системы во внешнем силовом поле (гравитационном или электромагнитном), 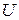 - суммарная внутренняя энергия системы, зависящая только от ее внутреннего состояния.
- суммарная внутренняя энергия системы, зависящая только от ее внутреннего состояния.
Внутренняя энергия включает в себя все возможные виды взаимодействия и движения частиц (атомов, молекул, ионов, электронов, нуклонов), составляющих термодинамическую систему. Так, например, система, находящаяся в газообразном состоянии, обладает внутренней энергией, состоящей из:
1) кинетической энергии беспорядочного теплового поступательного и вращательного движения молекул;
2) колебательного движения атомов и молекул;
3) потенциальной энергии взаимодействия молекул;
4) энергии электронных оболочек атомов и ионов;
5) энергии движения и взаимодействия нуклонов (протонов и нейтронов) в атомных ядрах.
В дальнейшем для простоты будем рассматривать термодинамические системы, которые макроскопически неподвижны и которые не подвержены действию внешних силовых полей. Тогда полная энергия такой системы равна ее внутренней энергии.
Важно отметить, что внутренняя энергия термодинамической системы является однозначной функцией ее состояния. Это значит, что значение внутренней энергии системы 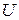 в данном состоянии не зависит от того, каким образом система пришла в это состояние. Как и в случае потенциальной энергии, значение
в данном состоянии не зависит от того, каким образом система пришла в это состояние. Как и в случае потенциальной энергии, значение 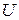 определяется с точностью до некоторой постоянной
определяется с точностью до некоторой постоянной 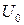 , величина которой зависит от выбора «уровня» отсчета внутренней энергии системы, т.е. от того, какое состояние системы мы будем считать состоянием с нулевой потенциальной энергией.
, величина которой зависит от выбора «уровня» отсчета внутренней энергии системы, т.е. от того, какое состояние системы мы будем считать состоянием с нулевой потенциальной энергией.
Работа и количество теплоты. Обмен энергией между закрытой системой и внешней средой может осуществляться двумя качественно различными способами: путем теплообмена и за счет совершения работы. Энергия, передаваема термодинамической системе или отдаваемая этой системой посредством теплообмена, называется теплотой. Энергия, передаваемая системе или отдаваемая системой при ее силовом взаимодействии с внешней средой, называется работой. Если на систему не действуют внешние силовые поля, то работа может совершаться только путем изменения объема термодинамической системы. Пользуясь третьим законом Ньютона, нетрудно показать, что работа 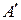 , совершаемая внешними телами над системой, равна со знаком минус работе
, совершаемая внешними телами над системой, равна со знаком минус работе 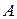 , совершаемой системой против внешних сил, т.е.
, совершаемой системой против внешних сил, т.е.
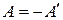 .
.
В отличие от работы передача энергии путем теплообмена носит, как было отмечено выше, качественно иной характер. Теплообмен происходит между телами или различными частями одного тела, имеющими различную температуру. В отличие от работы, совершение которой над системой может приводить к изменению любого вида энергии, передача системе теплоты приводит к увеличению кинетической энергии частиц системы, т.е. к увеличению ее внутренней энергии.
Первое начало термодинамики. В общем случае обмен энергией между системой и внешней средой может происходить одновременно двумя способами: за счет совершения над системой работы и сообщения системе теплоты. Пусть в результате некоторого процесса системе сообщается элементарное количество теплоты 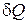 и одновременно над системой совершается элементарная работа
и одновременно над системой совершается элементарная работа 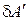 . Переданная при этом системе энергия, очевидно, идет на изменение ее внутренней энергии. Обозначим это элементарное изменение как
. Переданная при этом системе энергия, очевидно, идет на изменение ее внутренней энергии. Обозначим это элементарное изменение как 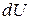 . Таким образом, можем записать, что
. Таким образом, можем записать, что
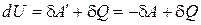 ,
,
или
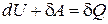 . (1)
. (1)
Соотношение (1) в математической форме выражает первый закон (начало) термодинамики:
количество теплоты, переданной системе, расходуется на изменение ее внутренней энергии и совершение системой работы против внешних сил.
Как мы видим, первое начало термодинамики по сути представляет собой одну из форм записи закона сохранения энергии.
Сразу же отметим, что величины 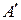 (или
(или 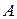 ) и
) и 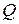 не являются функциями параметров состояния системы, в связи с чем
не являются функциями параметров состояния системы, в связи с чем 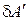 и
и 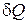 нельзя рассматривать как полные дифференциалы этих функции. Ниже мы увидим, что работа, совершаемая над системой при переводе ее из некоторого состояния 1 в состояние 2, и количество теплоты, переданное при этом системе, зависят от вида процесса, которым система переводится из состояния 1 в 2.
нельзя рассматривать как полные дифференциалы этих функции. Ниже мы увидим, что работа, совершаемая над системой при переводе ее из некоторого состояния 1 в состояние 2, и количество теплоты, переданное при этом системе, зависят от вида процесса, которым система переводится из состояния 1 в 2.
При использовании соотношения (1) следует иметь в виду, что
1) если система в ходе некоторого процесса получает теплоту, то 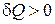 , если система отдает теплоту, то
, если система отдает теплоту, то 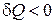 ;
;
2) если система в ходе рассматриваемого процесса совершает работу над внешними телами, то 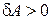 , если внешние тела совершают работу над системой, то
, если внешние тела совершают работу над системой, то 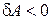 .
.
Работа и теплота алгебраические аддитивные величины, поэтому суммарная теплота, переданная системе в ходе процесса 1-2 и совершенная при этом газом работа равны
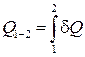 ,
, 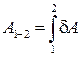 . (2)
. (2)
Работа при расширении и сжатии идеального газа. Рассмотрим сосуд под невесомым поршнем площадью 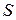 , в котором находится идеальный газ. Первоначально будем полагать, что система находится в положении равновесия. При этом очевидно, что давление газа под поршнем
, в котором находится идеальный газ. Первоначально будем полагать, что система находится в положении равновесия. При этом очевидно, что давление газа под поршнем 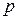 равно внешнему давлению над поршнем
равно внешнему давлению над поршнем 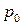 . Предположим, что в ходе некоторого процесса давление газа под поршнем начинает расти. Тогда поршень придет в движение и, преодолевая внешнее давление, будет подниматься вверх, увеличивая объем сосуда под поршнем. За бесконечно малый интервал времени
. Предположим, что в ходе некоторого процесса давление газа под поршнем начинает расти. Тогда поршень придет в движение и, преодолевая внешнее давление, будет подниматься вверх, увеличивая объем сосуда под поршнем. За бесконечно малый интервал времени 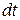 поршень переместится на малую величину
поршень переместится на малую величину 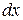 . При этом объем под поршнем изменится на величину
. При этом объем под поршнем изменится на величину 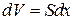 . В случае расширения газа
. В случае расширения газа 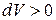 . Будем считать, что изменение объема газа
. Будем считать, что изменение объема газа 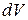 настолько мало, что давление газ практически не изменяется. Тогда совершаемая газом работа, очевидно равна
настолько мало, что давление газ практически не изменяется. Тогда совершаемая газом работа, очевидно равна
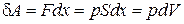 . (3)
. (3)
Полученное для элементарной работы соотношение (3) показывает, что знак работы определяется знаком приращения объема системы. Если происходит сжатие газа, то 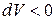 и
и 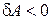 , если газ расширяется, то
, если газ расширяется, то 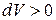 и
и 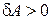 .
.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 489; Нарушение авторских прав?; Мы поможем в написании вашей работы!