
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительное дезаминирование
|
|
|
|
Элиминирование аминогруппы
Реакция характерна для бактерий и грибов. Для примера можно привести превращение аспарагиновой кислоты в фумаровую
Н СООН
НООС- СН2-СН-СООН ———> > С = С < + NH3
| НООС Н
NH2 фумаровая кислота(транс-бутендиовая)
Рассмотрите внимательно еще раз схему трех наиболее важных реакций трансаминирования. В двух из них участвует а -кетоглутаровая кислота, а образуется глутаминовая. Для непрерывности процесса необходимо превратить обратно глутаминовую кислоту в а -кетоглутаровую. В клетках организма человека это происходит путем реакции окислительного дезаминирования.
В организме человека только глутаминовая кислота участвует в обратимой реакции окислительного дезаминирования, схема которой приведена ниже.
НООС-СН2-СН2 -СН-СООН + НАД + —> НООС-СН2-СН2-С-СООН + НАДН + Н+
| | |
NH2 NH
глутаминовая кислота иминоглутаровая
Далее иминоглутаровая кислота подвергается гидролизу, образуется кетоглутаровая кислота и аммиак
НООС-СН2-СН2-С-СООН + НОН —> НООС-СН2-СН2-С-СООН + NH3
| | | |
NH О
а-кетоглутаровая кислота
7.7. Строение витамина В6 и механизм реакции с его участием
Каталитическая роль витамина В6 в реакциях декарбоксилирования и транстаминирования аминокислот сводится к образованию промежуточного соединения - азометина (основания Шиффа)(реакция нуклеофильного присоединения- элиминирования воды). Витамин В6 существует в трех активных формах. В реакции декарбоксилирования участвует пиридоксамин, а в переаминировании - амино- и альдегидная.
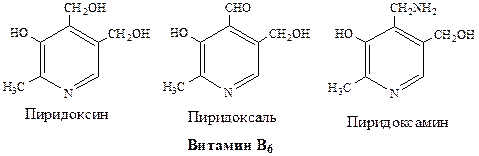
Все 3 формы витамина — бесцветные кристаллы, хорошо растворимые в воде. Активны в виде фосфорных эфиров – пиридоксальфосфата, пиридоксаминофосфата
R - OH + АТФ ———> R – OРО3 Н2 + АДФ
активный витамин В6
Схема реакции переаминирования
- НОН изомеризация
R1 - CH –COOH + В6 – СН = О < =======> R1 - CH –COOH < =======>
| |
NH2 N=СН - В6
аминокислота пиридоксальфосфат азометин (1)
+ НОН
R1 - C –COOH < =======> R1 - C –COOH + В6 – СН2 - NH2
| | гидролиз | |
N — СН2 - В6 О
азометин(2) кетокислота пиридоксаминфосфат
Аминокислота реагирует с пиридоксальфосфатом - альдегидной формой витамина В6. Образуется азометин(1), который изомеризуется в азометин (2). После гидролиза образуется кетокислота и аминоформа витамина В6- пиридоксаминфосфат.
Пиридоксаминфосфат реагирует с новой кетокислотой, реакция проходит в обратном направлении в соответствии со схемой через образование азометина (2), затем азометина(1). Кетокислота в итоге превращается в аминокислоту, а витамин В6 вновь возвращается в альдегидную форму.
7.8. Реакция поликонденсации, образование полипептидов
Аминокислоты способны к поликонденсации, в результате которой образуется полимер- полиамид.
Полимеры, состоящие из а – аминокислот, называются полипептидами, или пептидами. Амидная связь (СО- NH) в таких соединениях называется пептидной связь (пептидной группой).
Механизм реакции поликонденсации SN аналогичен реакции образования амидов кислот(см. лекцию «Карбоновые кислоты»)
В биологических системах синтез полипептидов происходит на рибосомах, каждая аминокислота связана с транспортной РНК, различные ацил -тРНК последовательно удлиняют полипептидную цепь в соответствии с триплетным кодом иРНК, локализованной на рибосоме. Началом полипептидной цепи является аминогруппа. содержащая свободную а- аминогруппу, а концом – содержащая свободную а- карбоксильную группу.
В последовательное соединение аминокислот принято называть первичной структурой белка.
NH2 - СН- СООН + NH2 - СН- СООН + NH2 - СН- СООН + … ——>
| | |
R1 R 2 R3
пептидная группа
nН2О + NH2 - СН- СО- NH - СН- СО- [ NH - СН- СО]х - NH - СН- СООН….

 | | | |
| | | |
R1 R 2 R3 Rn
начало цепи конец цепи
N- концевая С- концевая
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 329; Нарушение авторских прав?; Мы поможем в написании вашей работы!