
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кобальт
|
|
|
|
Цинк
В природі існує п’ять стабільних ізотопів цинку, серед них найбільше припадає на 64 Zn (8,89 %) і 66 Zn (27,81 %). Серед дев'яти радіоактивних ізотопів найбільше біологічне значення має 65 Zn з періодом напіврозпаду 245 діб. У сполуках цинк проявляє ступінь окиснення +2, а як відновник легко заміщує у розчинах Fe, Cu, Nі, Co та інші елементи. За розчинністю у воді Zn наближається до заліза та міді, але він більш рухливий у зв’язку із більшою розчинністю його оксидів і гідроксидів. Сполуки цинку за розчинністю розташовуються у такій послідовності: найлегше розчинні ZnSO4 і ZnCl2, значно менш розчинним є його карбонат (ZnCO3), а до слаборозчинних належать фосфат (Zn3(PO4)2 та сульфід цинку (ZnS). Для природних вод найбільш характерними є його гідроксокомплекси [ZnOH]+ та в меншій мірі – [Zn(OH)2]o.
Серед мінералів, до складу яких входить цинк, найбільш поширені в природі сульфід цинку (сфалерит) та смітсоніт, що містить до 65 % цинку. Джерелами надходження цинку в гідросферу є океанічні залізо-магнієві конкреції та донні осади вулканічного походження. Тільки за рахунок гідротермічних процесів, пов’язаних з океанічною вулканічною діяльністю, в гідросферу надходить в середньому 4×1017 г/рік цинку, або приблизно 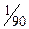 його щорічного надходження з річковим стоком.
його щорічного надходження з річковим стоком.
У грунтах цинк легкорухливий, але при міграції він досить швидко сорбується органічними та мінеральними речовинами, до складу яких входить алюміній, залізо, кремній, марганець та інші елементи. Саме висока сорбційна здатність деяких речовин грунту стосовно цинку визначає його найбільший вміст у верхньому (приповерхневому) шарі грунту. У грунтах цинк знаходиться у різних формах: він може входити до складу слаборозчинних оксосульфатів, карбонатів, фосфатів, силікатів та інших сполук, утворює комплекси з гуміновими та фульвокислотами. У кислих грунтах розчинність Zn вища, ніж у нейтральних і лужних. При високому вмісті в грунті фульвокислот та гліцину його розчинність падає. Ці чинники впливають на надходження Zn з водозбірної площі у водні об'єкти.
Значна кількість цинку надходить у водні об'єкти з техногенними забрудненнями. Так, у залізорудних магнетитових родовищах його вміст у хвостосховищах протягом року досягає 4 тис. т за рік. У грунтах навколо фабрик по збагаченню поліметалевих руд його вміст досягає 0,3 %. Істотні джерела надходження цинку у водні об'єкти – рудникові змивні води та стічні води гальванічних цехів, виробництв паперу, лаків і фарб, хімічних засобів захисту рослин, комбінатів кольорової металургії та теплових електростанцій, які працюють на кам’яному вугіллі.
У поверхневих водах суші вміст цинку оцінюється в мікрограмах на 1 л води (мкг/дм3). Його вміст у воді і грубодетритному мулі має тенденцію до збільшення від гумідних до аридних ландшафтних зон. Дані щодо вмісту цинку у воді і донних відкладах деяких водойм України наведені у табл. 15.
Таблиця 15
Вміст цинку у воді і донних відкладах деяких водних об'єктів України
| Водні об'єкти | Вода (мкг/дм3) | Донні відклади на глибині 0–5 см (мг/кг сухої маси) |
| Дністер | ||
| Дністровське водосховище | 102,7–228,8 | 72,5–75,0 |
| Середній Дністер | 78,4–94,9 | 47,5 |
| Дубосарське водосховище | 17,5–78,9 | 47,5–62,5 |
| Нижній Дністер | 23,0–162,0 | 37,5–102,5 |
| Гирло Дністра | 9,4–158,5 | – |
| Водосховища Дніпра | ||
| Київське | 7,5–72,8 | 43,6–105,8 (54,9) |
| Канівське | 9,6–94,4 | |
| Кременчуцьке | 14,9–128,6 | 48,2–91,6 (67,5) |
| Запорізьке | 6,4–176,8 | 90,6–186,5 (104,8) |
| Лимани | ||
| Дніпровсько-Бузький | 16,5–175,0 | 64,5–155,0 (81,3) |
| Дністровський | 10,3–145,0 | – |
| Річки | ||
| Дунай (Кілійська дельта) | 10,2–173,0 | – |
Примітка. Вказані граничні величини; в дужках – середні концентрації.
Таблиця складена за даними П.М. Линника (1999), С.Й. Кошелевої, К.М. Цапліної (1998).
У воді цинк знаходиться у розчинній формі та у складі завислих частинок органічного і мінерального походження. У річок, які формують водність Київського водосховища, завислі форми Zn становлять 50–90 % його загального вмісту, з них до 30–40 % поступово осідає на дно і накопичується в донних відкладах. На співвідношення окремих форм цинку у воді впливає вміст та комплексоутворююча здатність органічних та мінеральних сполук, що надходять у водойми з водозбірної площі. Так, у річковому стоку р. Прип’ять на розчинені форми припадає 77,5 %, у верхньому Дніпрі – 40, в р. Тетерів – 54 %. У Десні, навпаки, до 70 % цинку припадає на його завислі форми, тобто на комплекси з органічними і мінеральними речовинами.
Каскадне розташування дніпровських водосховищ зумовлює поступове випадіння (седиментацію) завислих форм цинку, що і визначає зростання його концентрації у донних відкладах від верхнього Київського до нижче розташованого Канівського водосховища. У процесах сорбції цинку важливу роль відіграють гідробіонти. Планктонні організми можуть абсорбувати до 40–48 % розчиненого у воді цинку. Для порівняння відзначимо, що гідратовані частинки оксиду заліза адсорбують на собі до 95 %, апатиту – 86, глини і торфу до 99 % цинку.
Вміст цинку у океанічних і морських водах значно менший, ніж у річкових. Для океанічних вод середній вміст цинку оцінюється в 7,6 мкг/дм3, в тому числі 7,0 мкг/дм3 розчинених і 0,6 мкг/дм3 завислих форм. Для морських вод ці показники дещо вищі. При загальній концентрації 11,0 мкг/дм3 на розчинені форми припадає 10, а на завислі – 1,0 мкг/дм3. У формуванні мікроелементного складу морських вод виняткова роль належить річковому стоку. Це чітко виявляється при співставленні вмісту цинку у річковій і морській водах, а також у воді естуаріїв, до яких надходить річковий стік. Так, вміст цинку у воді гирлових ділянок річок становить у середньому 90 мкг/дм3. При переході в естуарії або затоки внаслідок зменшення швидкості течії і різкого прискорення седиментації загальна концентрація цинку у воді знижується до 14,3 мкг/дм3, а у прилеглій акваторії моря вона зменшується ще в 2—3 рази. Це один із суттєвих чинників, який обумовлює значно меншу концентрацію не тільки цинку, а й інших мікроелементів (мідь, марганець) у морських (океанічних) водах у порівнянні з річковими.
У процесах, пов’язаних з кругообігом цинку у водних екосистемах, важлива роль належить гідробіонтам. Їх здатність до акумуляції цього металу давно цікавить вчених з точки зору можливості їх використання як показників (моніторів) забруднення водойм і водотоків. Встановлено, що водяні рослини і безхребетні накопичують у своєму тілі значну кількість мікроелементів в умовах, коли їх вміст у воді має лише слабко виявлену тенденцію до зростання.
Так, наприклад, на р. Усмань (Воронізький біосферний заповідник), при досить незначних (12,3 %) змінах концентрації цинку у воді між найбільш чистою південною і більш забрудненою північною частинами річки, накопичення металу в рослинах виявлялося набагато більшим. Різниця вмісту цинку в сестоні на цих ділянках становила 41,7 %, а у вищих водяних рослин вміст цинку з чистої і забрудненої ділянок відрізнявся на 110 %. У двостулкового молюска кульки рогової (Sphaerіum corneum), відібраних із цих ділянок ріки, різниця вмісту цинку у м’яких тканинах становила 85 %. Ще у більшій мірі виявлялась різниця у накопиченні цього елементу у черевоногих молюсків – звичайного ставковика (Lіmnaea stagnalіs) – 100 % і котушки роговидної (Planorbarius corneus) – 160 %.
Накопичення цинку притаманне не тільки прісноводним, а й морським (океанічним) гідробіонтам. Вміст його в океанічних організмах дещо менший в порівнянні з морськими. Так, середня концентрація цинку в морському фітопланктоні оцінюється в 90–93 мг/кг сухої маси, а в океанічному – 61 мг/кг. Така ж тенденція виявляється і у зоопланктону: в морському вміст цинку становить в середньому 41 мг/кг, а в океанічному – 36 мг/кг сухої маси.
Здатність водяних рослин до накопичення цинку пов’язана з особливостями його біологічної дії. Він впливає на ключові реакції фотосинтезу. Відома його роль у перетворенні сполук, які містять сульфгідрильні групи, в забезпеченні синтезу нуклеїнових кислот і білків. Поряд з іншими елементами цинк приймає участь у регуляції синтезу крохмалю та в інших реакціях, пов’язаних з вуглеводним та фосфорним обміном у рослин. У водяних тварин цинк входить до складу карбоангідрази, яка каталізує реакцію дегідратації вугільної кислоти. Він активує ферментативну активність кишкової інвертази, амілази і пептидази у риб. При збільшенні концентрації цинку у воді до 0,1 мг/дм3 активується синтез РНК і ДНК в печінці, кишечнику і м’язах риб. Більш високі концентрації пригнічують синтез нуклеїнових кислот. Відомий вплив цинку на окиснювано-відновні процеси, на зв’язування кисню тканинами.
Як і інші мікроелементи, цинк у великих концентраціях може ставати токсичним, що виявляється в порушенні передачі нервових імпульсів, гальмуванні рухливості риб та інших функціональних порушеннях соматичних органів. Токсична дія розчиненого у воді цинку залежить як від його концентрації, так і від наявності інших хімічних елементів у воді. Так, в присутності кадмію і міді у воді токсичність цинку для риб зростає, і, навпаки, у воді, насиченій кальцієм і магнієм, для прояву токсичної дії необхідні значно більш високі його концентрації.
На відміну від водяних рослин і безхребетних, у риб висока акумулятивна здатність до накопичення цинку в організмі не виявлена. Відмічається лише різниця у вмісті цинку між окремими органами і тканинами. Найбільше його виявляється, крім кісткової тканини, у лусці (118–10 мг/кг). При цьому характер живлення риб не впливає на тканинний розподіл цинку. Так, у чехоні, яка є планктофагом і в меншій мірі хижаком, його середній вміст у м’язах становить 63 мг/кг сухої маси. У бентофагів плітки і ляща ці показники були відповідно 134 і 73,3 мг/кг; у окуня (мішаний тип живлення) вміст цинку в м’язах 102 мг/кг сухої маси. У типових хижаків – судака (84 мг/кг) і щуки (125 мг/кг сухої маси) рівень цинку у м’язах схожий з такими ж величинами у бентофагів.
Серед залозистих органів риб найбільш високим вмістом цинку виділяється печінка. У печінці осетра його вміст становить 157, білуги – 203 і севрюги – 246 мг/кг сухої маси. Вміст цинку у ляща дещо менший – 139–158 мг/кг сухої маси. Значно більш високий вміст цинку характерний для сазана. У нього в усіх органах і тканинах виявлено в 5–8 разів більше цинку, ніж у інших костистих риб.
На різних стадіях розвитку риб вміст цинку в їх організмі може істотно змінюватися. Наприкінці кожного з періодів розвитку (ембріонального, личинкового, малькового) зростає його вміст як в окремих органах, так і в організмі в цілому. У личинок його більше, ніж в ікрі, що розвивається. Це ще раз підтверджує важливу метаболічну роль цинку в життєдіяльності риб. Відомо, що в личинковий період розвитку у риб різко зростає потреба не тільки у макроелементах, а й в мікроелементах, зокрема в цинку. Він в більшій кількості потрібен для формування кісткового скелету, плавців, луски; як активатор лужної фосфатази, цинк необхідний для синтезу і активації цинкмістких ферментів, що забезпечують процеси тканинного дихання, які у період раннього онтогенезу риб відбуваються досить інтенсивно. Саме це і визначає більш високу акумулюючу здатність організму риб на ранніх стадіях розвитку (личинки, мальки), для яких характерний і більш чітко виявлений вплив характеру живлення на акумуляцію цинку в організмі, ніж у дорослих риб. З віком подовжуються трофічні ланцюги і змінюється сам характер живлення молоді. Наприклад, сазан і лящ поступово переходять до придонного способу життя і починають живитися бентосними організмами, які містять менше цинку та інших мікроелементів (залізо, марганець), ніж планктонні. Все це і визначає вікову динаміку змін вмісту цинку в організмі риб на різних стадіях онтогенезу.
Кобальт належить до елементів, які утворюють сполуки практично з усіма галогенами (CoF2, CoF3, CoCl2, CoBr2, CoІ2). Всі галогеніди двовалентного кобальту добре розчинні у воді. Серед інших сполук, які зустрічаються у природі, заслуговують на увагу карбонат кобальту (СoCO3), нітрат кобальту [Co(NO3)2 × 6H2O], сульфат кобальту [CoSO4 × 7H2O].
У розчинах для кобальту характерні два стани окиснення, при яких він виступає як двовалентний (Со 2+) і тривалентний (Со 3+) елемент. Двовалентний кобальт (Со 2+) у процесі розчинення його солей взаємодіє з молекулами води. В присутності лігандів він легко окиснюється молекулярним киснем і може сприяти його транспорту. В природних водах кобальт може знаходитись у різних формах. На його взаємодію з іншими речовинами впливає рН і окиснювано-відновний потенціал (Eh) середовища. Кобальт може утворювати комплекси з гуміновими кислотами. При рН води 6,5–8,0 виявляється його максимальна здатність до комплексоутворення з фульвокислотами.
Метаболічна роль кобальту пов’язана з його участю в процесах кровотворення і перенесенням кисню гемоглобіном та іншими пігментами крові. Він є необхідним елементом у синтезі гемоглобіну, що відбувається опосередковано – через вітамін В12, в структуру якого входить кобальт.
В організмі тварин кобальт активує іонізацію і резорбцію заліза, сприяючи тим самим включенню атомів заліза в молекулу гемоглобіну. Внаслідок його впливу на еритропоез (процес утворення еритроцитів) в крові зростає кількість формених елементів крові, що свідчить про його безпосередню участь у реакціях, які відбуваються у кровотворних органах. Гемопоетичний (гемопоез – кроветворення) вплив кобальту виявляється найбільш ефективно, якщо в організмі присутні залізо і мідь, тобто ті елементи, які приймають участь у механізмі переносу кисню гемоглобіном та іншими пігментними білками.
Крім участі в кровотворенні, кобальт сприяє синтезу білків, асиміляції азоту та накопиченню в органах і тканинах білків. Введення у кормові суміші риб солей кобальту сприяло збільшенню біомаси цьогорічок майже на 20 %, а додаткове введення в гранульовані кормові суміші комплексу мікроелементів, до яких входять кобальт, марганець і молібден (у кількості 3 мг на 1 кг корму), стимулює приріст біомаси у молоді коропа на 15 %, а у дворічних коропів – на 22 %.
Як уже відзначалось, вплив кобальту на процеси перенесення гемоглобіном кисню виявляється в присутності іонів заліза і міді. Він впливає також на обмін і біологічну дію кальцію і фосфору. Так, недостатнє надходження в організм солей кобальту призводить до неповного засвоєння кальцію і фосфору. При дефіциті кобальту у воді знижується і їх утилізація молюсками та іншими водяними тваринами.
Кобальт активує кісткові і кишкові фосфатази, карбоксилази, аргінази, каталази і деякі пептидази. В той же час під його впливом знижується активність сукцинатдегідрогенази і цитохромоксидази.
В поверхневих водах суші, зокрема, у водних об'єктах України, вміст кобальту може коливатись у межах від слідових концентрацій до 0,01 мг/дм3. Спостерігається зниження концентрації кобальту від весни до літа, що пов'язано з його осадженням із завислими частинками та утилізацією гідробіонтами.
Роль гідробіонтів у кругообігу кобальту досить значна. Так, наприклад, у фітопланктоні рибоводних ставків у розрахунку на 1 кг сухої маси припадає
30 мг кобальту. Серед макрофітів найбільше кобальту накопичує сальвінія плаваюча, а найменше – очерет звичайний. В організмі безхребетних його вміст значно вищий, ніж у воді, що свідчить про його акумуляцію у біологічних рідинах і тканинах. Значну кількість кобальту накопичують олігохети і личинки хірономід.
Вміст кобальту в крові осетрових риб становив: у осетра – 2,66 мг/кг, у севрюги – 2,29, у білуги – 1,53 мг/кг сухої маси. У м’язах вказаних риб його вміст коливався в межах 1,06–1,6 мг/кг.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 496; Нарушение авторских прав?; Мы поможем в написании вашей работы!