
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
N-n n-n
|
|
|
|



 → [-R-C C—R′—C C—]n
→ [-R-C C—R′—C C—]n
O O
Реакции поликонденсации, как и все реакции конденсации, большей частью являются равновесными. Их можно осуществлять в условиях, близких к равновесным (равновесная поликонденсация) или когда равновесие сдвинуто в сторону образования полимера (неравновесная поликонденсация).
Примером равновесной поликонденсации может быть синтез полиамидов из аминокислот или дикарбоновых кислот и диаминов, а образование фенолоформальдегидных смол и полиамидов из дихлорангидридов дикарбоновых кислот и диаминов являются примерами неравновесной поликонденсации. При проведении неравновесной поликонденсации подбирают такие реагенты и такие условия, чтобы реакция протекала далеко от равновесия, т.е. отсутствовали деструкция полимера низкомолекулярными продуктами, обменные реакции и т.п. Этого достигают проведением процесса при таких низких температурах, при которых обменные реакции замедлены, а исходные вещества достаточно реакционноспособны, чтобы в этих условиях образовывать полимер, а также получением полимера такого химического строения, который не способен к гидролизу и иным деструктивным превращениям при взаимодействии с низкомолекулярным продуктом поликонденсации и с исходными веществами.
При равновесной поликонденсации для максимального превращения исходных веществ в полимер из системы необходимо удалять низкомолекулярный продукт реакции. С этой целью поликонденсацию проводят при повышенных температурах (обычно в токе инертного газа), на заключительной стадии процесс проводят в вакууме. Смещение равновесия путём удаления из сферы реакции низкомолекулярного соединения способствует получению полимера с большей молекулярной массой.
В некоторых случаях при взаимодействии функциональных групп наряду с линейными полимерами образуются побочные циклические продукты. Направление реакции, т.е. возможность протекания циклизации или линейной поликонденсации, определяется в основном условиями проведения реакции и строением исходного бифункционального вещества. При разбавлении системы и повышении температуры поликонденсации выход циклических продуктов, как правило, возрастает. Циклизация является основным направлением реакции в тех случаях, когда могут образовываться ненапряжённые пяти- и шестичленные циклы (например, при циклизации аминомасляной, аминовалериановой, оксимасляной кислот).
Кинетика линейной поликонденсации. Обычно при рассмотрении кинетики поликонденсации принимают, что реакционная способность функциональных групп не зависит от размера молекул и вязкости реакционной среды. Принятие этих экспериментально проверенных допущений позволяет при расчёте скорости процесса пользоваться единой константой скорости реакции и заменять концентрации молекул концентрациями функциональных групп.
Скорость линейной поликонденсации, схематично изображённой следующим образом,
 X-R-X + Y-R-Y → X(-R-)nY + X-Y
X-R-X + Y-R-Y → X(-R-)nY + X-Y
X-R-Y + X-R-Y
измеряется скоростью изменения концентрации одной из расходуемых в реакции функциональных групп (CX или CY):
-dCX/dt = -dCY/dt = k′CкатCXCY
где k′ - эффективная константа, имеющая размерность константы скорости реакции третьего порядка, Скат – концентрация катализатора.
Катализаторами поликонденсации служат те же соединения, которые катализируют аналогичные реакции конденсации низкомолекулярных веществ. Например, в качестве катализаторов полиэтерификации используют минеральные кислоты, сульфокислоты, кислые соли и др. Концентрация катализатора остаётся в течение всего процесса постоянной, что позволяет заменить k′Cкат на k - эффективную константу скорости второго порядка.
Принимая, что СX = CY = C, получим:
- dC/dt = kC2
После интегрирования и последующих преобразований это уравнение приобретает вид
ktC0 = q/(1-q)
где q = (C0 – Ct)/C0 – глубина превращения, С0 и Сt – начальная и текущая концентрации функциональных групп.
Данное уравнение справедливо для неравновесных процессов и для начальной стадии равновесных процессов, на которой скоростью обратной реакции можно пренебречь.
Кинетические параметры равновесной и неравновесной реакций сильно различаются. Равновесные реакции характеризуются относительно малыми скоростями реакций (k ≈ 10-3 – 10-5 л/(моль∙с) в обычных условиях) и довольно высокими значениями энергии активации (85 – 170 кДж/моль); они могут быть как экзо-, так и эндотермическими. Для неравновесной поликонденсации характерны в основном высокие скорости реакций (k до 105 л/(моль∙с)) и низкие значения энергии активации (8 – 40 кДж/моль); эти процессы, как правило, сильно экзотермичны.
Средняя степень полимеризации образующегося полимеравыражается уравнением Карозерса
Pn = C0/C = 1/(1 - q) = 1 + kC0t
Из уравнения следует, что Pn однозначно определяется глубиной превращения и линейно возрастает с увеличением продолжительности реакции. Согласно графику зависимости средней степени полимеризации от

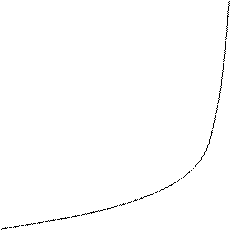


 Pn
Pn





 2
2

0,5 0,8 1,0 q
глубины превращения, приведённому на рисунке, высокомолекулярные продукты могут получаться только при степенях превращения q > 0,95. При меньших конверсиях образуются лишь олигомерные вещества (в отличие от цепной полимеризации, при которой высокомолекулярные продукты могут образовываться уже при самых малых степенях превращения).
Теоретически при линейной поликонденсации степень полимеризации образующегося продукта должна бесконечно увеличиваться с ростом q. Однако, практически достичь степени полимеризации, превышающей 103, очень трудно. Одна из причин этого – трудность соблюдения строгих стехиометрических соотношений реагирующих функциональных групп из-за присутствия примесей и протекания побочных реакций. При отсутствии стехиометрического соотношения функциональных групп, если CX < CY, средняя степень полимеризации определяется по уравнению
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 374; Нарушение авторских прав?; Мы поможем в написании вашей работы!