
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Подгруппа фтора
|
|
|
|
Галогены – элементы VII группы – фтор, хлор, бром, йод, астат (астат мало изучен в связи с его радиоактивностью). Галогены – ярко выраженные неметаллы. Лишь йод в редких случаях обнаруживает некоторые свойства, схожие с металлами.
В невозбужденном состоянии атомы галогенов имеют общие электронную конфигурацию: ns2np5. Это значит, что галогены имеют 7 валентных электронов, кроме фтора.

Физические свойства галогенов: F2 – бесцветный, трудно сжижающийся газ; Cl2 – желто-зеленый, легко сжижающийся газ с резким удушливым запахом; Br2 – жидкость красно-бурого цвета; I2 – кристаллическое вещество фиолетового цвета.
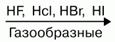
Водные растворы галогеноводородов образуют кислоты. НF – фтороводородная (плавиковая); НCl – хлороводородная (соляная); НBr – бромоводородная; НI – йодоводородная. Силы кислот сверху вниз снижаются. Плавиковая кислота является самой слабой в ряду галогеново-дородных кислот, а йодоводородная – самой сильной. Это объясняется тем, что энергия связи Нг сверху уменьшается. В том же направлении уменьшается и прочность молекулы Н Г, что связано с ростом межъядерного расстояния. Растворимость малорастворимых солей в воде тоже уменьшается:
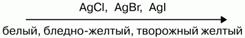
Слева направо растворимость галогенидов уменьшается. АgF хорошо растворим в воде. Все галогены в свободном состоянии – окислители. Сила их как окислителей снижается от фтора к йоду. В кристаллическом, жидком и газообразном состоянии все галогены существуют в виде отдельных молекул. Атомные радиусы возрастают в том же направлении, что приводит к повышению температуры плавления и кипения. Фтор диссоциирует на атомы лучше йода. Электродные потенциалы при переходе вниз по подгруппе галогенов снижаются. У фтора самый высокий электродный потенциал. Фтор – самый сильный окислитель. Любой вышестоящий свободный галоген вытеснит нижестоящий, находящийся в состоянии отрицательного однозарядного иона в растворе.
фторхлорбромиод1.Электролиз KF
2KF 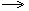 2K+ F2
2K+ F2
2.Нагревание рекоторых фторидов
2CoF3 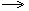 2CoF2 + F2
2CoF2 + F2 
1.Электролиз хлоридов
2KCl 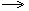 2K+ Cl2
2K+ Cl2
2.Метод Дикона
4HCl + O2 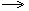 2H2O + 2Cl2
2H2O + 2Cl2
3.Окисление хлороводорода
2KMnO4 + 16HCl =2KCl + 2MnCl2 + 8H2O + 5Cl21.Вытеснение из бромидов
MgBr2 + Cl2 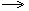 MgCl2 + Br2
MgCl2 + Br2
1.Обработка иодата гидросульфитом натрия
2NaIO3 + 5NaHSO3 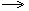 2Na2SO4+ 3NaHSO4 + H2O + I2
2Na2SO4+ 3NaHSO4 + H2O + I2
Химические свойства галогенов.
Рассмотрим свойства галогенов на примере хлора:
| 1.Взаимодействие с металлами | Mg + Cl2 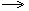 MgCl2 MgCl2
|
| 2.Реакции с неметаллами | H2 + Cl2 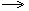 2HCl 2HCl
|
| 3.Взаимодействие со щелочами на холоду | 2NaOH + Cl2 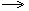 NaCl + NaClO + H2O NaCl + NaClO + H2O
|
| 4.Взаимодействие со щелочами при нагревании | 6NaOH + 3Cl2 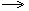 5NaCl + NaClO3 + 3H2O 5NaCl + NaClO3 + 3H2O
|
| 5.Вытеснение менее активных галогенов из галогенидов | 2KBr + Cl2 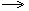 2KCl + Br2 2KCl + Br2
|
| 6. С водой | H2O + Cl2 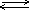 HCl + HClO(хлорная вода) HCl + HClO(хлорная вода)
|
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 1205; Нарушение авторских прав?; Мы поможем в написании вашей работы!