
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема № 6. Окислительно-восстановительные реакции
|
|
|
|
Тема № 5. Гидролиз солей
Тема № 4. Реакции обмена в водных растворах электролитов
Тема № 3. Электролитическая диссоциация
Напишите уравнения полной диссоциации в водных растворах следующих электролитов.
1. HNO3, H2SO4, HCIO4, H2SeO4, HBr.
2. Mg(NO3)2, K2SiO3, Ba(OH)2, H3BO3, KNaSO4
3. NaOH, NH4OH, Ca(OH)2, Ba(OH)2, KNO2.
4. Fe2(SO4)3, Mg(NO3)2, K3PO4, KCI, (NH4)2SO4.
5. HCI, NaCI, HCIO4, K2CO3, Ba(OH)2.
6. AI(OH)3, Na3PO4, H2SO4, HNO3, KCI.
7. AICI3, FeSO4, Ca(OH)2, NaHCO3, Ba(H2PO4)2.
8. FeCI3, Ca(H2PO4)2, KNaSO4, NH4CI, Na2SiO3.
9. H3BO3, H2SO3, CuCI2, CH3COONa, Pb(NO3)2.
10. K2SiO3, MnSO4, H2S, MgOHCI, Ca(NO3)2.
Составьте полные и сокращенные ионные уравнения реакции между следующими веществами:
1. а) Нитрат кальция + карбонат калия; б) Азотная кислота + гидроксид бария;
2. а) Нитрат бария + сульфат калия; б) карбонат калия + соляная кислота.
3. а) карбонат натрия + серная кислота; б) гидроксид натрия + нитрат железа(III).
4. а) нитрат свинца + сульфат калия; б) силикат натрия +гидроксид бария.
5. а) хлорид железа(III)+ гидроксид калия; б) сульфат железа(II)+ фосфат натрия.
6. а) карбонат магния + соляная кислота; б) хлорид алюминия + нитрат серебра.
7. а) гидроксид железа(II)+ азотная кислота б) ацетат натрия +серная кислота.
8. а) сульфид калия +соляная кислота; б) карбонат натрия + азотная кислота.
9. а) сульфат натрия + хлорид бария; б)гидроксид натрия + сернистая кислота.
10. а) хлорид магния + гидроксид калия; б) хлорид железа(II) + нитрат серебра.
Составить молекулярное и ионно-молекулярное уравнения реакций гидролиза 4-х солей и оценить рН раствора:
1. а) NaCl; б) Na2CO3; в) AlCl3; г) CuS.
2. а) Na2SO4; б) K2S; в) MnCl2; г) AgI.
3. а) KCl; б) CuCO3; в) FeCl2; г) K2SO3.
4. а)KNO3; б) K2SO3; в) ZnI2; г) BaCO3.
5. а) LiCl; б) Na2SO3 в) ZnCl2; г)Ag2CO3.
6. а) LiNO3; б) K3PO4; в) AgBr; г) ZnBr2.
7.а)LiCl; б) Na2SiO3; в) ZnSO4; г) CaSO4.
8. а) Li2SO4; б) K2SO3; в) PbI2; г) MnBr2.
9. а)Li2SO3; б) KF; в) Fe(NO3)2 г) MnCO3.
10. а)NaCl; б) ZnI2; в)MgS; г)FeF2.
Подберите коэффициенты методом ионно-электронного баланса, укажите окислитель и восстановитель.
1. Al +K2Cr2O7 + H2SO4 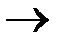 Al2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O.
Al2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O.
2. KClO3 + FeSO4 + H2SO4 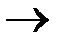 KCl + Fe2(SO4)3 + H2O.
KCl + Fe2(SO4)3 + H2O.
3. KMnO4 + HCl 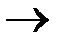 KCl + Cl2 + MnCl2 + H2O.
KCl + Cl2 + MnCl2 + H2O.
4. FeCl2 + KMnO4 + HCl 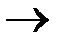 FeCl3 + MnCl2 + KCl + H2O.
FeCl3 + MnCl2 + KCl + H2O.
5.Ti2(SO4)3+ KMnO4+ H2SO4 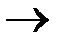 Ti(SO4)2 + MnSO4 + K2SO4 + H2O.
Ti(SO4)2 + MnSO4 + K2SO4 + H2O.
6. Cu + HNO3 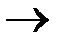 Cu(NO3)2 + NO + H2O.
Cu(NO3)2 + NO + H2O.
7.Zn + KMnO4 + H2SO4 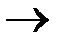 ZnSO4 + MnSO4 + K2SO4 + H2O.
ZnSO4 + MnSO4 + K2SO4 + H2O.
8. Ag + HNO3 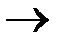 AgNO3 + H2O + NO2.
AgNO3 + H2O + NO2.
9.Mg + H2SO4 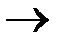 H2S + MgSO4 + H2O.
H2S + MgSO4 + H2O.
10.K2Cr2O7 + H2S + H2SO4 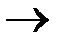 Cr2(SO4)3 + S + K2SO4 + H2O.
Cr2(SO4)3 + S + K2SO4 + H2O.
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 465; Нарушение авторских прав?; Мы поможем в написании вашей работы!