
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Газовых системах
|
|
|
|
Расчет константы равновесия в реальных (неидеальных)
В газообразных системах, находящихся под достаточно высоким давлением, условие химического равновесия приводит к тому, что
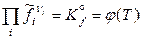 , (12.57)
, (12.57)
где 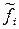 – относительная летучесть i -го компонента. Докажем это:
– относительная летучесть i -го компонента. Докажем это:
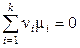 ,
, 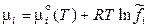 ,
, 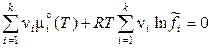 ,
,
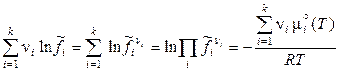 ,
,
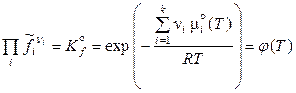 .
.
Поскольку
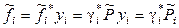 .
.
где 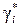 – коэффициент летучести i -го газа при давлении, равном общему давлению смеси, то
– коэффициент летучести i -го газа при давлении, равном общему давлению смеси, то
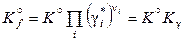 , (12.58)
, (12.58)
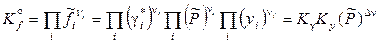 . (12.59)
. (12.59)
При Р = 1 атм коэффициенты летучести равны единице, поэтому
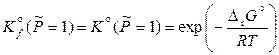 . (12.60)
. (12.60)
Окончательно для реакции в реальной газовой системе получаем
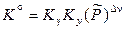 . (12.61)
. (12.61)
Для расчета коэффициентов летучести компонентов удобно пользоваться законом соответственных состояний.
Рассмотрим также вопрос о влиянии давления на состав равновесной газовой системы. Для реакции
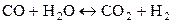
изменение числа молей газообразных веществ Δν = 0 и в идеально-газо-вых условиях давление не влияет на состав равновесной смеси:
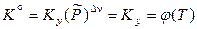 .
.
Однако в реальных условиях с увеличением давления и температуры коэффициенты летучести участников реакции все больше отличаются от единицы и уже К γ ≠ 1. Например, для данной реакции при T = 900 K и P = 500 атм 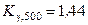 . Тогда при постоянной температуре 900 К и давлении 500 атм
. Тогда при постоянной температуре 900 К и давлении 500 атм
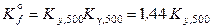 ,
,
а при давлении 1 атм
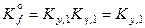 .
.
Следовательно,
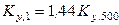 ,
,
и, следовательно, состав равновесной смеси при увеличении давления сдвигается в сторону исходных веществ (величина Ky уменьшается с увеличением давления).
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 277; Нарушение авторских прав?; Мы поможем в написании вашей работы!