
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основы графического метода в термодинамике
|
|
|
|
Расчет работы в технической термодинамике.
В терминологии лекции 1 работа внешней среды над рабочим телом – это просто количество деформационного воздействия dw = pdv. Причем, ранее показано, что dw не является полным дифференциалом и что величина
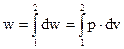 (2.22)
(2.22)
сильно зависит не только от параметров начального и конечного состояния в точках 1 и 2 процесса, но и от его траектории.
Если известно уравнение связи p = p(v), то расчет количества работы сводится ко взятию интеграла в (2.22). В технической термодинамике эта связь давления и удельного объема чаще всего представляется в виде:
pvn = const или pvn = p1v1n, т.е. p = p1v1nv-n, при n = const. (2.23)
Это уравнение в технической термодинамике носит название политропы – каждое значение n определяет свою «тропу», т.е. траекторию, и отражает связи параметров p и v. Подробнее о политропах будем говорить в лекции 3.
Если подставить эту зависимость p = p(v) в (2.22), то получим табличный интеграл, который после несложных преобразований с помощью (2.23) приводится к одному из следующих видов:
 или
или 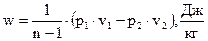 . (2.24)
. (2.24)
Расчетные формулы (2.24) пригодны для политропического процесса для любого реального вещества.
Для идеального газа с учетом связи pv = RуT расчетная формула в (2.24) несколько упрощается:
 (2.25)
(2.25)
Полная работа деформации (сжатия или расширения) за процесс рассчитывается как:
W = mw, Дж, где m – масса рабочего тела.
Если зависимость p = р(v) представлена в графическом виде, т.е. процесс с рабочим телом изображен на диаграмме p – v для какого-то вещества, то расчет количества работы можно провести в соответствии с рис. 2.4, как площадь под линией процесса до оси v.
Расчет количества работы возможен с помощью первого закона термодинамики:
Δu = q – w → w = q – Δu, (2.26)
если предварительно найти изменение внутренней энергии Δu и количество теплоты q так, как показано в этой лекции выше.
Замечание. В этом параграфе до сих пор шла речь о работе деформации рабочего тела, т.е. сжатия или расширения термодинамической системы в геометрическом пространстве. Однако, в технической термодинамике необходимо уметь рассчитывать работу проталкивания:
dw΄ = vdp, Дж/кг (2.27)
Особенно, этот расчет необходим для проектирования компрессоров и для определения мощности их привода. В этом случае (2.27) называют располагаемой работой.
На рис. 2.10 представлены две диаграммы в осях p – V теоретическая рабочая и p – v термодинамическая для процесса компремирования. Для идеального одноступенчатого компрессора этот процесс состоит из двух изобар и одной политропы с заданным показателем n.

Рис. 2.10. Иллюстрация работы компрессора в диаграммах p – V и p – v.
Процесс 0 – 1 – всасывание исходной газовой среды, процесс 1 – 2 –
сжатие, 2 – 3 – проталкивание сжатого газа потребителю.
Площадь слева от кривой процесса сжатия pvn = const и представляет собой затраченную на сжатие газа работу (располагаемая работа):
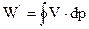 . Дж.
. Дж.
Можно перейти к удельному объему v от геометрического V, если уделить последний на все количество газа m, вошедшего в цилиндр компрессора за весь процесс всасывания 0 – 1. Тогда техническая работа компрессора равна
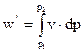 Дж/кг. (2.28)
Дж/кг. (2.28)
Снова воспользуемся уравнением политропы:
pvn = const → pvn = p1v1n → v = v1p11/n p-1/n (2.29)
и подставим полученную зависимость v = v(p) в интеграл (2.28). Опять получается табличный интеграл, после преобразования результата интегрирования с помощью (2.29) окончательно приходим к равенству:
w΄ = nw, где w рассчитывается по (2.24) или (2.25).
Иными словами, работа, затраченная на компрессию газа (располагаемая) в n раз больше работы простого сжатия.
Мощность двигателя для привода одноступенчатого идеального компрессора рассчитывается как:
Nдвиг = Gw΄/η, Вт, (2.30)
где G – массовый расход сжимаемого газа, кг/с, η – коэффициент полезного действия привода.
Замечание. В инженерной практике и, следовательно, в технической термодинамике приходится рассматривать процесс проталкивания газов через каналы, сопла (реактивные двигатели, газовые и паровые турбины). Линейные скорости течения газов в таких каналах настолько велики (звуковые и сверхзвуковые скорости), что процесс течения газа можно рассматривать как адиабатический (нет теплообмена). Это означает, что без учета трения потока газа о стенки канала и трения в самом потоке – s = const, ds = 0. В этой ситуации работа проталкивания рассчитывается через функцию состояния – энтальпию (2.5):
dh = Tds + vdp → dh = vdp → w΄ = 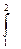 dh = Δh = h2 – h1.
dh = Δh = h2 – h1.
Здесь для идеального газа справедливо выражение (2.20), а для реального рабочего тела используются расчетные таблицы свойств веществ (например, «Таблицы состояния аммиака», «Таблицы для воды и водяного пара» и т.д.).
5.1. p – v диаграмма.
На рис. 2.8 представлены графики зависимости pv=RуT для различных изопроцессов: показан ход изобары (p = const), изохоры (v = const), изотермы (pv = const), изоэнтропы (pvk = const) для идеального газа. По построению в p – v координатах две линии – прямые (p и v), одна (T = const) – равнобокая гипербола и неравнобокая – изоэнтропа (s = const) pvk = const.
Такой график удобен для качественного анализа изменения параметров и функций процессов. Для точных расчетов не используется.

Рис. 2.8 Графики зависимостей р от v для различных изопроцессов p, v, T, s = const с
рабочим телом в состоянии идеального газа.
5.2. T – s диаграмма.
Рассмотрим ход кривых p = const и v = const в диаграмме с координатами T – s. В термодинамике количество термического воздействия (теплоты) рассчитывается как dq = Tds, а в калориметрии – как dq = cdT. Отсюда
Tds = cdT → ds = cdT/T → s2 –s1 = 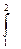 [cx(T)/T] dT =
[cx(T)/T] dT = 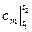 ln T2/T1.
ln T2/T1.
Расчетную формулу для приращения энтропии Δs получим из сх|t2t1 при х = р или х =v:
Δs = 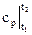 lnT2/T1 для p = const и Δs =
lnT2/T1 для p = const и Δs = 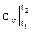 lnT2/T1 для v = const. (2.31)
lnT2/T1 для v = const. (2.31)
Окончательно,
T2 = T1exp{(s –s0)/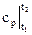 } и T2 = T1exp{(s –s0)/
} и T2 = T1exp{(s –s0)/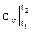 }.
}.
Таким образом, изобара и изохора в осях T – s являются обычными экспонентами, причем из-за того, что ср > cv, изохора круче изобары (см. рис. 2.9), т.к. dT/ds = T/c – тангенс угла касательной к графику соответствующей кривой.

Рис. 2.9. Взаимное расположение графиков процессов
p = const и v = const в осях (Ts), так как cp > cv то изохора проходит круче изобары.
Здесь же показаны процессы s = const и Т = const.
В поле графика T – s (см. рис. 2.9) прямые линии T = const и s = const при избранных масштабах температур и условных значений энтропии (отсчет от s0 = 0 в избранном масштабе), а так же экспоненты p = conct и v = const образуют сетку энтропийной (тепловой) диаграммы.
Возможно использование оси ординат для нанесения условного значения энтальпии от h0 = 0: h = cр|t0*t кДж/кг. Такая диаграмма удобна для широко распространенных изобарных и изоэнтропийных процессов. В первом случае (p = const) dh = Tds + vdp, т.е. h = ∫Tds = qp. Во втором (s = const) dh = Tds + vdp, т.е. h = ∫vdp – работа компрессора.
Для инженерной практики теплофизические институты создают диаграммы p – v и T – s для различных веществ и рабочих тел. Использование их существенно ускоряет расчетный процесс, если не требуется особенная точность.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 3010; Нарушение авторских прав?; Мы поможем в написании вашей работы!