
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Особенности свойств многоатомных спиртов
|
|
|
|
Лекция 7
Важнейшими представителями многоатомных спиртов являются двухатомный спирт этандиол-1,2 (этиленгликоль), и трехатомный спирт пропантриол-1,2,3 (глицерин):

Существуют многоатомные спирты, содержащие и б о льшее количество групп –ОН в молекуле, например, пятиатомный спирт ксилит, который используют в качестве заменителя сахара:
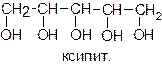
Этиленгликоль и глицерин – вязкие бесцветные жидкости, смешивающиеся с водой в любых соотношениях. Между молекулами многоатомных спиртов, так же как и между молекулами одноатомных спиртов, действуют водородные связи.
Водные растворы этиленгликоля определенной концентрации не замерзает даже при -70 оС, поэтому такие растворы используют в качестве антифризов для охлаждения автомобильных двигателей. Этиленгликоль очень ядовит.
Глицерин, напротив, нетоксичен, хорошо смягчает кожу. Его вводят в состав различных косметических средств, используют в пищевой промышленности.
Химические свойства многоатомных спиртов во многом схожи со свойствами одноатомных спиртов. Для них характерны кислотные свойства (более сильные, чем у одноатомных спиртов, но все еще более слабые, чем у воды); реакции замещения групп –ОН; образование сложных эфиров; различные виды дегидратации и окисления.
Особенность их реакционной способности состоит в том, что две или три группы –ОН во многих случаях реагируют независимо друг от друга, Так, при действии щелочных металлов на этиленгликоль сначала замещается атом водорода у одной гидроксильной группы, а затем и у второй:
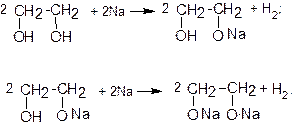
Обладая несколько более сильными кислотными свойствами по сравнению с одноатомными спиртами, многоатомные спирты вступают в реакцию с гидроксидами некоторых переходных металлов, например, со свежеосажденным гидроксидом меди (II).
При этом голубой осадок Cu(OH)2 растворяется, и наблюдается образование ярко-синего гликолята меди:
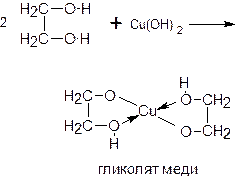 .
.
Эта реакция характерна и для других многоатомных спиртов и является качественной реакцией, позволяющей обнаружить в составе органического вещества наличие нескольких гидроксильных групп.
Замещение групп –ОН на галоген в случае многоатомных спиртов также происходит поочередно, причем первая гидроксильная группа замещается легче, а вторая – труднее:
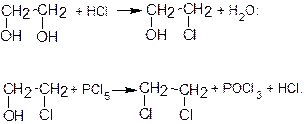
Многоатомные спирты, как и одноатомные, взаимодействует с органическими и неорганическими кислотами с образованием сложных эфиров, например:
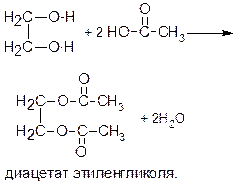
Особенно важны в практическом отношении сложные эфиры глицерина. Так, сложные эфиры глицерина и высших карбоновых кислот (например, стеариновой С17Н35-СООН, олеиновой С17Н33-СООН) представляют собой жиры, примером которых может служить тристеарат глицерина – твердый жир животного происхождения:
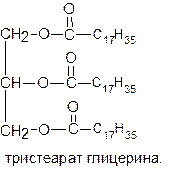
При взаимодействии глицерина с азотной кислотой можно получить соответствующий сложный эфир ‑ тринитрат гицерина:
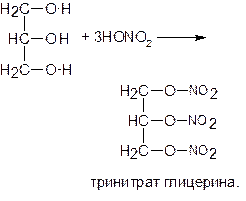
Тринитрат глицерина (нитроглицерин) – взрывчатое вещество и одновременно лекарственный препарат: его 1%-й спиртовой раствор применяют в медицине в качестве сосудорасширяющего средства.
Двухатомные спирты можно получить при «мягком» окислении алкенов водным или слабощелочным раствором перманганата калия
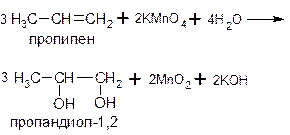
а также путем гидролиза соответствующих дигалогензамещенных алканов, например:
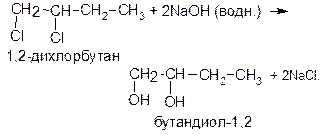
Глицерин образуется при гидролизе природных жиров, в промышленности его получают через ряд стадий из пропилена.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Даны вещества:
| а) |
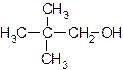
| г) | 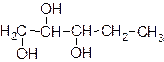
|
| б) | 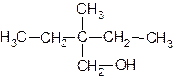
| д) | 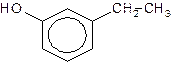
|
| в) | 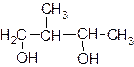
| е) | 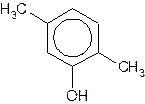
|
Назовите каждое из веществ в соответствии с правилами номенклатуры ИЮПАК.
2. Даны вещества
| а) б) в) г) д) е) | 2,3,4-триметилпентанол-1; 4-метил-3-этилпентанол-2; 2-метилпропандиол-1,3; бутантриол-1,2,4; 3,4-диэтилфенол; 2,4,6-тринитрофенол. |
Напишите структурные формулы этих веществ.
3. Напишите структурные формулы всех спиртов, изомерных диэтиловому эфиру, дайте им названия. Укажите среди записанных вами веществ два первичных спирта, вторичный и третичный спирты.
4. Напишите уравнения следующих реакций, указывая условия их протекания:
а) пропанола-2 с натрием;
б) 2-метилбутанола-2 с хлороводородом;
в) метанола с пентахлоридом фосфора;
г) этиленгликоля с бромоводородом;
д) фенола с бромной водой;
е) гидрирования 2-метилфенола.
5. Напишите уравнения реакций межмолекулярной и внутримолекулярной дегидратации пропанола-1. Укажите, в каких условиях преимущественно образуется простой эфир, а в каких – алкен.
6. Напишите уравнения реакций с участием метанола, приводящих к образованию
а) диметилового эфира;
б) метилового эфира уксусной кислоты.
Какое из этих веществ относится к простым, а какое – к сложным эфирам?
7. Закончите следующие уравнения реакций окисления спиртов (не забудьте подобрать коэффициенты):
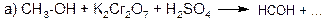
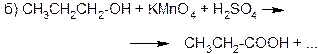
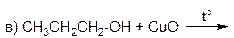
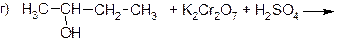
8. Напишите уравнения реакций получения пропанола‑2 и пропандиола‑1,2
а) из пропилена;
б) из хлорзамещенных алканов соответствующего строения.
9. Гидратацией каких двух алкенов можно получить 2‑метилбутанол‑2? Напишите уравнения соответствующих реакций. Почему с помощью реакции гидратации нельзя получить 2‑метилбутанол‑1?
10. В одной из пробирок находится этиленгликоль, во второй – этиловый спирт, в третьей – водный раствор фенола. Приведите уравнения реакций, позволяющих различить эти вещества.
11. При нагревании смеси этилового и пропилового спиртов с концентрированной серной кислотой может образоваться пять новых органических веществ: два алкена и три простых эфира. Назовите эти вещества, напишите уравнения реакций, которые приводят к их образованию.
12. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а)
 ;
;
б)
 ;
;
в)
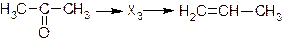
13. Напишите уравнения реакций, позволяющих через ряд стадий получить:
а) бутадиеновый каучук из этанола;
б) 2,3-диметилбутан из изопропилового спирта;
в) 1,2-дибром-2-метилпропан из 2-метилпропанола-2.
14. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
гексан → бензол → хлорбензол→ фенолят натрия → →фенол → 2,4,6-трибромфенол.
15. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
карбид кальция → ацетилен → бензол → изопропилбензол → фенол → циклогексанол.
16. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
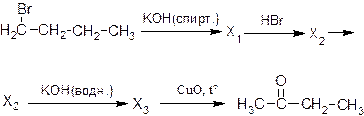
17. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
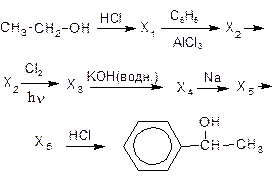
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 3743; Нарушение авторских прав?; Мы поможем в написании вашей работы!