
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методи проведення та вимоги до реакцій в якісному хімічному аналізі
|
|
|
|
Класифікація методів якісного аналізу
Якісний аналіз можна здійснювати або за допомогою хімічних реакцій, або використовуючи фізичні властивості складових речовини. Тому методи якісного аналізу поділяють на:
– хімічні – ґрунтуються на проведенні хімічних реакцій, які супроводжуються характерними зовнішніми ознаками – утворенням осаду, зміною кольору, появою запаху. Хімічний аналіз може проводитись як «мокрим» способом (реакції проводяться у розчині), так і «сухим» способом – пірохімічні реакції забарвлення полум’я (наприклад, йони К+ забарвлюють полум’я у фіолетовий колір) або забарвлення «перлів» (на платиновій дротинці в полум’ї пальника стоплюють зразок речовини з бурою, при цьому утворюється кулька, так званий «перл», за її забарвленням виявляють йони, що містились у зразку речовини).
– фізичні – ґрунтуються на спостереженні різних фізичних властивостей досліджуваної речовини, так спектральний метод заснований на дослідженні спектрів поглинання або випромінювання речовини, яку аналізують, люмінесцентний метод – на здатності речовини світитися в ультрафіолетовому випромінюванні. Ці методи не потребують проведення хімічних реакцій.
– фізико-хімічні (або інструментальні) – засновані на вимірюванні певних фізичних властивостей речовин (оптичної густини, сорбційних властивостей, питомої електропровідності) у процесі хімічної реакції, наприклад, спектрофотометрія, кондуктометрія, хроматографія та ін.
Для хімічного аналізу можна брати більші або менші кількості речовин, що досліджуються. Залежно від цього розрізняють макроаналіз (макрометод) – використовується для аналізу 0,1-1 г речовини, такий аналіз виконується у пробірках, напівмікроаналіз (напівмікрометод) – використовується 0,01 - 0,1 г речовини, виконується у звичайних або мікропробірках, мікроаналіз (мікрометод) – використовується не більше 0,01 г речовини, такий аналіз можна виконувати краплинним способом на смужках фільтрувального паперу або годинниковому склі (можна виконувати аналіз на поставленій догори дном колбі або стакані). Оскільки зовнішній ефект реакції не залежить від кількості взятої речовини для дослідження, то в більшості випадків користуються напівмікрометодом. Іноді треба дослідити якісний і кількісний склад речовини при незначній її кількості. У таких випадках застосовують ультрамікроаналіз, коли для аналізу беруть дуже малу кількість речовини, а зовнішній ефект реакції спостерігають під мікроскопом.
Хімічні реакції, які застосовуються в якісному хімічному аналізі повинні мати характерні зовнішні ознаки, тобто володіти так званим аналітичним ефектом. Реакції, які супроводжуються зовнішніми ознаками, називають аналітичними або якісними. Якісні реакції за допомогою яких можна визначити певний йон або речовину, відрізнити цей йон чи речовину від інших називають індивідуальними або характерними. Однак для виявлення певного йону за допомогою характерної для нього реакції, цей йон необхідно відокремити від інших йонів розчину, оскільки сторонні йони можуть заважати виявленню, утворюючи осади, забарвлення і маскуючи таким чином характерні зовнішні ознаки індивідуальної реакції на йон, який виявляють.
Є реакції, проведенню яких не заважають сторонні йони. Такі реакції називаються специфічними, але таких реакцій дуже мало. Наприклад, специфічною є характерна реакція на Fe3+-йон – взаємодія з калій гексаціанофератом (ІІ) у слабокислому середовищі. При цьому утворюється темно-синій осад берлінської блакиті:
Fe3+ + K4[Fe(CN)6] ® KFe[Fe(CN)6]¯ + 3K+
Реакції, які дають однаковий аналітичний ефект з декількома йонами називаються вибірковими або селективними. Наприклад, Cl–-іони, утворюють білий осад з Ag+, Hg22+, Pb2+-іонами. До селективних відносяться так звані групові реакції, які призначені для виявлення певної групи йонів.
До важливих умов, необхідних для виконання характерної реакції, також відносяться:
ü кислотність середовища, наприклад, осади, які розчиняються в кислотах і лугах можна одержати лише в нейтральному середовищі;
ü температура розчину;
ü концентрація йону, достатня для його виявлення в розчині.
З останньою умовою пов’язана чутливість хімічної аналітичної реакції, адже чим меншу кількість речовини можна виявити за тією або іншою реакцією, тим вона чутливіша. Найменшу кількість речовини або йонів, яку можна виявити за допомогою тієї чи іншої реакції за певних умов, називають відкриваємим мінімумом. Ця величина є дуже малою і виражається у мікрограмах (мкг) і звичайно позначається грецькою літерою g: 1g=1мкг=10-6г.
Чутливість реакції характеризують не лише абсолютною кількістю речовини, а й значенням концентрації йону або речовини в розчині.
Найменша концентрація речовини або йону в розчині, при якій їх ще можна виявити за даною реакцією, називається граничним розведенням. Граничне розведення – відношенням одиниці маси речовини або йонів (г) до об’єму розчинника (см3).
Приклад. Приготовано 500 см3 розчину, в якому міститься 1 г йонів, які виявляють. Встановлено, що при розведенні цього об’єму у 20 раз, в одній краплині об’ємом 0,02 см3 ще можна виявити шукані йони. Скільки буде складати граничне розведення та відкриваємий мінімум у цьому випадку?
Рішення: Граничне розведення h = 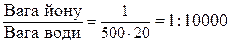 .
.
Після цього знаходимо відкриваний мінімум: 10 000 – 1 г
0,02 – х.
Звідси х = 0,02: 10 000 = 2 × 10-6 г = 2g.
Слід зазначити, що для багатьох якісних реакцій має значення кількість добавленого реактиву. Переважно реактив добавляють у надлишку, але не надто великому, щоб в разі утворення утворений осаду він не розчинився.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1739; Нарушение авторских прав?; Мы поможем в написании вашей работы!