
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основні закони масопередачі
|
|
|
|
В процесах переносу речовини, що розподіляється, з однієї фази в іншу розрізняють два випадки:
переніс з потоку рідини в потік рідини, або масообмін між потоками рідини;
переніс з твердого тіла в потік рідини (або переніс у зворотному напрямку), тобто
масообмін між твердою фазою і потоком рідини.
Елементарними законами, котрим підчиняється переніс речовини, що розподіляється, з однієї фази в іншу, є закон молекулярної дифузії, закон масовіддачі і закон масопровідності.
8.9 Закон молекулярної дифузії (перший закон Фіна)
Молекулярна дифузія в газах і розчинах рідин відбувається в результаті хаотичного руху молекул, не пов'язаного з рухом потоку рідини. Відбувається переніс молекул речовини, що розподіляється, з області високих концентрацій в область низьких концентрацій. Кінетика переносу відповідає в цьому випадку першому закону Фіка: кількість продифундованої речовини пропорційна градієнту концентрацій, площі, перпендикулярній напрямку дифузійного потоку і часу.
 (8.9.1)
(8.9.1)
де dM - кількість продифундованої речовини;
дС/дХ - градієнт концентрацій в напрямку дифузії;
dF - елементарна площадка, через яку проходить дифузія;
dr- тривалість дифузії;
D - коефіцієнт пропорційності, або коефіцієнт дифузії.
З рівняння (8.7.4.) випливає:
коефіцієнт дифузії показує, яка кількість речовини дифундує через поверхню 1м2 протягом 1с при різниці концентрацій на відстані 1м. рівній одиниці.
Знак мінус в правій частині рівняння показує, що при молекулярній дифузії в напрямку переміщення речовини концентрація зменшується.
Очевидно, що спосіб вираження концентрації і її розмірність визначають розмірність коефіцієнта дифузії.
Якщо прийняти одиниці вимірів [М]=кг, [F]=m2, [т]=с, [С]=кг/м3, [Х]=м, то одиниця виміру D буде:
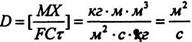
Чисельні значення коефіцієнту дифузії беруться з довідника або знаходяться з наступних формул:
для газів
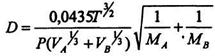 (8.9.2)
(8.9.2)
для рідин
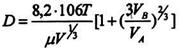 (8.9.3)
(8.9.3)
де Т-абсолютна температура, К;
Р -тиск, Па;
V і V - мольні об'єми взаємодіючих речовин, см3/моль;
МА і Мв – мольні маси, кг/моль;
μ - в'язкість рідини, в котрій відбувається дифузія,
Коефіцієнт дифузії залежить від агрегатного стану системи (D для газів приблизно на чотири степені вище, ніж для рідин). Коефіцієнт дифузії збільшується зі збільшенням температури і зменшується з підвищенням тиску. Коефіцієнт дифузії в рідинах (на відміну від газів) суттєво змінюється зі зміною концентрації.
Формула (8.9.3.) справедлива лише для розбавлених розчинів. Для концентрованих розчинів необхідний відповідний перерахунок, для якого рекомендується наступна залежність:
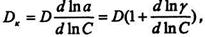 (8.9.4)
(8.9.4)
де Dx - коефіцієнт дифузії в розчині з концентрацією С; а - активність дифундуючої речовини; С - концентрація дифундуючої речовини; γ - коефіцієнт активності.
8.10 Диференційне рівняння молекулярної дифузії (другий закон Фіка)
Для виведення диференційного рівняння молекулярної дифузії виділимо в нерухомому середовищі або в рухомому ламінарному потоці елементарний паралелепіпед з ребрами dx, dy, dz (рис. 8.9.1).
Якщо через цей елементарний паралелепіпед за рахунок молекулярної дифузії переміщується речовина, що розподіляється, то через ліву задню і нижню грань за час dτ в нього входять кількості речовини, відповідно Мх, My, Мz, а через протилежні грані - праву, передню і верхню - виходять кількості речовини відповідно Mx+dx,My+dy,Mz+dz. Отже, елемент за час dτ набуває дифундуючої речовини в кількості
dM=(Mx - Mx+dx)+(My- My+dy)+(Mz - Mz+dz).
При цьому концентрація дифундуючої речовини підвищується на 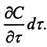
Згідно основного закону молекулярної дифузії,
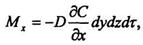

Отже,
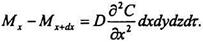
Аналогічно знайдемо:
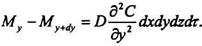
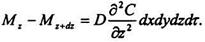
Складемо ліві та праві частини останніх рівнянь, отримаємо:
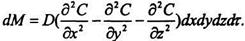 (8.10.1)
(8.10.1)
З іншої сторони, той же приріст кількості дифундуючої речовини в елементі можна знайти множенням об'єму елемента на зміну концентрацію за час dτ, тобто
 (8.10.2).
(8.10.2).
Співставимо вирази (8.10.1) і (8.10.2) і отримаємо диференційне рівняння
молекулярної дифузії:
 (8.10.3)
(8.10.3)
8.11 Закон масовіддачі (закон Щукарева )
Основний закон масовіддачі, або конвективної дифузії, був вперше сформульований Щукаревим при вивченні кінетики розчинення твердих тіл.
Він може бути сформульован так:
кількість речовини перенесеної від поверхні розподілу фаз у сприймаючу фазу, пропорційна різниш концентрацій у поверхні розподілу Фаз і в ядрі потоку сприймаючої фази, поверхні фазового контакту і часу ( рис..8.11.2):
d2M = p(Cr-Cf )dFdτ, (8.11.1)
де β- коефіцієнт масовіддачі - характеризує переніс речовини конвективними і дифузійними потоками одночасно; Сr - концентрація у сприймаючій фазі біля поверхні розподілу фаз; С f - концентрація в ядрі потоку сприймаючої фази.
При цьому слід зазначити, що концентрація на границі розглядається як рівноважна концентрація.
Якщо прийняти одиницю виміру
[М]=кг, [F]=m2, [ τ ]=с, [С]=кг/м3, то одиниця виміру β буде:
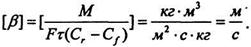
Коефіцієнт масовіддачі показує, яка кількість речовини передається від поверхні розподілу фаз у сприймаючу Фазу через один м2 поверхні Фазового контакту протягом 1с при різниці концентрацій, рівній одиниці.

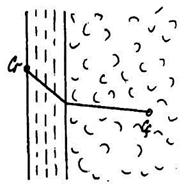
Рис. 8.11.1. До виводу диференційного рівняння молекулярної дифузії
Рис.8.11.2. До визначення закону конвективної дифузії.
8.12 Диференційне рівняння масовіддачі (конвективної дифузії)
В основу розгляду явищ конвективної дифузії покладено теорію дифузійного граничного шару. Згідно цієї теорії (рис.8.11.2), речовина, що розподіляється, переноситься з ядра потоку рідини до границі розподілу фаз безпосередньо потоками рідини і молекулярною дифузією. В системі, що розглядається, потік можна вважати таким, який складається з двох частин: ядра і граничного дифузійного шару. В ядрі переніс речовини здійснюється переважно струменями рідини в умовах турбулентності течії; концентрація речовини, що розподіляється, в даному перерізі в умовах стаціонарного режиму зберігається постійною по мірі наближення до граничного дифузійного шару турбулентний переніс затухає, з приближенням до границі починає переважати переніс за рахунок молекулярної дифузії. Відповідно до цього з'являється градієнт концентрації речовини, що розподіляється, що зростає з приближенням до границі.
При наявності конвективної дифузії концентрація речовини, що розподіляється, в елементарному об'ємі фази (див. рис. 8.11.1) змінюється не лише в наслідок молекулярної дифузії, але також і в результаті механічного переносу його із зони однієї концентрації в другу. В цьому випадку концентрація речовини, що розподіляється, буде функцією не лише координат х, у, z і часу т, але складовою швидкості переміщення елемента ωх, ωy, ωz.
При конвективній дифузії елемент переміщується з однієї точки простору в іншу. В цьому випадку зміна концентрації розподіляючої речовини в елементі може бути виражено за допомогою субстанційної похідної, котра враховує зміну величини з часом і зміни, пов'язані з переміщенням елемента з однієї точки простору в другу:
 (8.12.1)
(8.12.1)
В рівнянні (8.12.1)  являє собою локальну зміну концентрації речовини, що розподіляється, а
являє собою локальну зміну концентрації речовини, що розподіляється, а  – конвективну зміну концентрації.
– конвективну зміну концентрації.
Якщо в рівнянні молекулярної дифузії (8.10.3) замінити локальну зміну концентрації
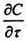 повним
повним  , згідно (8.12.1),. то в результаті отримаємо диференційне рівняння конвективної дифузії:
, згідно (8.12.1),. то в результаті отримаємо диференційне рівняння конвективної дифузії:
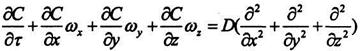 (8.12.2)
(8.12.2)
Це рівняння є математичним описанням процесу переміщення в рідкій (газовій) фази конвективної дифузії.
8.13 Рівняння подібності конвективної дифузії.
Кількість речовини, що розподіляється, яка перемішується з фази в фазу біля границі, можна визначити виходячи з основного закону конвективної дифузії:
dM = β(C2-Cf )dFdτ
Позначимо (С2 - Сf ) = ΔС, отримаємо
dM = βΔCdFdτ. (8.13.1)
Цю ж кількість речовини dM можна знайти і іншим методом. Біля поверхні розподілу фаз речовина переміщується в другу фазу внаслідок молекулярної дифузії. Кількість переданої із фази в фазу речовини dM можна знайти виходячи з основного рівняння молекулярної
дифузії: dM = -D· дС/дх ·dFdτ
Величина dM в останньому рівнянні і рівнянні (8.13.1) є однією і тією ж кількістю речовини, вираженою різними способами, отже
 (8.13.2)
(8.13.2)
Рівняння (8.13.2) характеризує умови на границі фаз, що розглядаються. Для отримання безрозмірних дифузійних чисел подібності перетворимо рівняння (8.12.2) і (8.13.2) методами теорії подібності. З рівняння (8.13.2) діленням обох частин рівняння на праву частину рівняння отримаємо безрозмірний комплекс βΔСдх/DдC.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1918; Нарушение авторских прав?; Мы поможем в написании вашей работы!