
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Условие равновесия в гетерогенной системе
Условие термодинамического равновесия в растворе
Взаимосвязь между энергией Гиббса раствора и химическими потенциалами отдельных компонентов описывается уравнением (2.3):
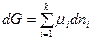
Приняв, что химический потенциал является постоянной величиной, проинтегрируем полученное уравнение:
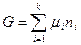
Продифференцируем теперь при условии переменных массы раствора и его состава:
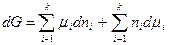
При равновесии dG = 0, тогда
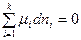 ,
,
следовательно,
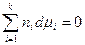 .
.
Разделим на 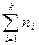 :
:
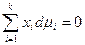 , (2.4)
, (2.4)
где 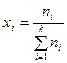 – мольная доля i -го компонента.
– мольная доля i -го компонента.
Уравнение (2.4) – уравнение Гиббса-Дюгема – является условием равновесия в гомогенном многокомпонентном растворе.
Для двухкомпонентного раствора условие равновесия имеет вид:
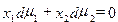 .
.
Рассмотрим систему, состоящую из k независимых компонентов и m фаз, находящуюся в состоянии термодинамического равновесия при р, Т = const. Общее условие равновесия в системе имеет вид:
dG = 0.
Общая энергия Гиббса складывается из энергий Гиббса каждой из фаз:
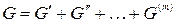 .
.
Продифференцируем:
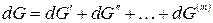 .
.
Для каждой из фаз
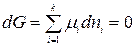 .
.
Подставим значение dG для каждой фазы:
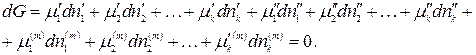
Пусть без нарушения равновесия из первой фазы во вторую перешло бесконечно малое число моль 1-го компонента. При этом числа моль всех остальных компонентов постоянны во всех фазах и значения внешних параметров не изменяются: р, Т = const. Тогда условие равновесия приобретает вид:
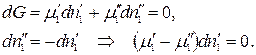
Произведение равно нулю, если хотя бы один из множителей равен нулю, но согласно условию 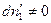 , тогда
, тогда
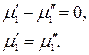
Следовательно, химический потенциал первого компонента одинаков в обеих фазах. Рассматривая аналогичные частные случаи для других компонентов и фаз, получим:
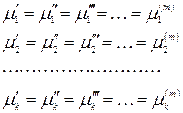
Полученное уравнение является условием равновесия в m -фазной
k -компонентной системе и называется теоремой равновесия Гиббса:
условием термодинамического равновесия в гетерогенной системе является равенство химических потенциалов каждого компонента во всех фазах при Р, Т = const или V, Т = const
В качестве примера рассмотрим двухфазную трехкомпонентную систему. Условие равновесия для такой системы имеет вид:
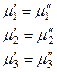 ,
,
где 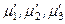 – химические потенциалы 1, 2 и 3-го компонентов в одной фазе;
– химические потенциалы 1, 2 и 3-го компонентов в одной фазе;
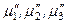 – химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
– химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
|
|
Дата добавления: 2013-12-11; Просмотров: 301; Нарушение авторских прав?; Мы поможем в написании вашей работы!