
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физические свойства. Четыре первых представителя ряда метана – газообразные вещества, начиная с пентана (С5) до гексадекана (С16) углеводороды нормального строения – жидкости
|
|
|
|
Четыре первых представителя ряда метана – газообразные вещества, начиная с пентана (С5) до гексадекана (С16) углеводороды нормального строения – жидкости, С17 и выше – твёрдые вещества.
Алканы с разветвлённой цепью углеродных атомов кипят при более низких температурах по сравнению с алканами нормального строения; с увеличением числа заместителей, превращением молекул в более разветвлённые, разница в температурах кипения алканов нормального и разветвлённого строения возрастает.
Все алканы легче воды, их плотность не превышает 0,8 г/∙см-3.
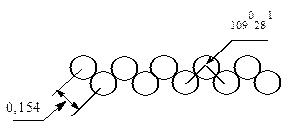
Алканы практически не растворимы в воде, но хорошо растворимы в органических растворителях. Метан, этан и высшие гомологи не имеют запаха, средние обладают запахом бензина. В молекулах алканов цепочки углеродных атомов имеют зигзагообразную форму. Угол между валентностями составляет 1090281; центры углеродных атомов расположены друг от друга на расстоянии 0,154 нм, расстояние от центра углеродного атома до центра атома водорода 0,11 нм.
В процессе разработки месторождений физическое состояние и свойства углеводородов с изменением температуры и давления не остаются постоянными. Для правильного установления технологического режима эксплуатации месторождений и систем сбора нефти и газа необходимо знать изменение состояний и свойств углеводородов в широком диапазоне давления и температуры.
Химические свойства и переработка
В молекулах алканов, как известно, все атомы связаны между собой прочными σ-связями, а валентности углеродных атомов полностью насыщены водородом. Поэтому алканы не вступают в реакции присоединения. Они проявляют при обычных условиях чрезвычайно высокую химическую инертность: не взаимодействуют с ионными реагентами (кислотами, щелочами), окислителями, активными металлами (поэтому, например, металлический натрий можно хранить в керосине).
По этой причине предельные углеводороды в своё время получили название парафинов* (от лат. рarum affinis - малое сродство).
Основные химические превращения алканов идут только при сообщении им достаточно высокой энергии (за счёт нагревания или УФ-облучения). При этом может произойти или разрыв связи С-Н с последующей заменой атома водорода на другой атом или группу атомов (реакции замещения), или же разрыв молекулы по связи С-С (реакции расщепления).

* - В нефтяной практике парфинами называют твёрдые углеводороды, содержащиеся в нефтях и нефтепродуктах(Вопрос что же такое парафины?).
Наибольший интерес для нефтехимии представляют следующие реакции:
Галогенирование. Эта реакция идёт сравнительно легко с замещением атомов водорода в алканах на галогены. Из галогенов наиболее широко используется хлор, вследствие его доступности, дешевизны и высокой химической активности.
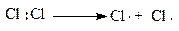
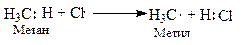
Молекулярный хлор под влиянием света расщепляется на атомный, который инициирует (начинает) радикальную реакцию; он отщепляет водород от метана, образуя радикал - метил и хлористый водород. Метильный радикал взаимодействует с молекулярным хлором и стабилизируется в первый продукт хлорирования метана - хлористый метил, который по аналогичной схеме подвергается дальнейшему хлорированию, образуя последовательно хлористый метилен, хлороформ и тетрахлорметан (четырёххлористый углерод):

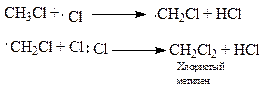
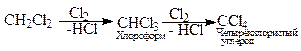
Подобно метану могут подвергаться хлорированию и другие алканы. Хлорирование углеводородов проводится в промышленных масштабах в паровой и жидкой фазах различными способами: при нагревании до 400-500 0С (термическое хлорирование), в присутствии катализаторов (каталитическое хлорирование) при специальном освещении реагирующих компонентов (фотохимическое хлорирование).
Хлорпроизводные метана и других низших алканов являются хорошими растворителями жиров, синтетических смол и каучуков. Их можно использовать и для очистки призабойной зоны нефтяных скважин от асфальто-смолистых и парафиновых отложений. Применяют также и при депарафинизации масел.
Хлорпроизводные алканов используют для получения спиртов, в том числе и высших спиртов.
При пропускании хлористого метила (или смеси его с хлорзамещёнными ароматическими углеводородами) над медно-кремниевым сплавом при 300 0С образуются алкил- и арилхлорсиланы которые являются исходным продуктом в синтезе кремнийорганических соединений, применяемых в производстве силиконовых жидкостей, консистентных смазок, смол и каучуков.
Хлорирование твёрдых парафинов осуществляют для получения присадок, понижающих температуру застывания масел (депрессорные присадки).
Нитрование. Нитрование алканов осуществляют с помощью азотной кислоты при температуре 200-450 0С. Нитрование всегда сопровождается частичным разложением углеводородов, что приводит к получению нитросоединений с меньшим числом атомов углерода.
Нитрометан, нитроэтан, нитропропан являются хорошими растворителями эфиров целлюлозы, полимеров, лаков. Они могут применяться в качестве добавок, снижающих температуру самовоспламенения дизельных топлив.
Восстановлением нитроалканов в кислой среде можно получить амины:
Амины используют для получения ингибиторов коррозии, поверхностно-активных веществ, для очистки газов от сероводорода.
Сульфирование. При слабом нагревании дымящая серная кислота сульфирует алканы, т. е. атом водорода в них замещается на сульфогруппу в результате образуются алкансульфокислоты.
Сульфохлорирование. При действии на алканы смеси сернистого газа и хлора идёт реакция сульфохлорирования. Сульфохлориды легко гидролизуются до сульфокислот.
Взаимодействием сульфохлоридов с избытком аммиака получают сульфамиды.
Сульфокислоты могут быть получены также и реакцией сульфоокисления.
Алкансульфокислоты образуют со щелочами соли – сульфонаты.
Сульфонаты и сульфамиды с 12-18 и выше атомами углерода, получаемые на основе жидких парафинов, выделяемых из дизельных фракций, служат в качестве поверхностно-активных и моющих веществ, эмульгаторов нефти и флотационных реагентов.
Дегидрирование. В присутствии катализатора при нагревании из алканов за счёт разрыва связи С-Н происходит отщепление атомов водорода, что приводит к образованию алкенов.
Особенно важен процесс дегидрирования бутана с целью получения бутадиена, который необходим для синтеза каучуков
Дегидрированием изопентана, выделяемого из газового бензина и газов нефтепереработки, получают изопрен, также важный полупродукт для синтеза каучуков.
Окисление. В присутствии большого избытка кислорода (или воздуха) при высокой температуре алканы сгорают полностью до воды и диоксида углерода. Эта реакция используется, главным образом, при получении из природного газа и нефтепродуктов тепловой энергии.
Окислением метана и продуктов его окисления можно получить метиловый спирт, формальдегид, муравьиную кислоту.
Метиловый спирт применяют в качестве горючего, растворителя, для предотвращения образования газовых гидратов в трубопроводах.
Формальдегид применяется во многих органических промышленных синтезах, большое количество его используется для получения пластмасс, пластификаторов, взрывчатых веществ. Применяют также для предотвращения бактериальной коррозии металлов.
Продукты окисления низших алканов находят применение в качестве готовой продукции или полупродуктов при синтезе присадок, моющих средств, алкилирующих агентов, компонентов ракетного топлива, растворителей.
И многие другие)
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 722; Нарушение авторских прав?; Мы поможем в написании вашей работы!