
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Префиксы и суффиксы для обозначения некоторых характеристических групп
|
|
|
|
| Характеристическая группа | Префикс | Суффикс |
- (С)OOH*
- СООН
- SO3H
- (С)H -O
СH- O
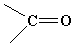 - OH
- SH
- NH2
- OH
- SH
- NH2
| карбокси сульфо- оксо- формил- оксо- гидрокси- мерканто- амино- | -овая кислота -карбоновая кислота -сульфокислота -аль -карбальдегид -он -ол -тиол -амин |
| - NO2 - OR - F, - Cl, - Br, -I (- Hal) | нитро- алкокси- фтор-, хлор-, бром-, иод- (галоген-) | |
* Атом углерода, заключенный в скобки, входит в состав главной углеродной цепи.
Как видно из таблицы, некоторые характеристические группы, а именно галогены, нитро- и алкоксигруппы, отражаются в общем названии только в виде префиксов, например бромметан, этоксиэтан, нитробензол.
Нумерацию атомов углерода в главной цепи начинают с того конца цепи, ближе к которому расположена старшая группа. Если таких возможностей оказывается несколько, то нумерацию проводят таким образом, чтобы либо кратная связь, либо другой заместитель, имеющийся в молекуле, получили наименьший номер.
В карбоциклических соединениях нумерацию начинают от того атома углерода, при котором находится старшая характеристическая группа. Если при этом невозможно выбрать однозначную нумерацию, то цикл нумеруют так, чтобы заместители имели наименьшие номера.
В группе циклических углеводородов особо выделяются ароматические углеводороды, для которых характерно наличие в молекуле бензольного кольца. Некоторые широко известные представители ароматических углеводородов иих производных имеют тривиальные названия, использование которых разрешено правилами ИЮПАК: бензол, толуол, фенол, бензойная кислота.
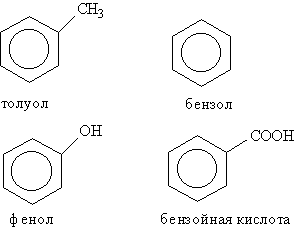
Радикал С6Н5-, образованный из бензола, называется фенил, а не бензил. Бензилом называют радикал С6Н5СН2-, образованный из толуола.
Составление названия органического соединения. Основу названия соединения составляет корень слова, обозначающий предельный углеводород с тем же числом атомов, что и главная цепь (мет-, эт-, проп-, бут-, пент: гекс- и т. д.). Затем следует суффикс, характеризующий степень насыщенности, -ан, если в молекуле нет кратных связей, -ен при наличии двойных связей и -ин для тройных связей, (например пентан, пентен, пентин). Если кратных связей в молекуле несколько, то в суффиксе указывается число таких связей: -диен, -триен, а после суффикса обязательно арабскими цифрами указывается положение кратной связи (например, бутен-1, бутен-2, бутадиен-1,3):
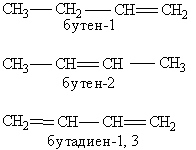
Далее в суффикс выносится название самой старшей характеристической группы в молекуле с указанием ее положения цифрой. Прочие заместители обозначаются с помощью приставок. При этом они перечисляются не в порядке старшинства, а по алфавиту. Положение заместителя указывается цифрой перед приставкой, например: 3-метил; 2-хлор и т. п. Если в молекуле имеется несколько одинаковых заместителей, то перед названием соответствующей группы словом указывается их количество (например, диметил-, трихлор- и т. д.). Все цифры в названиях молекул отделяются от слов дефисом, а друг от друга запятыми. Углеводородные радикалы имеют свои названия.
Предельные углеводородные радикалы:
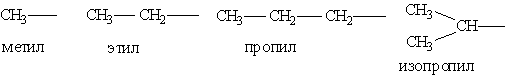
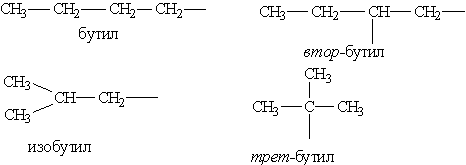
Непредельные углеводородные радикалы:
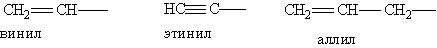
Ароматические углеводородные радикалы:
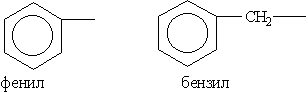
В качестве примера назовем следующее соединение:
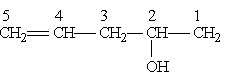
1) Выбор цепи однозначен, следовательно, корень слова — пент; далее следует суффикс -ен, указывающий на наличие кратной связи;
2) порядок нумерации обеспечивает старшей группе (—ОН) наименьший номер;
3) полное название соединения заканчивается суффиксом, обозначающим старшую группу (в данном случае суффикс -ол указывает на наличие гидроксильной группы); положение двойной связи и гидроксильной группы указывается цифрами.
Следовательно, приведенное соединение называется пентен-4-ол-2.
Тривиальная номенклатура представляет собой совокупность несистематических исторически сложившихся названий органических соединений (пример: ацетон, уксусная кислота, формальдегид и т. д.).
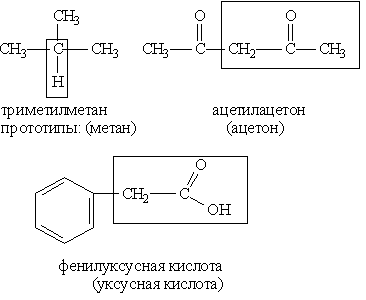
Рациональная номенклатура позволяет строить название вещества на основании его структуры с более простым соединением, выбранным в качестве прототипа. Способ такого построения иллюстрируют следующие примеры:
Изомерия. Выше было показано, что способность атомов углерода к образованию четырех ковалентных связей, в том числе и с другими атомами углерода, открывает возможность существования нескольких соединений одного элементного состава — изомеров. Все изомеры делят на два больших класса — структурные изомеры и пространственные изомеры.
Структурными называют изомеры, отвечающие различным структурным формулам органических соединений (с разным порядком соединения атомов).
Пространственные изомеры имеют одинаковые заместители у каждого атома углерода и отличаются лишь их взаимным расположением в пространстве.
Структурные изомеры. В соответствии с приведенной выше классификацией органических соединений по типам среди структурных изомеров выделяют три группы:
1) соединения, содержащие различные функциональные группы и относящиеся к различным классам органических соединений:

2) соединения, отличающиеся углеродными скелетами:
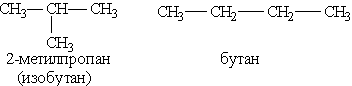
3) соединения, отличающиеся положением заместителя или кратной связи в молекуле:
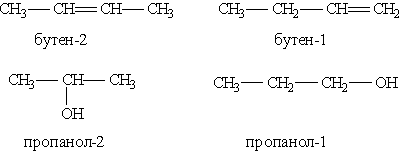
Пространственные изомеры (стереоизомеры). Стереоизомеры можно разделить на два типа: геометрические изомеры и оптические изомеры.
Геометрическая изомерия характерна для соединений, содержащих двойную связь или цикл. В таких молекулах часто возможно провести условную плоскость таким образом, что заместители у различных атомов углерода могут оказаться по одну сторону (цис-) или по разные стороны (транс-) от этой плоскости. Если изменение ориентации этих заместителей относительно плоскости возможно только за счет разрыва одной из химических связей, то говорят о наличии геометрических изомеров. Геометрические изомеры отличаются своими физическими и химическими свойствами.
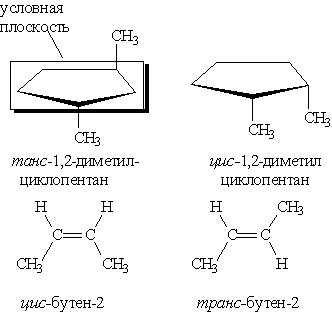
Оптическими изомерами называют молекулы, зеркальные изображения которых не совместимы друг с другом.
Таким свойством обладают молекулы, имеющие асимметрический центр — атом углерода, связанный с четырьмя различными заместителями. Например, в виде двух оптических изомеров существует молекула молочной кислоты СН3СН(ОН)—СООН, содержащая один асимметрический центр.
Взаимное влияние атомов в молекуле. Молекула органического соединения представляет собой совокупность атомов, связанных в определенном порядке, как правило, ковалентными связями. При этом связанные атомы могут различаться по величине электроотрицательности. Величины электроотрицательностей в значительной степени определяют такие важнейшие характеристики связи, как полярность и прочность (энергия образования). В свою очередь, полярность и прочность связей в молекуле в значительной степени определяют возможности молекулы вступать в те или иные химические реакции.
Электроотрицательность атома углерода зависит от состояния его гибридизации. Это связано с долей s-орбитали в гибридной орбитали: она меньше у sр3- и больше у sр2- и sр -гибридизованных атомов.
Лекция: Основные теоретические положения органической химии.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 2140; Нарушение авторских прав?; Мы поможем в написании вашей работы!