
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства
|
|
|
|
Физические свойства
Газов в гомологическом ряду нет. Это жидкости. Начиная с С12Н25ОН до С20Н41ОН – маслообразные и с С21Н43ОН — твердые вещества.
Ткип СН3ОН=65 °С, Ткип С2Н5ОН=78 °С, r(С2Н5ОН)=0,8 г/см3
Первичные спирты изостроения имеют более низкие температуры кипения, чем нормальные первичные спирты.
В спиртах имеет место ассоциация молекул друг с другом за счет образования водородной связи. [Длина водородной связи больше обычной связи –ОН, а прочность значительно меньше (раз в 10).] Поэтому метанол-жидкость, а метан-газ. Чтобы разрушить водородные связи, надо затратить энергию; это может быть осуществлено при нагревании спирта.
Спирты легче воды: их плотности меньше 1. Метиловый, этиловый и пропиловый спирты смешиваются с водой во всех соотношениях. По мере усложнения углеводородных радикалов растворимость спиртов резко падает. Бутиловый спирт растворяется частично. Высшие спирты в воде не растворяются, т.е. выталкиваются из воды.
Из сказанного можно сделать вывод, что растворимые спирты можно тушить разбавлением (до концентрации менее 25 %); не растворимые в воде спирты водой тушить не рекомендуется, т.к. при этом спирты всплывают на поверхность воды и процесс горения продолжается. Водные растворы содержащие 25 % спирта и более - являются ЛВЖ. Следует отметить, что разбавленные растворы спиртов относятся к категории трудно горючих веществ, т.е. склонны гореть в присутствии источника зажигания.
1.Спирты реагируют со щелочными металлами (Na, K и т.д.) с образованием алкоголятов:
2R—OH + 2Na ® 2R—ONa + H2
Реакция протекает не так бурно, как при использовании воды. Причем с увеличением молярной массы спирта его активность в указанной реакции уменьшается. Первичные спирты значительно активнее в реакциях со щелочными металлами, чем изомерные им вторичные и, особенно, третичные.
Спирты в данной реакции проявляют свойства кислот, но они еще более слабые кислоты, чем вода: Кдис Н2О=10-16; Кдис CH3OH=10-17; Кдис C2H5OH = 10-18. Последнее объясняется влиянием радикала на алкильную группу (R- доноры).
Практически же спирты нейтральные вещества: они не показывают ни кислой, ни щелочной реакции на лакмус, не проводят электрического тока.
2
Способы получения
В свободном виде в природе спирты встречаются редко.
1. Большое количество этилового спирта, а также пропиловый, изобутиловый и амиловый спирты получают из природных сахаристых веществ в результате брожения. Например:
С6Н12О6 ¾¾¾® 2С2Н5ОН + 2СО2
глюкоза дрожжи
2. Из этиленовых углеводородов гидратацией:
CH2 H t оC, P
II + ½ ¾¾® CH3—CH2—OH OH
CH2 OH Zn, H2SO4 ½
CH3—CH2—CH=CH2 + H2O ¾® CH3—CH2—CH—CH3
H2SO4 (правило Марковникова)
3. Из ацетилена гидратацией (по реакции Кучерова):
НОН H2
СНºСН ¾¾® СН3—СН=О ¾¾® CH3—CH2—OH
Нg2+ Ni
4. При гидролизе галогеналкилов:
NaOH
СН3—СН2—СН2—СН2—Cl + HOH ¾® CH3—CH2—CH2—CH2OH+NaCl
(для смещения равновесия реакцию ведут в щелочной среде).
4. При восстановлении альдегидов водородом в момент выделения образуются первичные спирты, кетонов – вторичные:
R—CH + 2 H ® R—CH2 (первичный спирт)
II ½
альдегид O OH
R' R'
кетон ½ ½
R—C=O + 2 H ® R—CH—OH (вторичный спирт)
Отдельные представители.
Метиловый спирт. Следует отметить сильную ядовитость СН3ОН. В то же время он используется как растворитель, из него получают формальдегид (необходимый для производства пластмасс), им денатурируют этиловый спирт и используют как горючее. В промышленности его получают из смеси СО и Н2 под давлением над нагретым катализатором (ZnO и др.), при сухой перегонке древесины (древесный спирт):
СО + 2Н2 ® СН3ОН (метанол)
(Пары спирта с воздухом образуют взрывоопасные смеси. ЛВЖ, Твсп.=8 оС).
От контакта с сильными окислителями (дымящая HNO3), CrO3 и Na2O2 метанол самовозгорается.
Этиловый спирт (этанол, винный спирт). Бесцветная жидкость с характерным запахом и жгучим вкусом. С водой образует азеотроп (96 % С2Н5ОН + 4 % Н2О). Химическим способом (осушая CaO, CuSO4, Ca) можно получить абсолютный спирт. Используется при получении каучуков, а также как растворитель, в парфюмерии (духи, одеколоны), горючее, дезинфицирующее средство, алкогольный напиток, на его основе готовят лекарства. (ЛВЖ, Твсп.=13 оС). С добавкой ядовитых дурно пахнущих веществ он называется денатуратом. Получают спирт в результате брожения сахаристых веществ, из целлюлозы (гидролизный спирт), гидратацией этилена в присутствии серной кислоты, восстановлением уксусного альдегида водородом, уксусный альдегид в свою очередь получают по реакции Кучерова с использованием ацетилена (см. стр. 66). Добавка метилового и этилового спиртов к моторному топливу способствует полноте сгорания топлива и устраняет загрязнение атмосферы.
Физиологически этиловый спирт действует на организм как наркотик, к которому появляется пристрастие, и который разрушает психику.
Многоатомные спирты.
Двухатомные спирты называются гликолями, трехатомные – глицеринами. По международной заместительной номенклатуре двухатомные спирты называются алкандиолами, трехатомные – алкантриолами. Спирты сдвумя гидроксилами при одном углеродном атоме обычно в свободном виде не существуют; при попытках получить их они разлагаются, выделяя воду и превращаясь в соединение с карбонильной группой – альдегиды или кетоны:
 ОН
ОН
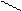 СН2 ® СН2=О + Н2О
СН2 ® СН2=О + Н2О
ОН


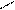 Трехатомные спирты с тремя гидроксилами при одном углеродном атоме еще более неустойчивы, чем аналогичные двухатомные, и в свободном виде неизвестны: ОН О
Трехатомные спирты с тремя гидроксилами при одном углеродном атоме еще более неустойчивы, чем аналогичные двухатомные, и в свободном виде неизвестны: ОН О
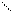
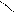 СН—ОН ® Н—С + Н2О
СН—ОН ® Н—С + Н2О
ОН ОН
муравьиная кис-та
Поэтому первым представителем двухатомных спиртов является производное этана состава С2Н4(ОН)2 с гидроксильными группами при различных углеродных атомах – 1,2-этандиол, или иначе - этиленгликоль (гликоль). Пропану соответствует уже два двухатомных спирта – 1,2-пропадиол, или пропиленгликоль, и 1,3-пропандиол, или триметиленгликоль:
СН2—СН2 СН2—СН—СН3 СН2—СН2—СН2
½ ½ ½ ½ ½ ½
ОН ОН ОН ОН ОН ОН
этиленгликоль пропиленгликоль триметиленгликоль
(1,2-этандиол) (1,2-пропандиол) (1,3-пропандиол)
Гликоли, в которых две спиртовые гидроксильные группы расположены в цепи рядом – при соседних атомах углерода, называются a-гликолями (например, этиленгликоль, пропиленгликоль). Гликоли со спиртовыми группами, расположенными через один углеродный атом, называются b-гликолями (триметиленгликоль). И так далее.
Среди двухатомных спиртов этиленгликоль представляет наибольший интерес. Он используется в качестве антифриза для охлаждения цилиндров автомобильных, тракторных и авиационных двигателей; при получении лавсана (полиэфир спирта с терефталевой кислотой).
Это бесцветная сиропообразная жидкость, не имеющая запаха, сладкая на вкус, ядовита. Смешивается с водой и спиртом. Ткип.=197 оС, Тпл.= —13 оС, d204=1,114 г/см3. Горючая жидкость.
Дает все реакции, характерные для одноатомных спиртов, причем в них может участвовать одна или обе спиртовые группы. Вследствие наличия двух ОН-групп гликоли обладают несколько более кислыми свойствами, чем одноатомные спирты, хотя и не дают кислой реакции на лакмус, не проводят электрического тока. Но в отличие от одноатомных спиртов они растворяют гидроксиды тяжелых металлов. Например, при приливании этиленгликоля к голубому студенистому осадку Cu(OH)2 образуется синий раствор гликолята меди:
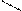 СН2—ОН CH2—O
СН2—ОН CH2—O
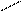 ½ + Cu(OH)2 ® ½ Cu + 2Н2О
½ + Cu(OH)2 ® ½ Cu + 2Н2О
СН2—ОН CH2—O
При действии PCl5 хлором замещаются обе гидроксидьные группы, при действии HCl – одна и образуются так называемые хлоргидрины гликолей:
СН2—СН2 CH2—CH2
½ ½ + 2PCl5 ® ½ ½ + 2POCl3 + 2HCl
OH OH Cl Cl
этиленгликоль 1,2-дихлорэтан
СН2—СН2 СН2—СН2
½ ½ + HCl ® ½ ½ + H2O
OH OH Cl OH
хлоргидрин этиленгликоля
При дегидратации из 2-х молекул этиленгликоля образуется диэтиленгликоль:
t
НО—СН2—СН2—ОН + НО—СН2—СН2—ОН ® НО(СН2)2—О—(СН2)2ОН
кат. диэтиленгликоль

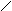
 Последний, может, выделяя внутримолекулярно одну молекулу воды, превращаться в циклическое соединение с двумя группами простого эфира – диоксан: СН2—СН2—ОН СН2—СН2
Последний, может, выделяя внутримолекулярно одну молекулу воды, превращаться в циклическое соединение с двумя группами простого эфира – диоксан: СН2—СН2—ОН СН2—СН2
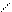
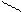
 О ¾® О О + Н2О
О ¾® О О + Н2О
СН2—СН2—ОН СН2—СН2
диэтиленгликоль диоксан
С другой сторон, диэтиленгликоль может реагировать со следующей молекулой этиленгликоля, образуя соединение тоже с двумя группами простого эфира, но с открытой цепью – триэтиленгликоль. Последовательное взаимодействие по такого рода реакции многих молекул гликоля приводит к образованию полигликолей – высокомелекулярных соединений, содержащих множество группировок простого эфира. Реакции образования полигликолей относятся к реакциям поликонденсации.
Полигликоли используются в производстве синтетических моющих средств, смачивателей, пенообразователей.
Окисление
При окислении первичные группы гликолей превращаются в альдегидные, вторичные - в кетонные группы.
Способы получения
Этиленгликоль получают щелочным гидролизом 1,2-дихлорэтана, а последний – хлорированием этилена:
2HOH
СН2=СН2 + Cl2 ® CH2Cl—CH2Cl ¾¾® CH2OH—CH2OH
Na2CO3
(давление)
Из этилена этиленгликоль может быть получен и путем окисления в водном растворе (реакция Е.Е. Вагнера, 1886): ОН ОН
[О] + НОН ½ ½
СН2=СН2 ¾¾¾® СН2—СН2
(KMnO4)
Глицерин СН2—СН2—СН2
½ ½ ½
ОН ОН ОН 1,2,3-пропантриол
В природе в свободном виде почти не встречается, но очень распространены и имеют большое биологическое и практическое значение его сложные эфиры с некоторыми высшими органическими кислотами – так называемые жиры и масла.
Используется в парфюмерии, фармации, в текстильной промышленности, в пищевой промышленности, для получения нитроглицерина и т.д. Это бесцветная горючая жидкость, без запаха, сладкая на вкус. (Следует сказать, что с увеличением числа групп ОН в молекуле сладость вещества увеличивается.) Очень гигроскопичен, смешивается с водой и спиртом. Ткип. 290 оС (с разложением), d204=1,26 г/см3. (Температуры кипения более высокие, чем у одноатомных спиртов – больше водородных связей. Это ведет к более высокой гигроксопичности и более высокой растворимости.)
Глицерин нельзя хранить с сильными окислителями: контакт с этими веществами приводит к возникновению пожара. (Например взаимодействие с KMnO4, Na2O2, CaOCl2 приводит к самовоспламенению.) Тушить рекомендуется водой и пеной.
Кислотность спиртовых групп в глицерине еще выше. В реакциях может участвовать одна, две или три группы. Глицерин также как и этиленгликоль растворяет Cu(OH)2, образуя интенсивно- синий раствор глицерата меди. Тем не менее, так же как одноатомные и двухатомные спирты, нейтрален на лакмус. Гидроксильные группы глицерина замещаются на галогены.
При действии водоотнимающих средств или при нагревании от глицерина отщепляется две молекулы воды (дегидратация). При этом образуется неустойчивый непредельный спирт с гидроксилом при углероде с двойной связью, который изомеризуется в непредельный альдегид акролеин (имеет раздражающий запах, как от дыма пригоревших жиров):
СН2—СН—СН2
½ ½ ½ ¾® СН2=С=СН—ОН ¾® СН2=СН—СНО
ОН ОН ОН -2Н2О промежуточный акролеин
непредельный спирт
При взаимодействии глицерина с азотной кислотой в присутствии Н2SO4 идет следующая реакция:
СН2—ОН НО—NO2 CH2—O—NO2
½ ½
CH—OH + HO—NO2 ¾® CH—O—NO2 + 3H2O
½ H2SO4 ½ азотнокислый эфир гли-
CH2—OH HO—NO2 CH2—O—NO2 церина (нитроглицерин)
(глицеринтринитрат)
Нитроглицерин – тяжелое масло (d15= 1,601 г/см3), не растворяется в воде, но хорошо растворимое в спирте и других органических растворителях. При охлаждении кристаллизуется (Тпл.=13 оС), очень ядовит.
Нитроглицерин – сильное бризантное взрывчатое вещество. [Синтезировал это соединение Альфред Нобель. На производстве этого соединения он создал себе колоссальное состояние. Проценты от того капитала используются до сих пор в качестве премиального фонда Нобелевских премий]. При ударе и детонации он мгновенно разлагается с выделением огромного количества газов:
4С3Н5(ОNO2)3 ® 12СО2 + 6N2 + О2 + 10Н2О
Для обеспечения безопасности при проведении взрывных работ им пользуются в виде так называемого динамита – смеси, состоящей из 75 % нитроглицерина и 25 % инфузорной земли (горная порода из кремнистых оболочек диатомовых водорослей). 1 % спиртовый раствор нитроглицерина используется в качестве сосудорасширяющего средства, взрывчатыми свойствами не обладает.
В технике глицерин получают гидролизом (омылением) природных жиров и масел:
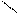 СН2—О—С =O СН2—ОН
СН2—О—С =O СН2—ОН
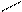
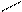 ½ R ½ О
½ R ½ О

 СН—О—С =O + 3Н2О ® СН—ОН + 3R—C
СН—О—С =O + 3Н2О ® СН—ОН + 3R—C
½ R ½ ОН
 СН2—О—С =O СН2—ОН
СН2—О—С =O СН2—ОН
R глицерин кислота
Другой способ получения глицерина заключается в сбраживании глюкозы (полученной осахариванием крахмала) в присутствии, например, бисульфита натрия по схеме:
NaHSO3 CH2—CH—CH2
С6Н12О6 ¾¾® ½ ½ ½ + CH3—CН=О + CO2
OH OH OH уксусный альдегид
При этом С2Н5ОН почти не образует. В последнее время глицерин получают и синтетическим путем исходя из пропилена газов крекинга или пропилена, получаемого из природных газов. По одному из вариантов синтеза, пропилен хлорируют при высокой температуре (400-500 оС), полученный хлористый аллил путем гидролиза переводят в аллиловый спирт. На последний действуют перекисью водорода, которая в присутствии катализатора и при умеренном нагревании присоединяется к спирту по двойной связи с образованием глицерина:
СН3 CH2—Cl CH2—OH CH2—OH
½ +Cl2 ½ +NaOH ½ HO—OH ½
СН ¾® CH ¾® CH ¾¾® CH—OH
II -HCl II -NaCl II ½
CH2 CH2 CH2 CH2—OH
пропилен хлоритый аллиловый глицерин
аллил спирт
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 1847; Нарушение авторских прав?; Мы поможем в написании вашей работы!